脂质体纳米颗粒(LNPs)是一种用于递送治疗分子(如药物和RNA)的纳米级系统,具有将疏水性和亲水性分子分别包裹在核心和表面的能力。LNPs通过提高药物稳定性和靶向性来增强生物利用度和疗效,是制药等领域有前途的递送工具。
本案例旨在利用对冲射流混合器制备空载脂质体纳米颗粒(LNPs),通过精确控制水相和有机相的流速,合成具有特定物理化学特性(如粒径、多分散性指数PDI和包封率)的LNPs。这些空载LNPs将作为研究平台,用于优化LNPs的制备条件,评估不同脂质配方的效率和稳定性,以及为后续的药物或核酸包载实验奠定基础。
1、 配置有机相溶液:称取41mg (790.17 g/mol, 0.05 mmol)DSPC,19.7 mg胆固醇(386.65 g/mol, 0.05 mmol);溶于20mL 无水乙醇中。
2、 使用两支10 mL的注射器,分别吸取水相和有机相(乙醇相)溶液,并安装到注射泵上。
3、 连接管路:将注射器的前端通过管路连接到反应器的进液口,确保连接处无泄漏。


图1. 反应器和注射泵通过管路连接的实验场景图。
4、 实验组1:控制总流速(Total Flow Rate,TFR)为20 mL/min,水相为15 mL/min,乙醇相为5 mL/min, 使得流速比(Flow Rate Ratio,FRR)为3:1, 收集2mL样品;设定水相为16.66 mL/min,乙醇相为3.33 mL/min;使得流速比为5:1,收集2mL样品;
5、 实验组2:控制总流速(TFR)为6 mL/min,水相为4.5 mL/min,乙醇相为1.5 mL/min, 使得流速比(FRR)为3:1,收集2 mL样品;设定水相为5 mL/min,乙醇相为1 mL/min;使得流速比(FRR)为5:1,收集2mL样品;
6、 将收集到的样品置于纯水中进行稀释以除去乙醇,样品与纯水的体积比为1:50。最终对其进行DLS表征。
样品 | 总流速(mL/min) | 水相:有机相流速比 | 纳米粒径(d,nm) | PDI |
1-1 | 20 | 3:1 | 126 | 0.122 |
1-2 | 20 | 5:1 | 106 | 0.143 |
2-1 | 6 | 3:1 | 144 | 0.067 |
2-2 | 6 | 5:1 | 110 | 0.154 |
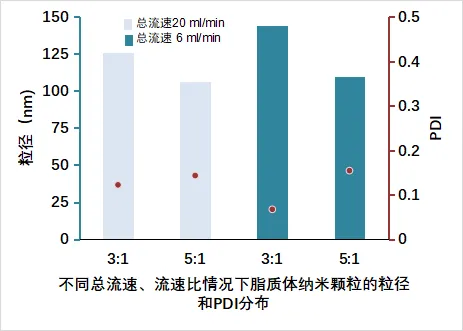
总流速、流速比对纳米颗粒粒径和PDI的影响
i) 对于所有样品,PDI<0.2, LNP平均尺寸小于150 nm,总体上呈单分散分布;
ii) 在总流量一致的情况下,提升水相:有机相流速比,均可减小LNP尺寸;
iii) 在流速比一致的情况下,提高总流量,有助于减小LNP尺寸;
● 前沿拓展
脂质体纳米颗粒的未来前景广阔,对药物输送和治疗领域具有以下几个影响:
* 个性化医疗:脂质体纳米颗粒可以定制以将特定药物输送到目标组织或细胞,从而实现个性化治疗方法。 这可能会带来更有效、更精确的治疗方法,并减少副作用。
* 联合疗法:脂质体纳米粒子可用于同时递送多种药物,从而实现针对多种疾病途径或机制的联合疗法。 这可以改善癌症等复杂疾病的治疗效果。
* 基因治疗:脂质体纳米颗粒已显示出为基因治疗应用提供遗传物质(例如 RNA 或 DNA)的前景。 通过实现靶向基因编辑或表达,这可能会彻底改变遗传性疾病和其他疾病的治疗。
* 再生医学:脂质体纳米颗粒可用于输送干细胞或生长因子,用于再生医学应用,例如组织修复或再生。 这可能为治疗损伤或退行性疾病开辟新的可能性。
总体而言,脂质纳米颗粒的持续研究和开发在推进药物输送和治疗方面具有巨大潜力,从而为多种疾病提供更有效和更有针对性的治疗。
[1]Tenchov, R., et al. Lipid Nanoparticles─From Liposomes to mRNA Vaccine Delivery, a Landscape of Research Diversity and Advancement, ACS Nano 2021, 15, 11, 16982–17015.
[2]https://insidetx.com/review/complete-guide-to-understanding-lipid-nanoparticles/
[3] Yang. et al. Formulation of Nanoparticles Using Mixing-Induced Nanoprecipitation for Drug Delivery. Ind. Eng. Chem. Res. 2020, 59, 9, 4134-4149.