
导读:
数字核酸检测技术以其绝对定量能力和无需校准的特点,为病原体的快速识别提供了有力工具。尽管已经开发了多种集成数字核酸检测技术,但在自动化和分析通量方面仍然存在限制。为了应对这些挑战,近期,广州市第一人民医院刘大渔研究员、徐邦牢教授团队提出了一种创新的数字-液滴微流控装置,该装置结合了数字微流控(DMF)模块和液滴微流控模块,旨在提升检测过程的自动化程度和分析通量。相关研究以“Rapid Detection of Uropathogens Using an Integrated Multiplex Digital Nucleic Acid Detection Assay Powered by a Digital-to-Droplet Microfluidic Device”为题目,发表在期刊《Analytical Chemistry》上。
本文要点:
1、本研究提出了一种创新的数字-液滴微流控装置,该装置由底部的数字微流控(DMF)模块和顶部的液滴微流控模块组成。
2、引入样品后,在DMF模块中完成核酸提取和洗脱,然后将核酸洗脱液分配并与多种扩增试剂混合,为下一步的检测做准备。
3、随后,反应液滴通过出液口被输送到液滴微流控模块的样品入口,然后由注射器真空产生的负压驱动液滴微流控模块内的四个并行单元中的液滴生成。
4、使用该装置执行一种结合环介导等温扩增(LAMP)技术的集成多重数字液滴核酸检测(imDDNA),以同时测定四种尿路病原体,即大肠杆菌、铜绿假单胞菌、肺炎克雷伯菌和粪肠球菌。
5、imDDNA的整个过程在75分钟内完成,检测范围跨越5个数量级(9.43×10–2.86×104拷贝/μL),并且在对批量临床标本的检测中与常规方法相比显示出91.1%的高一致性。
6、imDDNA操作简单、定量准确,在实现病原体快速检测方面具有潜在优势。
全文总结/概括:
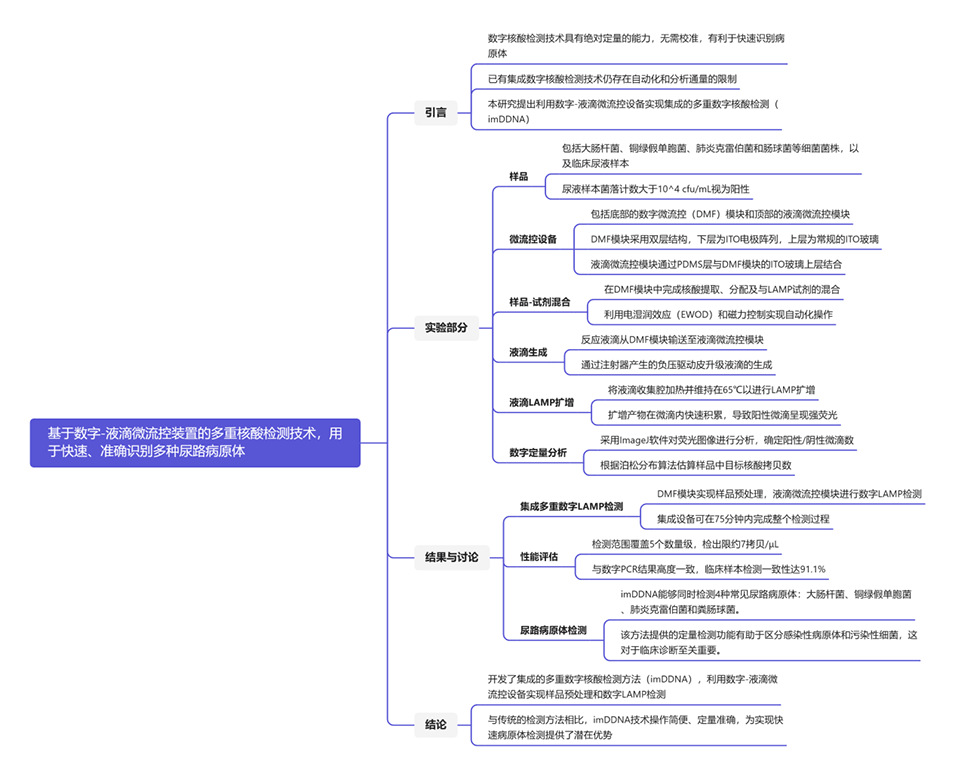
集成多重数字液滴核酸检测技术(imDDNA)具有以下主要优势:
1、快速检测:整个检测过程在75分钟内完成,显著缩短了病原体检测的时间,提高了检测效率。
2、高灵敏度和宽检测范围:检测范围覆盖5个数量级,能够检测从极低到较高的病原体拷贝数,增强了检测的灵活性和适用性。
3、操作简便:设备通过自动化设计,减少了手动操作步骤,降低了对专业技术人员的需求,使得非专业人员也能轻松进行准确的病原体检测。
4、定量准确性:利用数字微流控技术,imDDNA能够提供精确的定量结果,提高了检测的准确性和可重复性。
5、多重病原体同时检测:利用该技术能够同时检测多种尿路病原体,提高了检测效率和临床实用性。
6、高一致性:与传统方法相比,imDDNA显示出高达91.1%的一致性,验证了其在临床样本检测中的可靠性。
7、减少交叉污染风险:集成的设备减少了样本在多步骤检测过程中的暴露,从而降低了交叉污染的风险,提高了检测的可靠性。
8、现场测试潜力:设备的集成性和便携性使其适用于现场检测,扩展了检测的应用场景,特别是在资源有限的环境中。
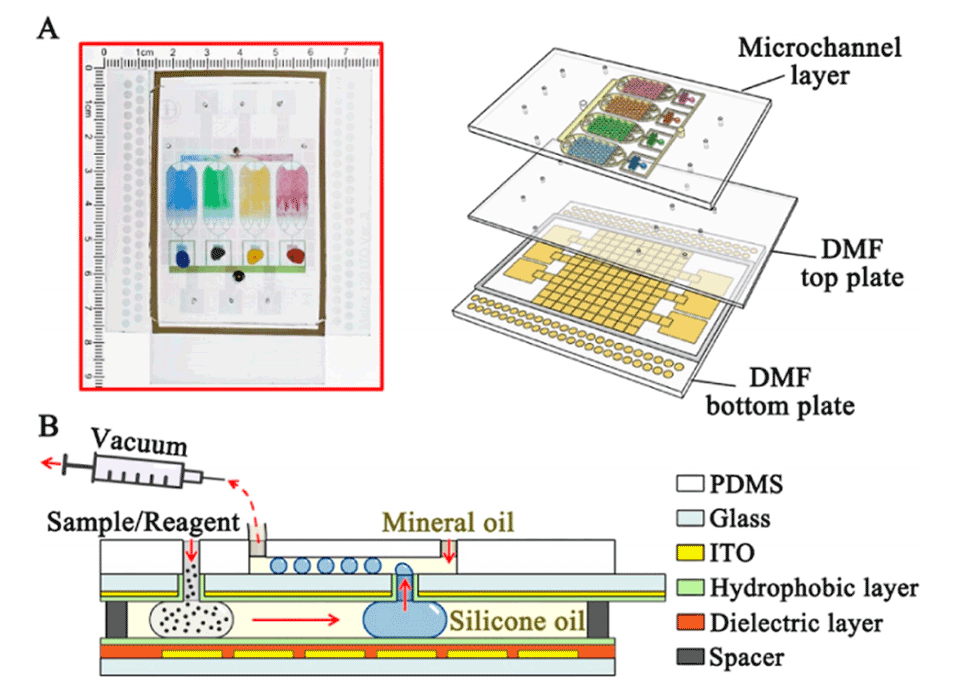
图1.微流控系统示意图。
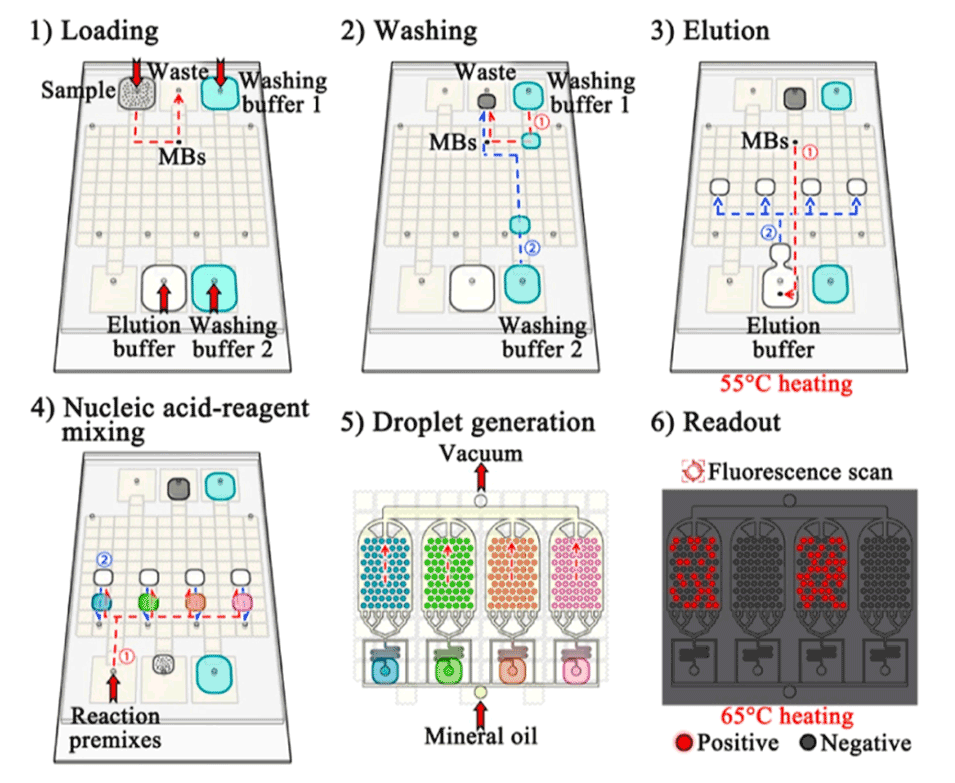
图2.imDDNA的程序。

图3.利用数字-液滴微流控装置执行集成多重数字LAMP。
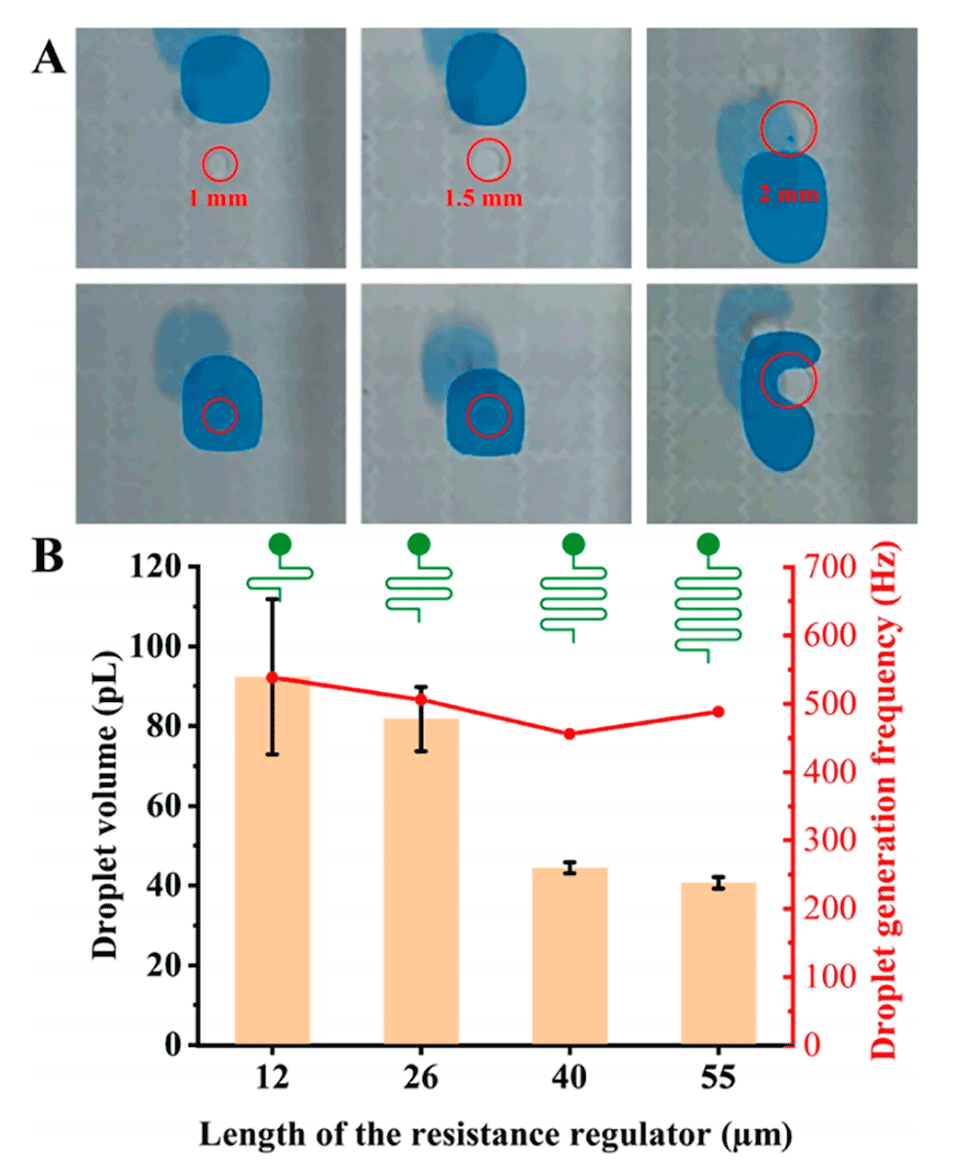
图4.集成参数的优化。
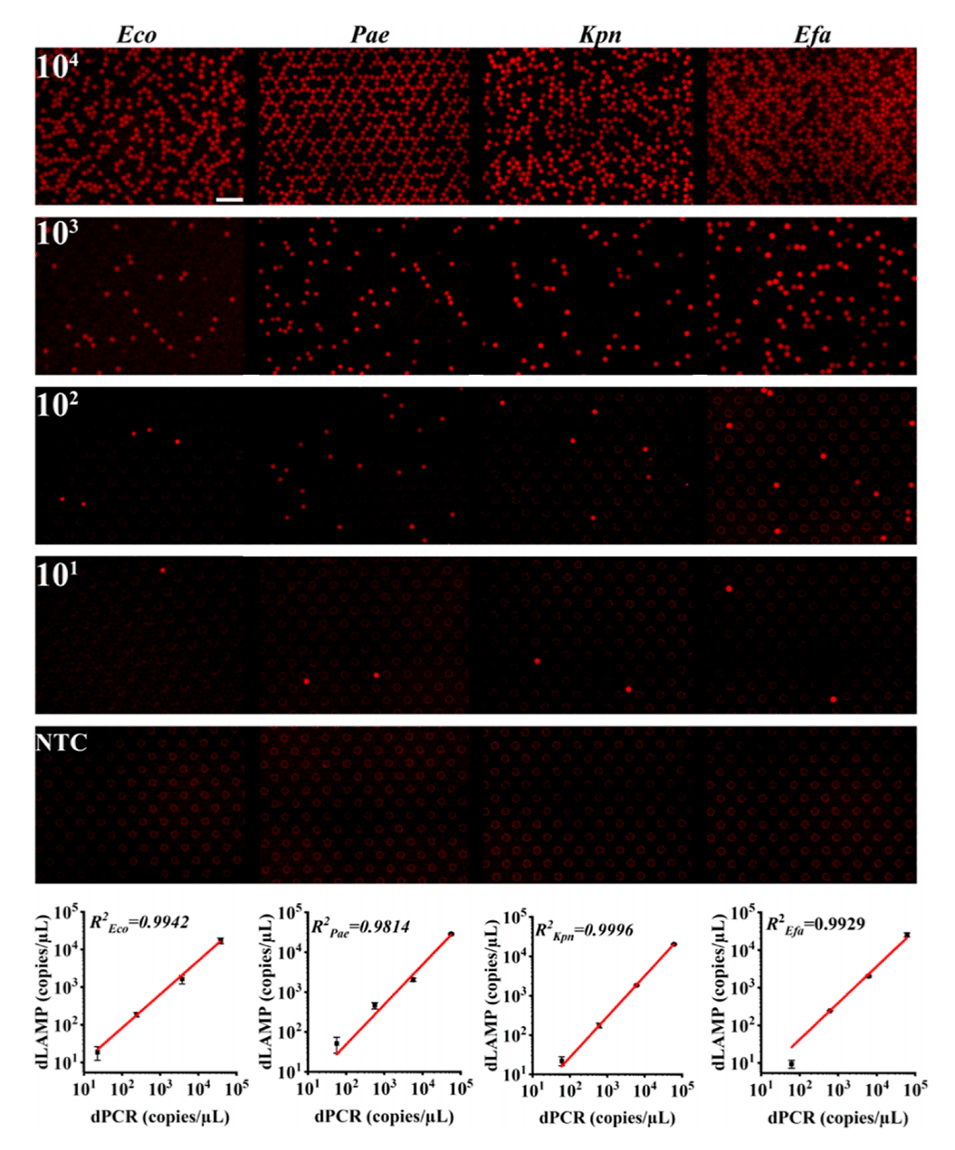
图5.不同浓度下各种细菌DNA的液滴LAMP结果。顶部:荧光显微镜图像显示了来自不同细菌菌株的连续稀释基因组DNA样本的液滴LAMP检测结果;(曝光时间:500ms,ISO:400;比例尺=200μm);底部:imDDNA定量与数字PCR的相关性(n=3)。
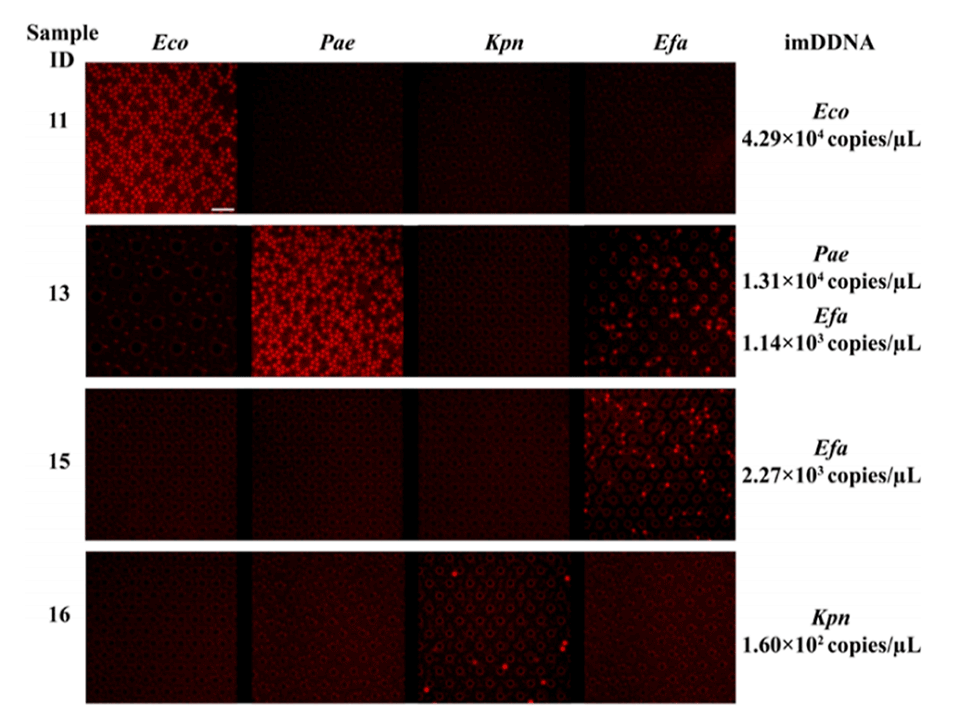
图6.尿路病原体阳性病例的代表性imDDNA结果(暴露时间:500ms,ISO:400;比例尺:200μm)。
原文链接:https://doi.org/10.1021/acs.analchem.4c02578














