输血是医院最常见的医疗程序之一,其中红细胞(RBC)是最常用的输血产品。由于血型不匹配可能导致免疫反应、红细胞溶解甚至患者死亡,因此正确匹配血型至关重要。A型和B型血的红细胞表面抗原由不同的寡糖组成,而O型血液的H抗原缺少这些末端糖,因此可以普遍输注给具有相同Rh血型的受血者。为了提高O型血的供应,科学家们提出通过酶促去除A型和B型红细胞的末端糖来实现血型转换。然而,早期的酶在活性和特异性方面存在不足,限制了其临床应用。近年来,通过筛选人肠道宏基因组库,研究人员发现了一种高效的双酶系统,能够在更温和的条件下实现红细胞的转换。这一进展为开发新的酶以生成普遍适用的O型血提供了新的可能性。

近期,有研究人员开发了一个简单且稳健的超高通量微流控筛选系统,用于寻找能够将B型红细胞转化为通用O型红细胞的高效α-半乳糖苷酶。通过这一系统,成功鉴定出α-1,3-半乳糖苷酶PvGH110,为血液供应提供了一种高效、简便的酶发现工具。相关研究以“Ultrahigh-Throughput Single Emulsion Droplet Screening for the Discovery of New B Antigen Cleaving Enzymes”为题目,发表在期刊《ACS Catalysis》上。
本文要点:
1、本研究开发了一种基于油包水单乳液液滴的超高通量微流控筛选系统,用于发现能够切割B型抗原的α-半乳糖苷酶。
2、该系统将来自人肠道宏基因组文库的单细胞与含有荧光基团的B型抗原四糖基质一同封装在微滴中,利用商用微流控细胞分选仪对含有活性酶的荧光微滴进行分选。
3、通过该筛选系统,鉴定并表征了一种来自人肠道微生物群的α-1,3-半乳糖苷酶PvGH110,该酶能够有效地将B型红细胞转化为O型。
4、该微流控筛选系统简单高效,可在非专业实验室中使用,为发现能够生成通用O型血液的酶提供了一种有前景的工具。
该微流控筛选系统的工作流程如下:
1、样本准备:从人肠道微生物组中提取单细胞,并与所需的实验组分(如底物、缓冲液、抗生素和耦合酶)混合。
2、液滴生成:使用商业化的聚二甲基硅氧烷(PDMS)微流控芯片,通过流聚焦接头将混合液与油相结合,生成油包水单乳液液滴。
3、液滴收集与培养:收集生成的液滴,并在适当条件下进行孵育,以促进细胞生长、裂解及酶的潜在水解反应。
4、液滴排序:通过高通量的微流控芯片对液滴进行排序,利用荧光激发检测到的荧光液滴被引导到收集腔,而非目标液滴则流入废液腔。
5、液滴去乳化:对收集到的荧光液滴进行去乳化处理,分离出细胞和反应产物。
6、后续筛选:将去乳化后的液滴中的克隆接种到琼脂平板上,进行二次筛选,以确认α-半乳糖苷酶活性。
7、候选酶的鉴定与表征:对筛选出的候选酶进行测序和功能表征,以确认其在B型红细胞转换为O型红细胞中的有效性。
这项研究中使用的微流控筛选系统与传统的酶筛选方法相比,具有以下优势:
1、高通量:微流控系统能够在较小的体积内生成大量液滴,从而实现对大量样本的同时筛选,显著提高了筛选效率。
2、减少试剂消耗:通过在pL级别的液滴中进行反应,微流控系统大幅降低了底物和试剂的使用量,相比传统方法节省了资源。
3、自动化流程:该系统实现了从样本准备到结果读取的全自动化,减少了人为操作的复杂性和潜在错误。
4、灵敏度提高:微流控技术通过在较小的反应体积中实现高灵敏度检测,能够识别低浓度的酶活性。
5、防交叉污染:采用油包水体系,有效防止了在筛选过程中可能出现的交叉污染,确保了结果的准确性。
6、实时监测与排序:系统能够实时监测液滴中的荧光信号,并根据活性进行排序,快速筛选出目标酶。
7、适应性强:微流控系统可以灵活调整实验条件,适应不同类型的酶和底物,具有广泛的应用潜力。
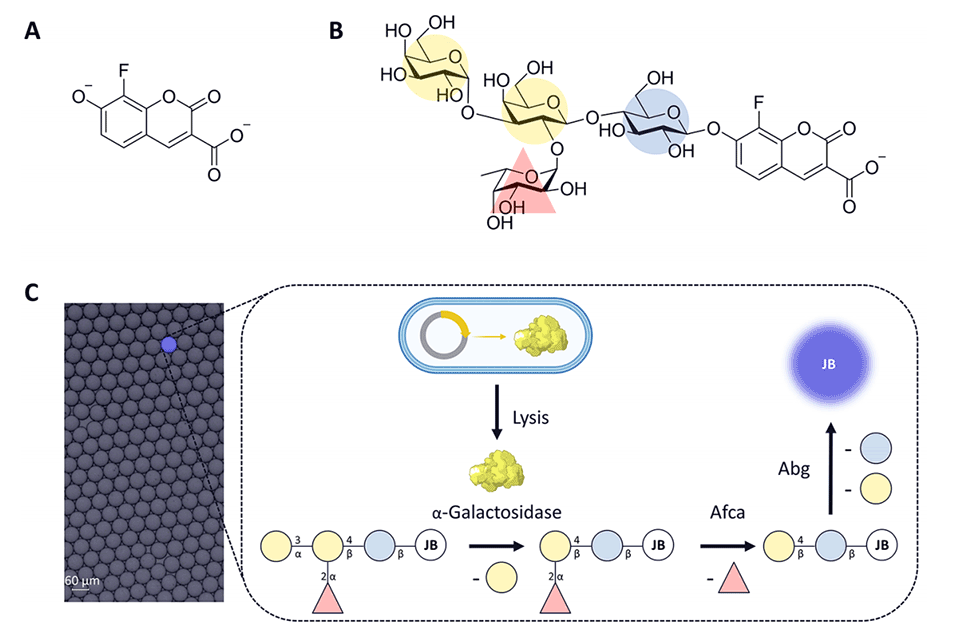
图1.展示了用于筛选B抗原切割酶的底物和方法。
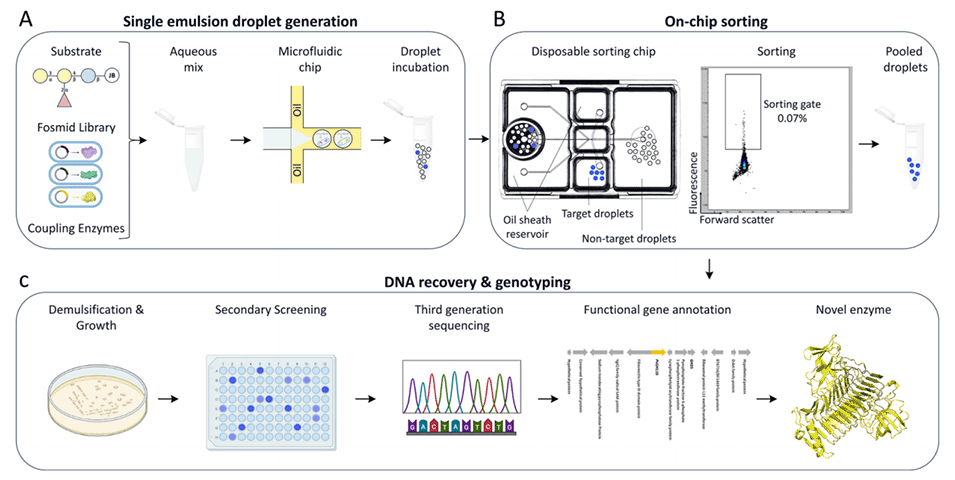
图2.描述了用于功能宏基因组筛选的超高通量筛选平台的工作流程,旨在发现新的B抗原切割酶。
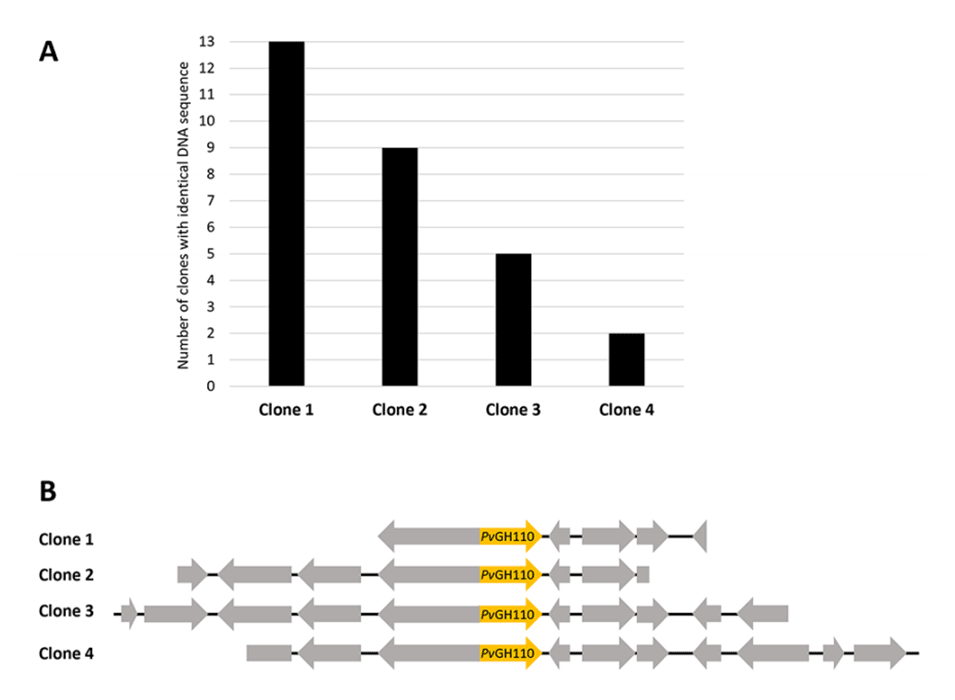
图3.展示了液滴微流控筛选结果:鉴定出四个不同的插入片段,编码来自Phocaeicola vulgatus的独特α-半乳糖苷酶(PvGH110)。
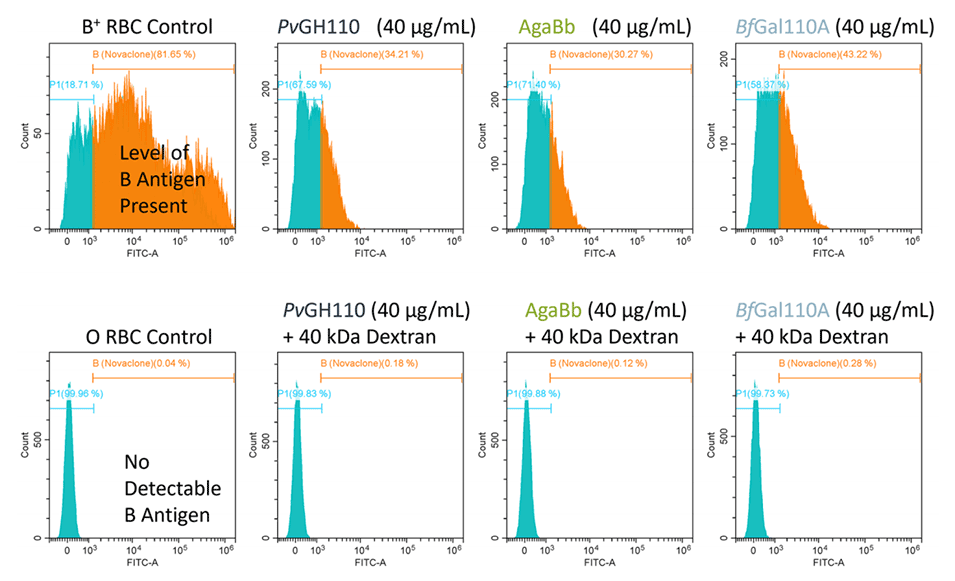
图4.测试了GH110酶在B+ RBC上的活性。
原文链接:
https://doi.org/10.1021/acscatal.4c02165














