在单细胞水平上对患者来源的类器官(PDO)进行基因测序已成为推断原始器官细胞异质性和提高癌症精准医学的一种很有前途的方法。不幸的是,由于PDO的起始数量有限以及建立过程不受控,现有的单细胞测序技术在处理临床样本时效率低下。

近期,中国医学科学院北京协和医院胸外科梁乃新团队与北京理工大学魏泽文团队合作,开发了一种基于微流控芯片的自动化系统(称为MASSO),用于对源自患者的类器官(PDO)进行单细胞水平的全基因组测序。相关研究以“Microfluidic Chip-Based Automatic System for Sequencing PatientDerived Organoids at the Single-Cell Level”为题目,发表在期刊《Analytical Chemistry》上。
本文要点:
1、本研究提出了一种基于微流控芯片的自动化系统(MASSO),用于在单细胞水平上对患者来源的类器官(PDO)进行基因测序。
2、MASSO系统在单一微流控芯片上完成PDO的建立、培养、消化及单细胞的分离、裂解和全基因组扩增,避免了珍贵PDO的损失,并确保了高质量的扩增结果。
3、通过自动化操作,消除了人为错误,提高了数据的重复性,促进了实验室研究与临床实践之间的衔接。
4、本研究首次成功实现了对肺癌PDO的单细胞全基因组测序,结果显示MASSO不仅能够识别常见的癌症相关突变,还能发现影响药物反应的特定突变,为理解PDO及其原始器官的细胞异质性奠定了基础。
使用MASSO系统对患者来源的类器官(PDO)进行基因测序的主要优势包括:
1、一体化操作:MASSO系统将PDO的建立、培养、消化以及单细胞的分离、裂解和全基因组扩增等所有步骤集成在一个微流控芯片(OSA-Chip)中,避免了在不同设备之间转移时可能造成的损失和污染。
2、高质量扩增:通过在芯片上进行全基因组扩增,确保了单细胞扩增的高质量,这对于准确识别突变至关重要。
3、自动化控制:MASSO系统的全自动化操作消除了人为错误,提高了实验数据的重复性,从而缩小了实验室研究与临床实践之间的技术差距。
4、高效处理:该系统能够高效处理来自临床样本的PDO,特别是在起始数量有限的情况下,克服了传统单细胞测序技术的效率低下问题。
5、精准识别突变:MASSO不仅能够识别常见的癌症相关突变,还能发现影响药物反应的特定突变,为精准医学提供了重要的技术基础。
OSA-Chip通过其独特的设计和功能支持PDO(患者来源的类器官)的培养和单细胞处理。具体来说,OSA-Chip由三个主要层次构成:阀门控制层、阀门膜层和样品处理层。这种结构使得OSA-Chip能够高效地执行PDO的建立、培养、消化以及单细胞的分离、裂解和全基因组扩增(WGA)。
PDO培养:OSA-Chip的PDO培养段包含多个培养腔室,能够在一个芯片上同时培养多个PDO。细胞与Matrigel的混合物被注入到培养腔室中,随后通过重力填充,确保细胞均匀分布并支持PDO的生长。
单细胞处理:当PDO培养完成后,OSA-Chip通过注入消化酶将PDO解离为单个细胞。解离后的细胞被转移到单细胞处理段,OSA-Chip在此段中执行单细胞的捕获、裂解和WGA。每个单细胞处理单元都设计有单细胞隔离位点、细胞裂解室、缓冲中和室和扩增室,确保单细胞的高效处理和高质量的WGA。
通过将所有这些步骤整合到一个微流控芯片中,OSA-Chip不仅避免了在不同设备间转移时可能导致的细胞损失,还提高了单细胞处理的效率和准确性。这种集成化的设计使得OSA-Chip成为临床应用中高效、可靠的技术平台。
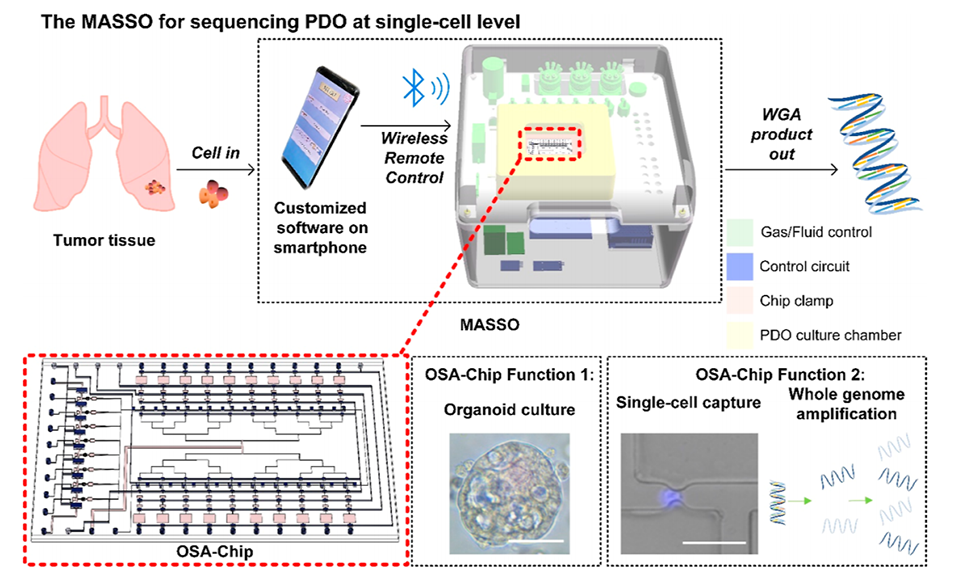
图1.基于微流控芯片的自动系统(称为MASSO)用于类器官的单细胞测序示意图。
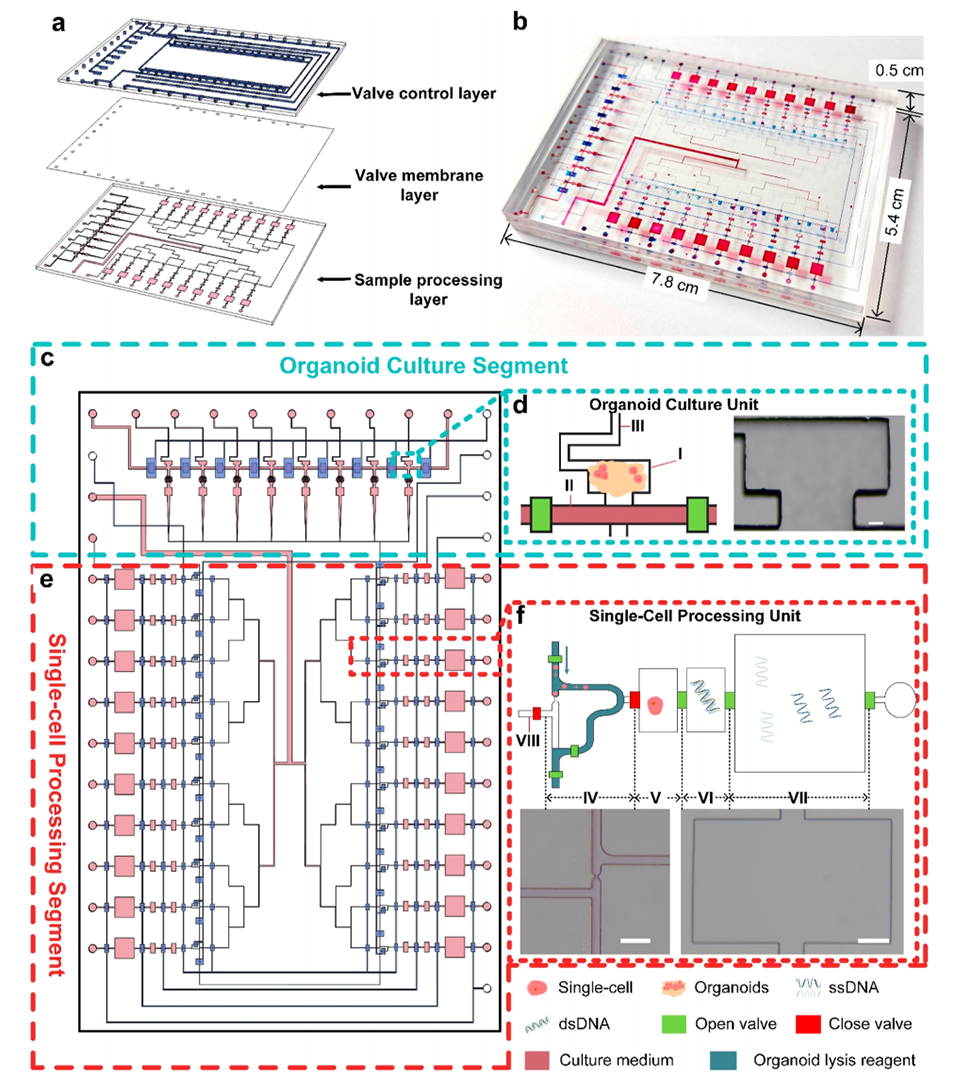
图2.微流控芯片(OSA-Chip)用于类器官培养、单细胞捕获和WGA。
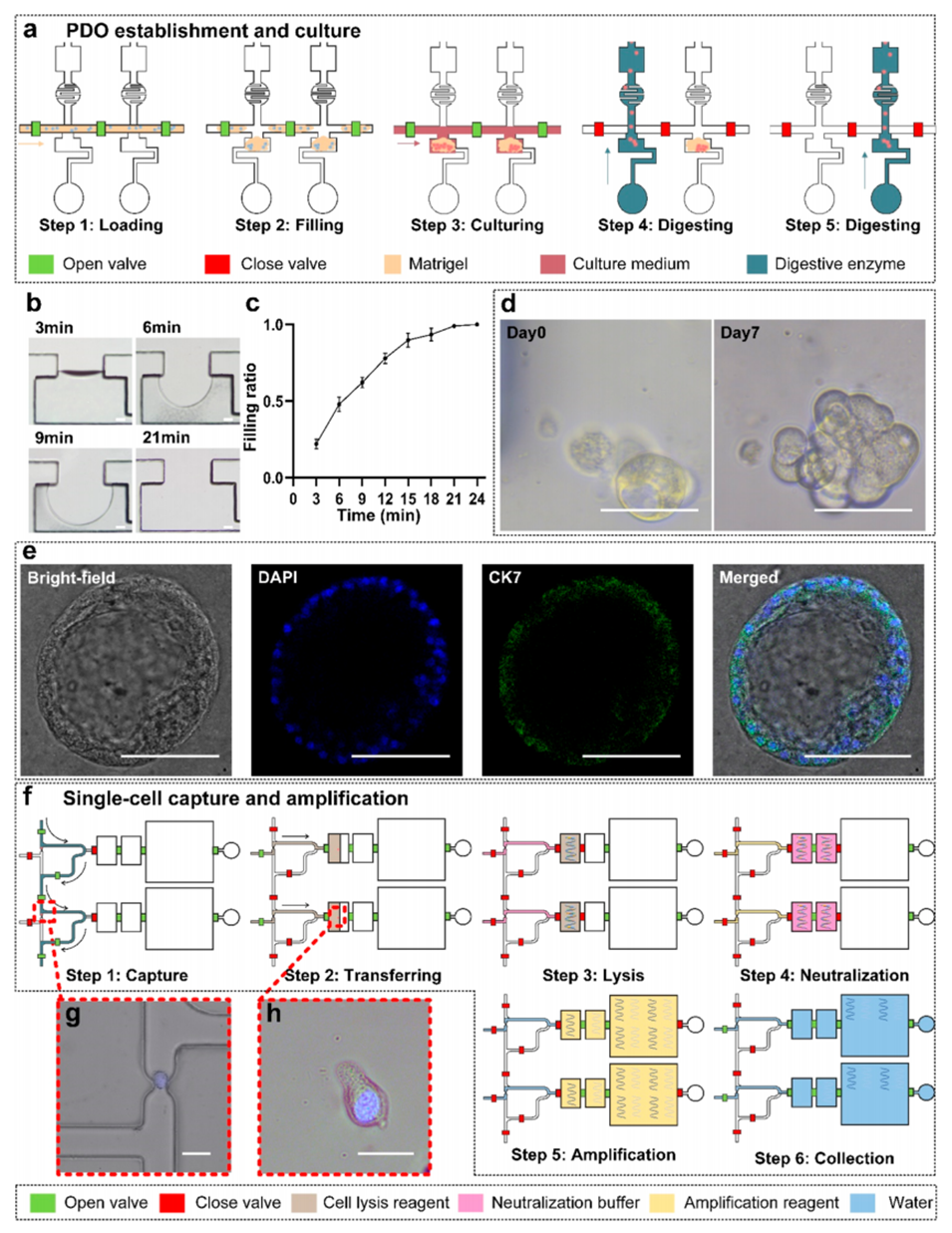
图3.OSA-Chip操作,包括PDO建立/培养、单细胞捕获和WGA。
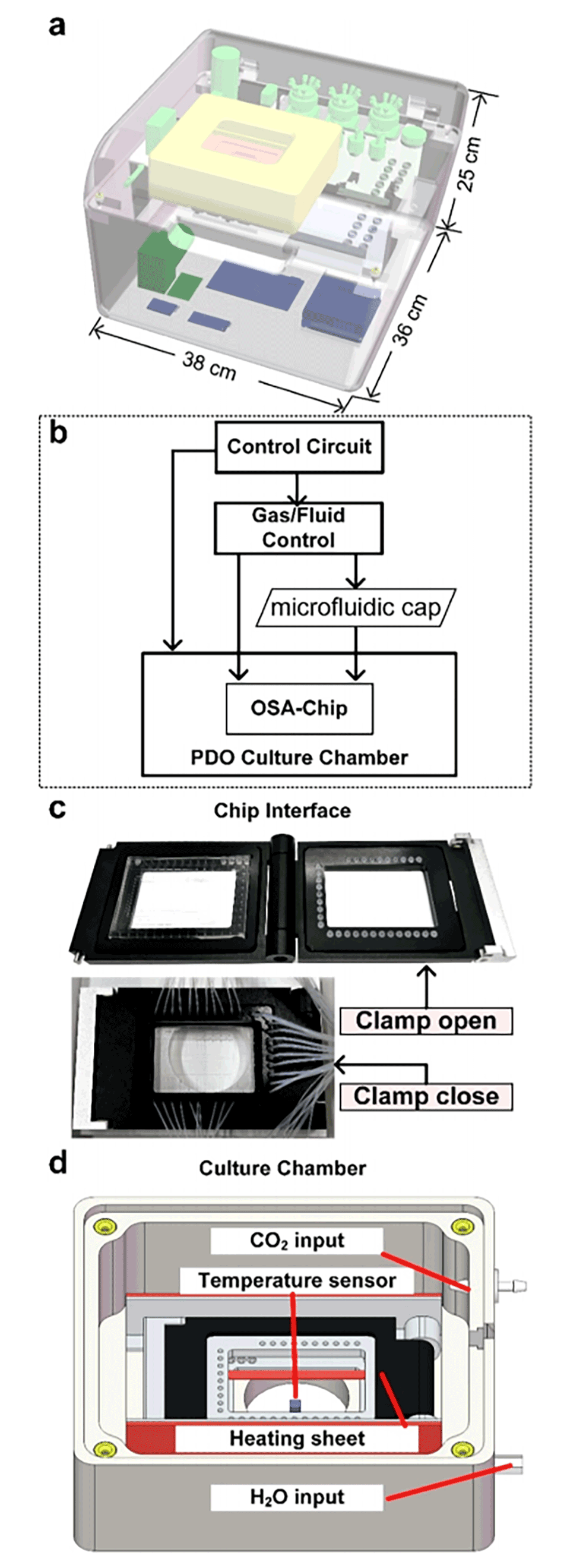
图4.MASSO及其组件。
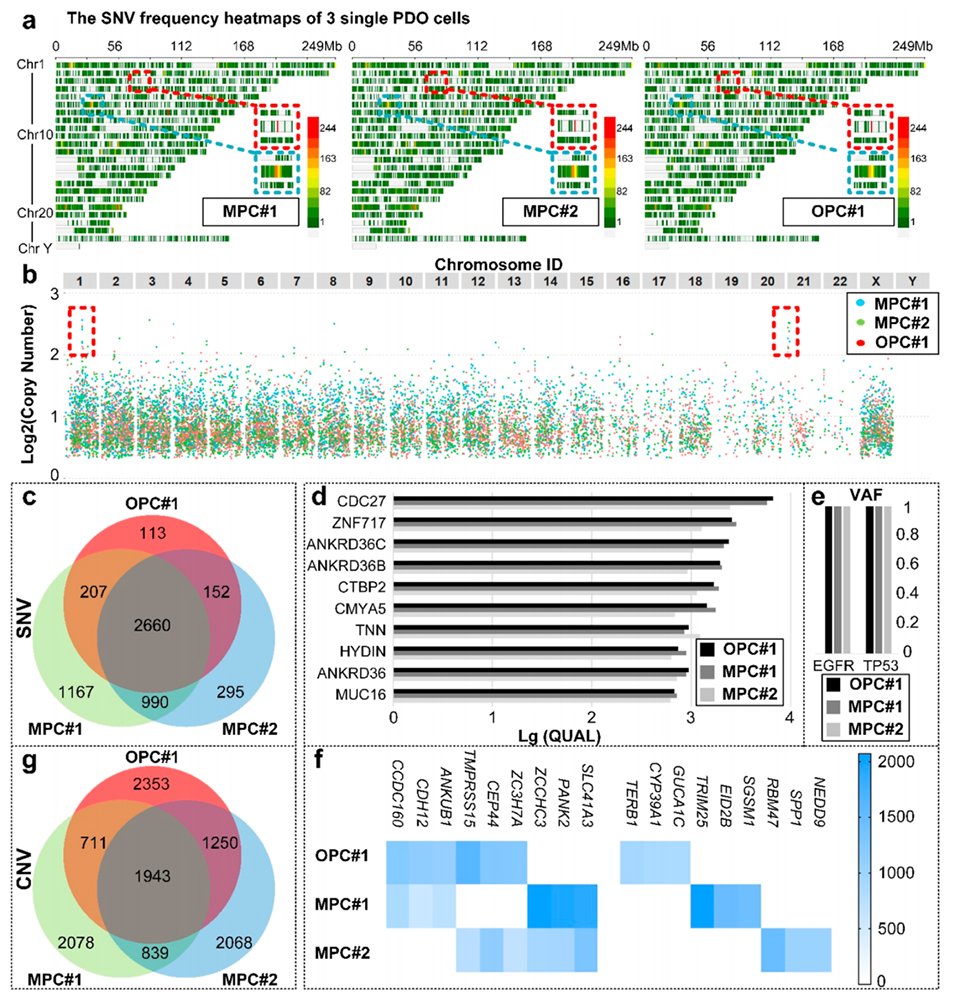
图5.3种PDO细胞的全基因组分析。
论文链接:https://doi.org/10.1021/acs.analchem.4c05111














