微流控纺丝水凝胶纤维可构建模拟血管、肌肉纤维或神经网络的纤维状组织,在组织工程和细胞移植领域极具应用价值。海藻酸盐因加工简便而被广泛用于制备纤维状水凝胶,但其存在细胞粘附性差、细胞-基质相互作用弱的问题,且这类材料需经交联处理,在生理条件下易发生离子溶出并丧失结构完整性。

为克服上述缺陷,该研究首次报道了通过微流控湿法纺丝制备纯壳聚糖纤维的方法,该方法无需使用交联剂,且所制纤维的细胞存活率可达85%,力学强度(695 MPa)也显著高于海藻酸盐纤维(2-4 MPa)。相关研究以“Pure Chitosan Microfluidic Spinning Affords Modular Core-Sheath Fibers and Hand-Crafted Scaffolds with Enhanced Fibroblast Compatibility”为题目,发表在期刊《Small》上。
本文要点:
1、该研究首次实现了无交联剂的纯壳聚糖微流控湿法纺丝,制备出模块化核壳结构纤维及可手工编织的支架材料,解决了海藻酸盐基水凝胶纤维细胞粘附性差、机械强度低、交联离子易溶出等痛点,为组织工程和细胞移植提供了新型生物材料。
2、研究团队设计PDMS微流控芯片,通过溶剂交换法实现壳聚糖纤维固化,制备出纯壳聚糖核壳纤维(Chs-Chs-MF)和氧化甲壳素纳米晶/壳聚糖复合核壳纤维(Chs-ChNC-MF),直径约200-250 μm;还可调控流率制备中空纤维,或在核/壳中负载亚甲基蓝等生物活性分子实现可控缓释。
3、表征结果显示,该纤维机械性能优异,干燥态Chs-ChNC-MF杨氏模量达695 MPa(远高于海藻酸盐纤维的2-4 MPa),湿态也有0.996 MPa,且结晶度提升至65%左右,鞘层流率提高可增强核内纳米晶的取向性;同时具备良好的加工性,可编织成纱布、卷曲为管状结构,水吸收性和水蒸气透过率适配生理环境,符合生物材料应用要求。
4、细胞相容性实验表明,HS-5骨髓成纤维细胞在纯壳聚糖纤维表面的存活率达85%,细胞粘附和铺展效果良好,而海藻酸盐纤维无活细胞留存;复合纤维因纳米晶改变表面特性,细胞存活率约65%,仍优于传统材料。
5、该研究以甲壳类废弃物衍生的壳聚糖为原料,契合联合国可持续发展目标,制备的纤维无需表面修饰即可支持细胞生长,可作为纤维状组织模板或人工组织构建的活单元,为自下而上的组织工程研究开辟了新方向,后续可进一步优化复合纤维的细胞相容性并验证药物递送的体外效果。
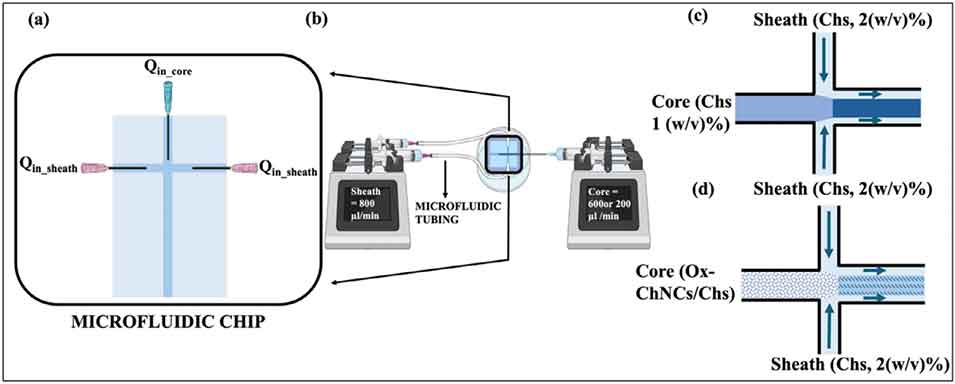
图1. 微流控湿法纺丝装置的示意图。(a) 微流控芯片;(b) 配备凝固浴的微流控湿法纺丝装置;(c) 制备Chs-Chs-MF的芯片接头放大图;(d) 制备Chs-ChNC-MF的芯片接头放大图。
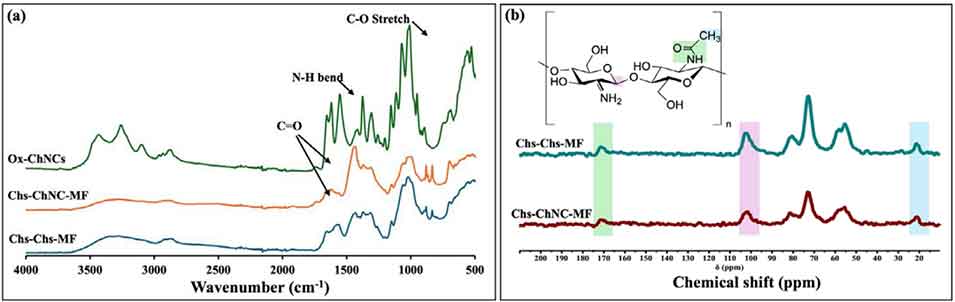
图2. (a) Ox-ChNCs、Chs-ChNC-MF和Chs-Chs-MF的傅里叶变换红外光谱图;(b) Chs-Chs-MF和Chs-ChNC-MF的13C光谱。
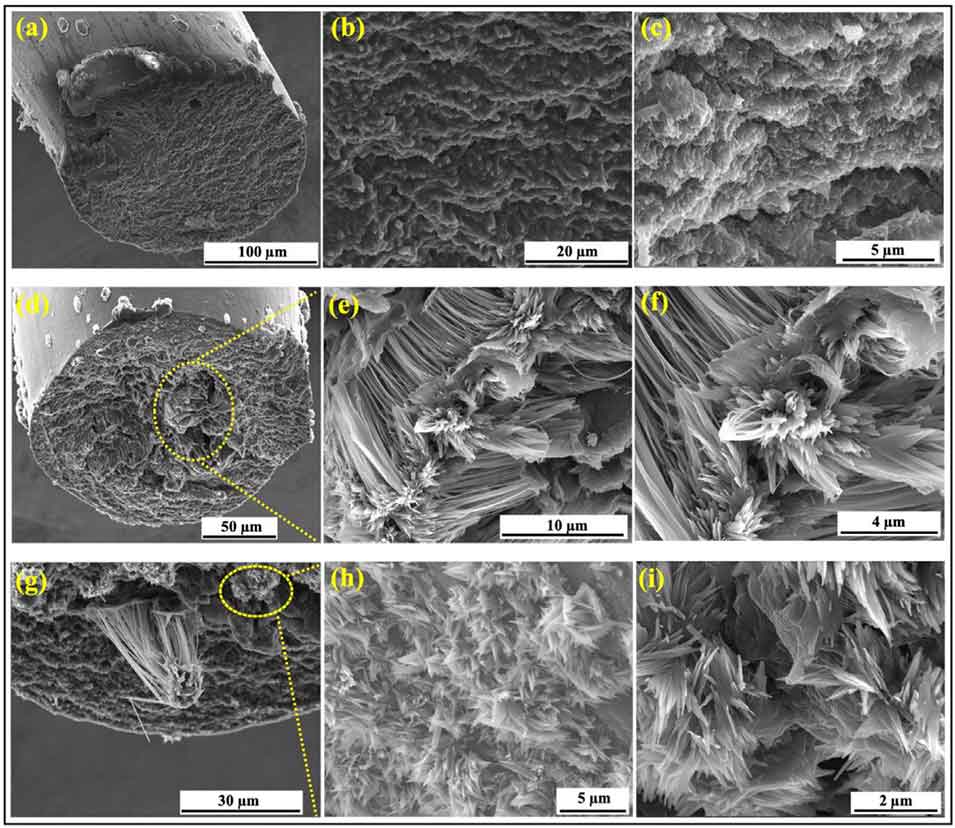
图3. (a) Chs-Chs-MF(鞘层流速800 μL/min,核层流速600 μL/min);(b)(c) Chs-Chs-MF的横截面;(d) Chs-ChNC-MF(核层为 1.5 (w/v)% Ox-ChNCs,流速200 μL/min,鞘层为壳聚糖);(e)(f) Chs-ChNC-MF的横截面;(g) 另一根Chs-ChNC-MF(比例尺= 30 μm,制备流速同上);(h)(i) 横截面放大图,比例尺分别为5 μm和2 μm。
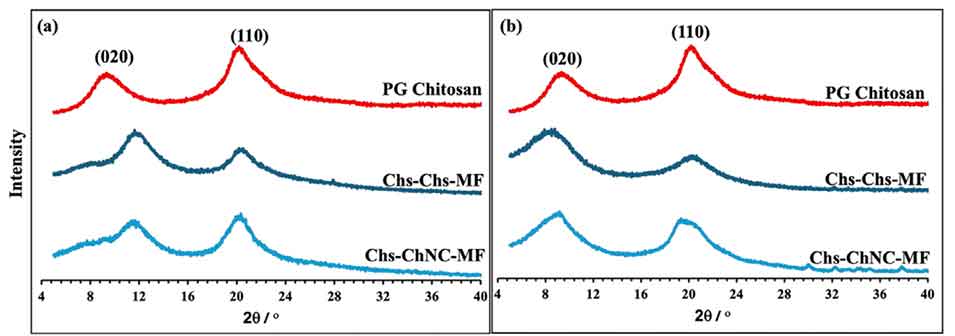
图4. PG壳聚糖、Chs-Chs-MF和Chs-ChNC-MF的X射线衍射图谱。(a) 纤维整体置于XRD样品架上的测试结果;(b) 纤维冷冻干燥并研磨成粉末后的测试结果。
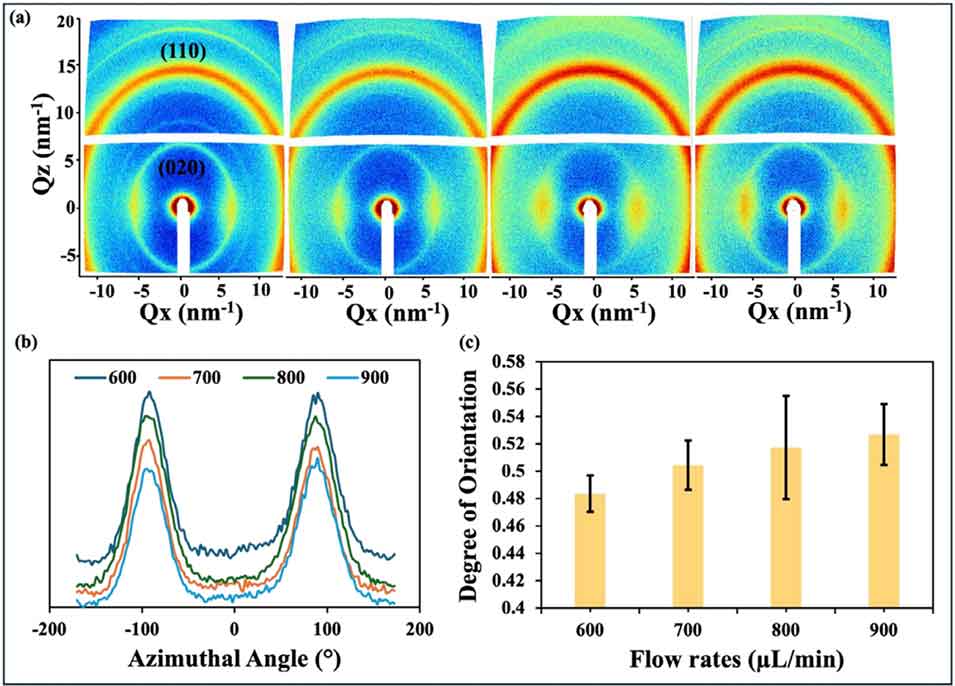
图5. (a) 垂直放置的Chs-ChNC-MF的二维广角X射线散射衍射图(从左至右,鞘层流速分别为600、700、800、900 μL/min);(b) 方位角峰的半高宽;(c) 由方位角强度分布计算得到的取向指数,数据为7次独立测量的标准差误差棒。
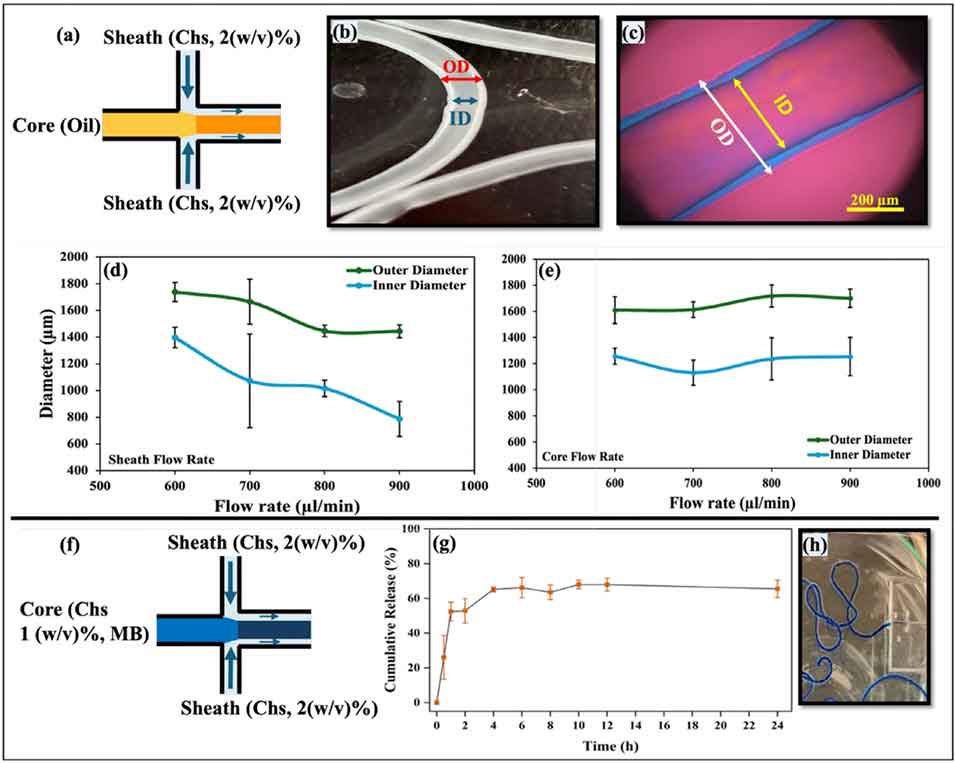
图6. (a) 壳聚糖-油复合纤维(Chs-oil-MF)的示意图;(b) 中空纤维实物图(核层流速600 μL/min,鞘层流速800 μL/min,普通手机拍摄);(c) 纤维的偏振显微镜图像;(d) 核层流速恒定700 μL/min时,改变壳聚糖鞘层流速制备的纤维内外径变化图;(e) 鞘层流速恒定800 μL/min时,改变油相核层流速制备的中空纤维内外径变化图;(f) 壳聚糖-亚甲基蓝复合纤维的示意图;(g) 亚甲基蓝的累积释放曲线(对应24 h的释放量);(h) 核层负载亚甲基蓝的纤维实物图,数据以平均值±标准差表示。
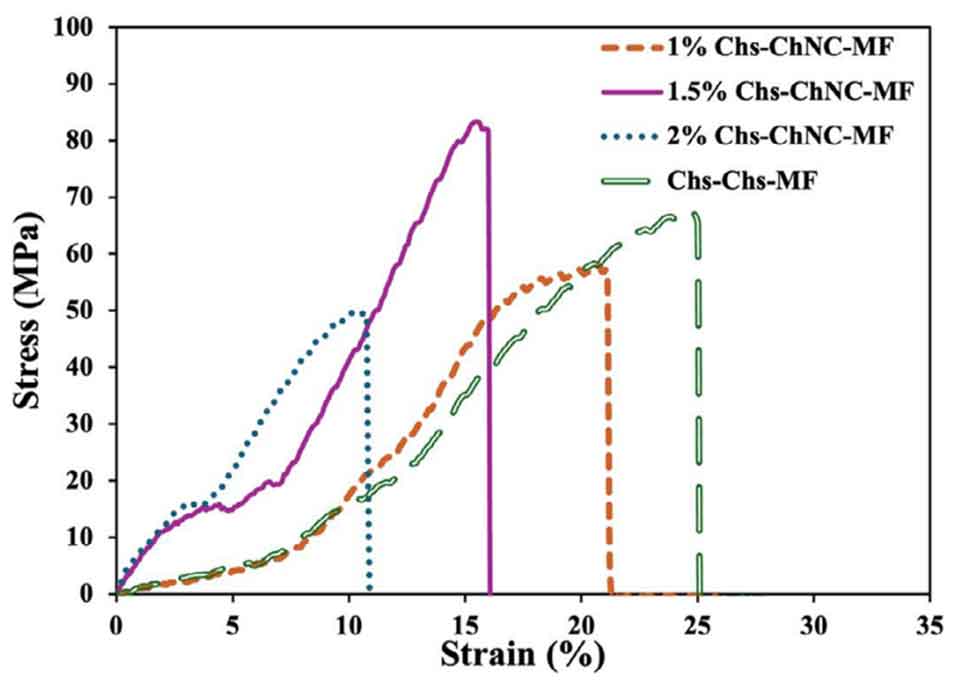
图7. 干燥态Chs-Chs-MF(鞘层流速800 μL/min,核层流速200 μL/min)及不同Ox-ChNCs浓度(1、1.5、2 (w/v)%)的干燥态Chs-ChNC-MF的应力-应变曲线。
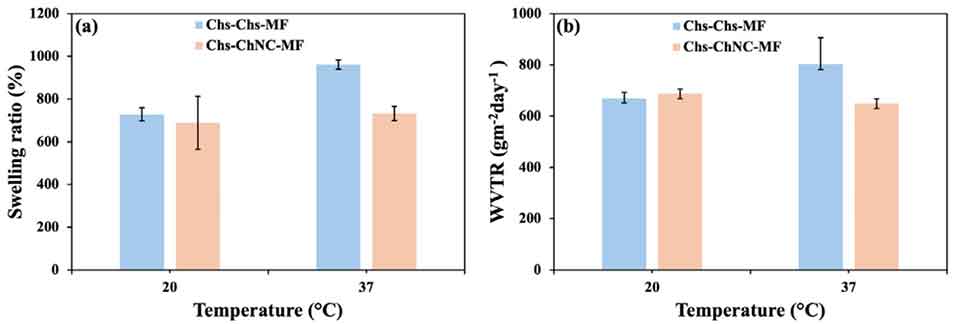
图8. (a) Chs-Chs-MF和Chs-ChNC-MF在20℃和37℃下浸泡8 h后的吸水性能;(b) Chs-Chs-MF和Chs-ChNC-MF制成的纱布在50%相对湿度、20℃和37℃条件下包裹玻璃瓶24 h后的水蒸气透过率,数据以平均值±标准差表示。
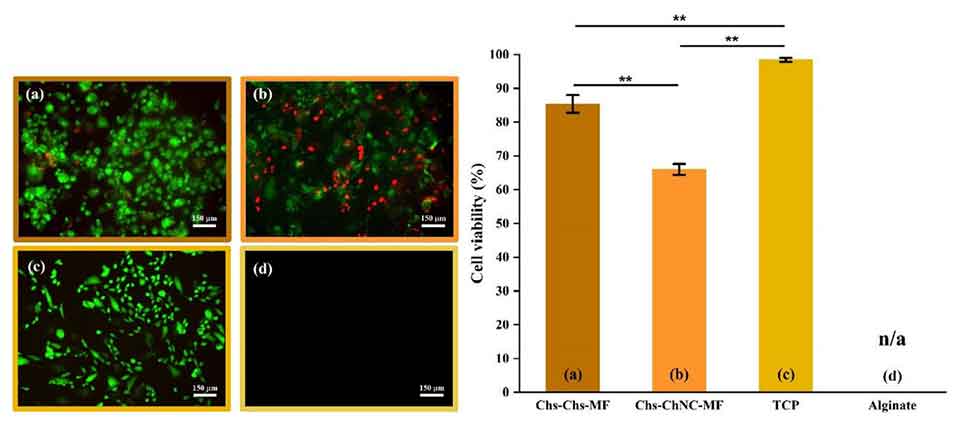
图9. 活/死(绿色/红色)细胞存活率分析。(a) Chs-Chs-MF;(b) Chs-ChNC-MF;(c) 组织培养塑料(TCP);(d) 海藻酸盐纤维。数据以平均值±标准差表示,采用单因素方差分析结合杜凯氏事后检验进行统计学分析(n=3,p<0.01)。
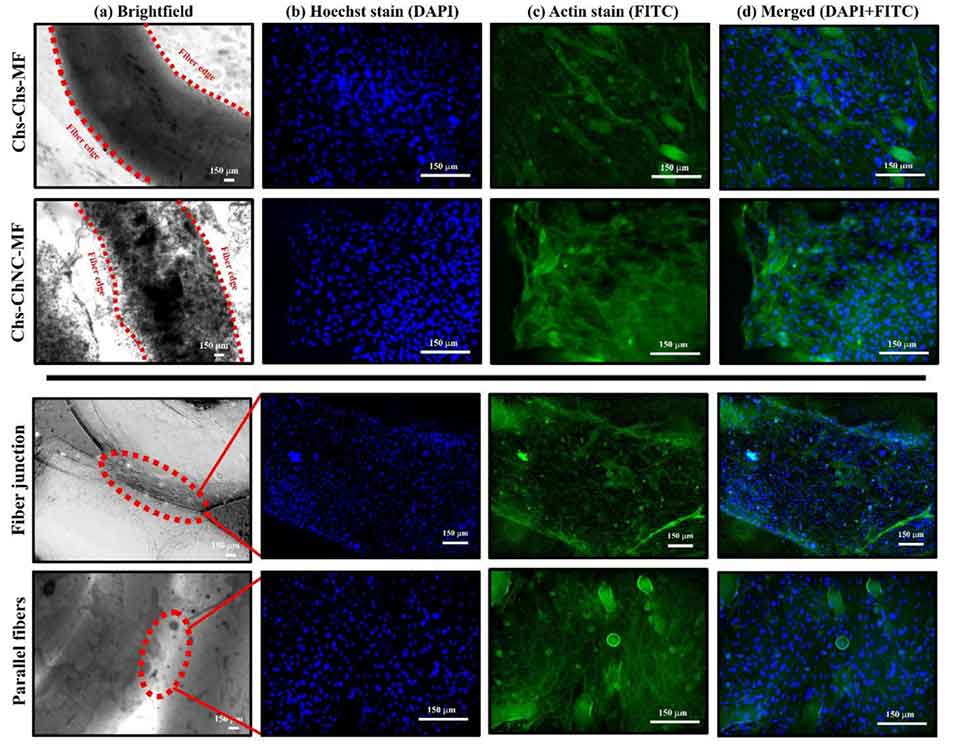
图10. Chs-Chs-MF和Chs-ChNC-MF基底上的细胞粘附及细胞骨架排布情况。(a) 明场图像勾勒出纤维边缘(红色虚线),标示观察区域;(b) Hoechst染色的细胞核(DAPI,蓝色),证实Chs-Chs-MF和Chs-ChNC-MF表面均有高密度细胞;(c) 肌动蛋白染色(FITC,绿色),可见壳聚糖纤维表面细胞骨架铺展良好,而Chs-ChNC-MF表面细胞的细胞骨架结构较不明显;(d) DAPI与FITC通道的融合图像,显示纤维表面及相邻纤维接触区域均有连续的细胞覆盖。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/smll.202510372
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














