SH2超亲体蛋白(SH2S)是一种基于SH2结构域改造的工程多肽,表现出显著增强的酪氨酸磷酸化蛋白结合能力,可用于治疗多种癌症。然而,其临床应用受限于血清稳定性差和肿瘤靶向不足等问题。

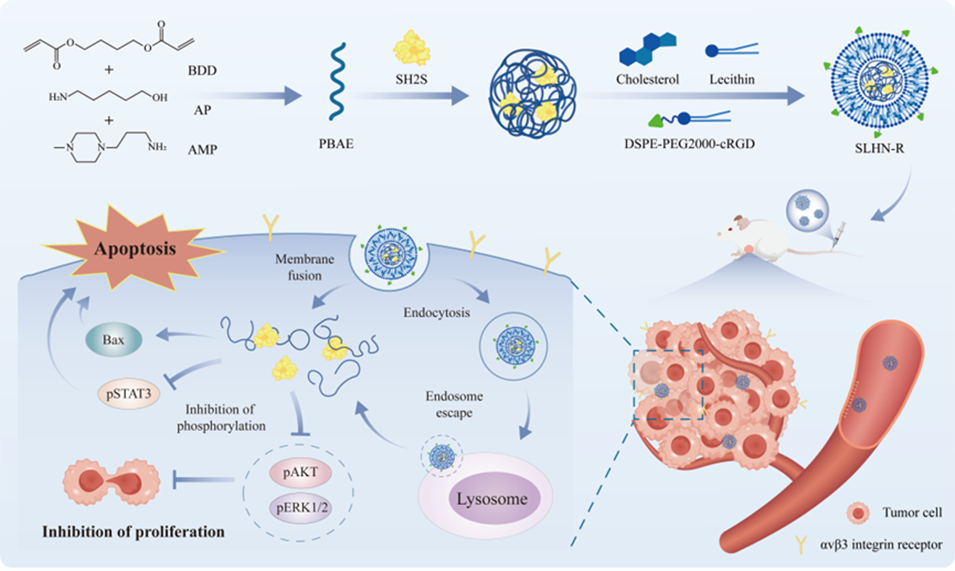
鉴于此,台州学院曹轩教授联合华中科技大学谭松巍教授等人,利用改良微流控技术构建了负载SH2S的脂质杂化纳米递送系统(SLHN),并通过cRGD修饰获得靶向型SLHN-R,成功突破SH2S血清稳定性差、肿瘤靶向不足的瓶颈。该递送系统可高效将SH2S递送至乳腺癌细胞,阻断致癌信号通路、重塑肿瘤免疫微环境,在低剂量下即可实现显著的乳腺癌抑瘤效果。相关研究以“Engineered lipid hybrid nanoparticles for targeted delivery of SH2 superbinder and breast cancer therapy”为题目,发表在期刊《Journal of Nanobiotechnology》上。
本文要点:
1、该研究构建了一种脂质杂化纳米粒(SLHN)递送系统,用于靶向输送SH2超亲体蛋白(SH2S)治疗乳腺癌,显著提升其体内稳定性、肿瘤靶向性与治疗效果。
2、研究首先针对SH2S血清稳定性差、无肿瘤靶向、入胞效率低的临床瓶颈,采用微流控技术,以阳离子聚合物PBAE、脂质、胆固醇为原料,制备包裹SH2S的脂质杂化纳米粒SLHN,并进一步修饰cRGD得到靶向型SLHN R;经表征确认纳米粒粒径均一、蛋白包封率高、结构稳定且生物相容性好。
3、随后探明SLHN的入胞机制:主要通过膜融合+网格蛋白介导内吞进入乳腺癌MCF 7、4T1细胞,入胞效率远高于游离SH2S;进入细胞后,SH2S竞争性取代内源SH2结构域蛋白,阻断AKT、ERK、STAT3磷酸化,诱导肿瘤细胞凋亡、抑制增殖与迁移。
4、体内动物实验显示,SLHN R的肿瘤靶向富集能力显著增强,组织穿透更深;0.5 mg/kg低剂量即可达到游离SH2S(10 mg/kg)的抑瘤效果,且无明显肝肾毒性;同时可重塑肿瘤免疫微环境,促进CD8+T细胞浸润、驱动巨噬细胞向M1型极化。
5、联合治疗研究表明,SLHN R与抗PD L1抗体联用呈现显著协同抑瘤效应,抑瘤率大幅提升,为乳腺癌靶向+免疫联合治疗提供新策略。
6、该研究首次利用微流控技术构建了由阳离子聚合物(PBAE)与蛋白(SH2S、BSA)共组装的脂质杂化纳米粒体系,有效解决蛋白药物体内稳定性不足、靶向性差的递送难题,兼具低剂量、高靶向、强疗效、高安全性优势,为多肽类抗癌药物的临床转化提供可行方案。
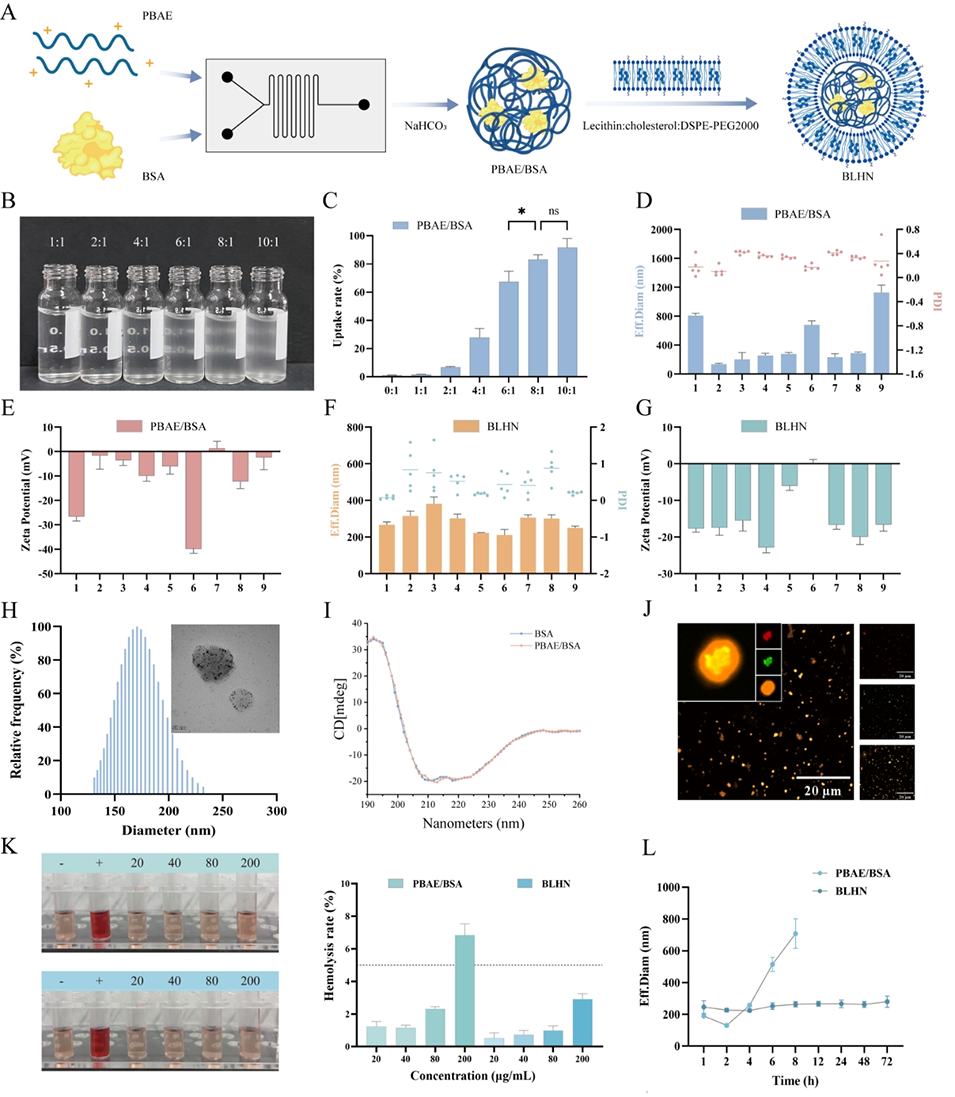
图1. 脂质杂化纳米粒的合成与筛选
SLHN 采用微流控技术联用薄膜分散法制备,全程为温和非共价组装,最大程度保护 SH2S 蛋白活性,具体步骤如下:
一、核心载体材料预制备
合成聚 β- 氨基酯(PBAE)以 1,4 - 丁二醇二丙烯酸酯(BDD)与 5 - 氨基 - 1 - 戊醇(AP)为原料,90℃氮气保护下反应 72h 得到中间体;再加入 1-(3 - 氨基丙基)-4 - 甲基哌嗪(AMP)室温反应 24h,经乙醚沉淀、离心、干燥纯化得到终产物 PBAE。
配置脂质原料按卵磷脂:胆固醇:DSPE-PEG2000 = 8:1:0.5的质量比,将三者溶于氯仿,旋蒸去除有机溶剂,形成均匀脂质薄膜。
二、微流控制备 PBAE/SH2S 复合物
将 PBAE 溶于 pH=6 的 LB 缓冲液(浓度 4.8mg/3mL),SH2S 蛋白溶于纯水(浓度 0.6mg);
两种溶液通过微流控芯片以300μL/min的流速混合;
出口处加入0.1M NaHCO₃调节体系 pH,完成 PBAE 与 SH2S 的静电组装。
三、薄膜分散法制备 SLHN
用上述 PBAE/SH2S 复合液对脂质薄膜进行水合,充分孵育后,脂质层包裹 PBAE/SH2S 内核,形成 SH2S 载药脂质杂化纳米粒(SLHN);
脂质总用量为蛋白质量的10 倍,保证包裹完全、粒径均一。
四、靶向型 SLHN-R 的制备(cRGD 修饰)
制备 SLHN 时,用Mal-DSPE-PEG2000替代普通 DSPE-PEG2000,通过巯基-马来酰亚胺共价反应将 cRGD 肽偶联于纳米粒表面,室温搅拌过夜,得到 cRGD 修饰的靶向纳米粒SLHN-R。
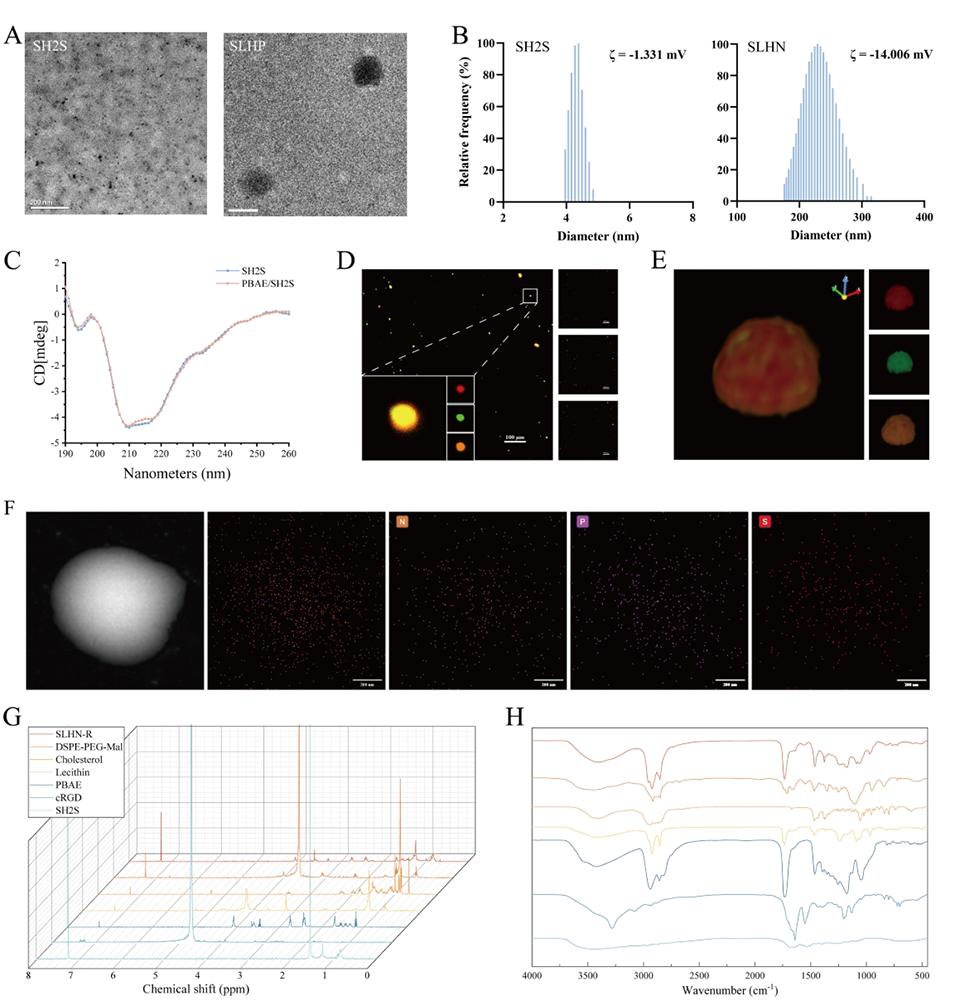
图2. SLHN 的表征
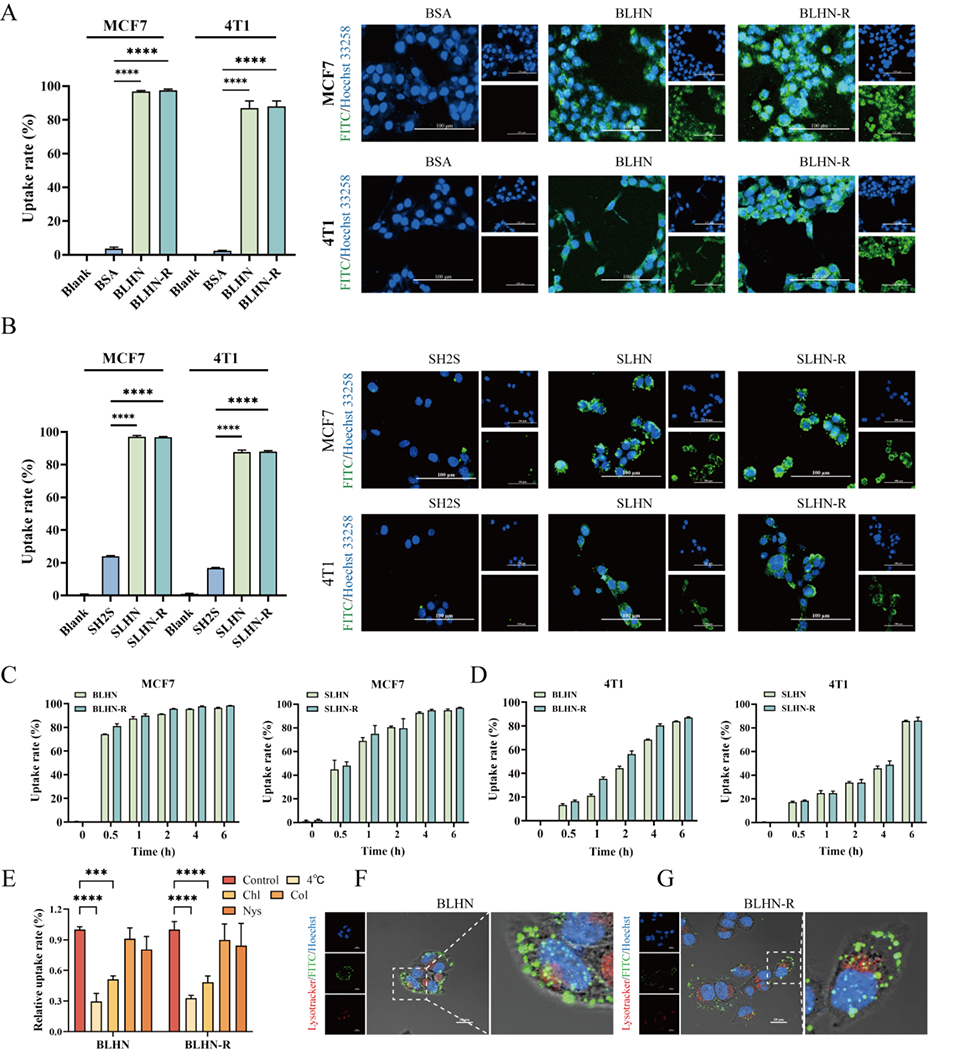
图3. 脂质杂化纳米粒增强蛋白向乳腺癌细胞内的递送
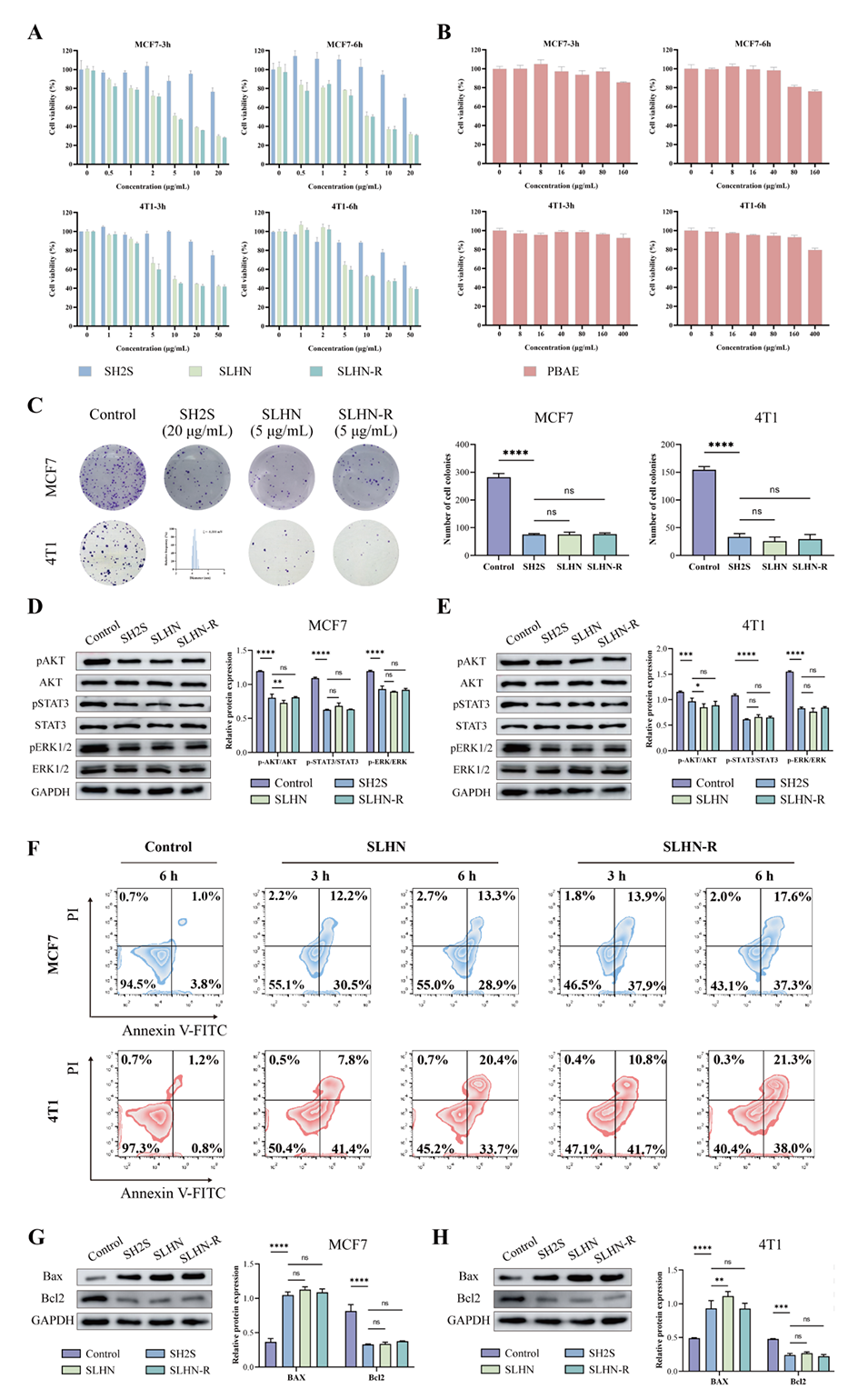
图4. 脂质杂化纳米粒抑制乳腺癌细胞增殖并诱导凋亡
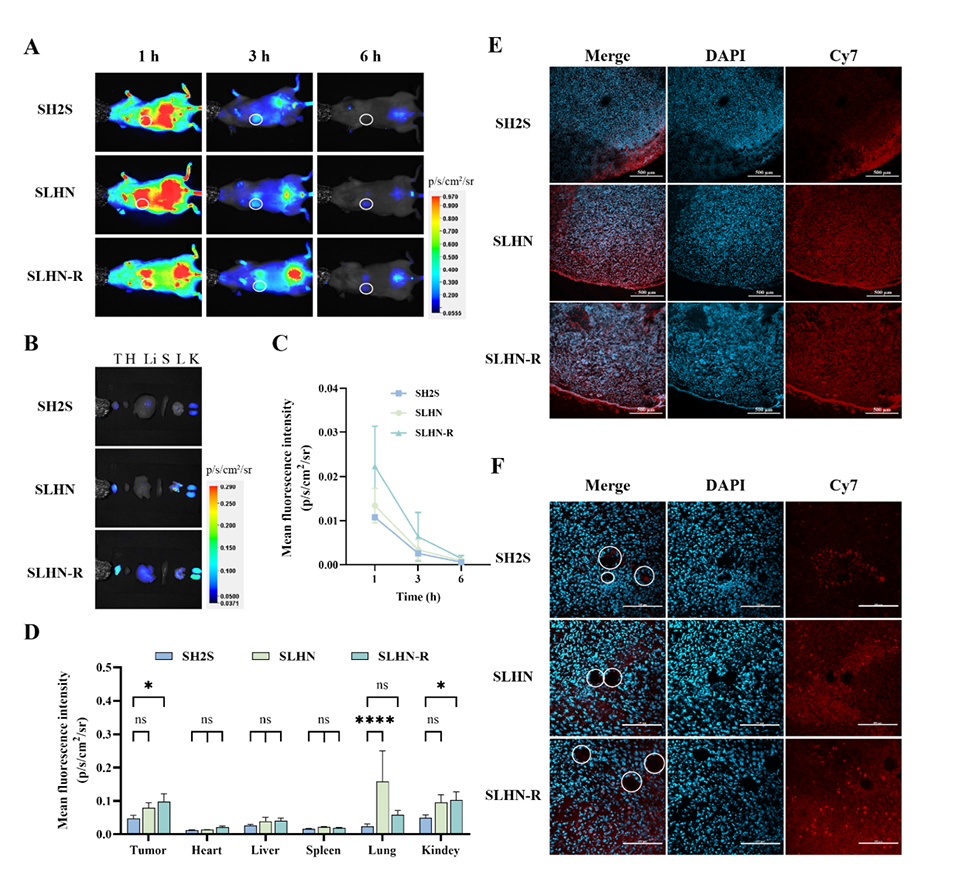
图5. 脂质杂化纳米粒改善 SH2S 蛋白在小鼠体内的分布
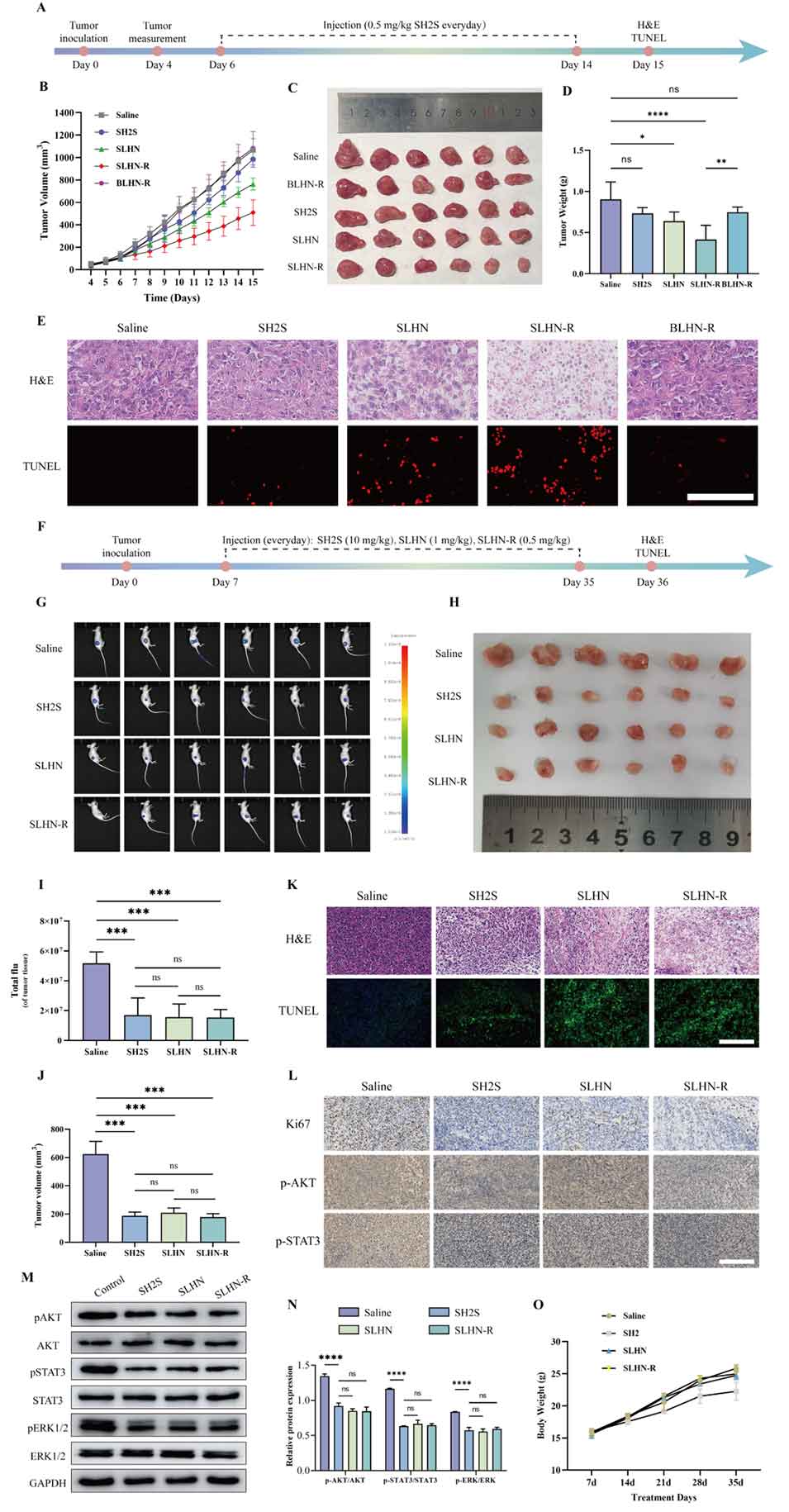
图6. 脂质杂化纳米粒在体内抑制 4T1 与 MCF7 肿瘤生长
论文链接:https://doi.org/10.1186/s12951-026-04249-w
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














