近日,华东理工大学顾震副教授、姜国俊副教授等研究人员在自动化水凝胶微囊制造领域取得重要进展,相关成果以“An intelligent microfluidic system for automated generation of hydrogel microcapsules with impedance-based feedback”为题,发表于国际权威期刊《Sensors and Actuators B: Chemical》。

这项研究介绍了一种用于自动生成水凝胶微囊(HGMCs)的智能闭环微流控系统。该系统创新性地整合了3D流动聚焦装置与阻抗检测技术,能够实时监控微囊生成状态并精确评估其核壳直径。研究团队开发了一个轻量化卷积神经网络(CNN)来识别微流控系统的运行状态,并结合模糊逻辑控制器(FLC)实现对生成过程的自主调节。实验结果表明,该系统具有极高的生成精度和稳定性,能显著降低微囊内外径的变异系数。此外,该平台已成功应用于间充质干细胞的自动化封装,证明了其在生物医药和材料科学领域的广泛应用潜力。这种低成本、无需标记且体积小巧的设计为大规模、高通量的微囊制造提供了高效的解决方案。
本文要点
1. 系统核心架构
该系统整合了以下关键组件,实现了微流控生成的闭环控制:
3D流式聚焦微流控芯片:通过3D打印工艺制造,并直接在芯片内集成了用于实时监控的微电极。
基于阻抗的反馈机制:利用阻抗传感代替传统的视觉反馈,具有成本低、无标记、无需额外光学系统以及对光敏感材料友好的优点。
轻量化卷积神经网络(CNN):用于实时分类微流控状态(如正常、气泡、不稳定等),并从阻抗波形中提取微胶囊的结构信息。
模糊逻辑控制器(FLC):一种无需精确模型的控制方法,能够处理微流控系统中的非线性和时间延迟,自动调节内相流速。
2. 技术优势与性能表现
高精度尺寸评估:系统可以评估微胶囊的核壳直径,分辨率达到 07 µm。
优异的结构均一性:闭环控制显著提高了微胶囊的质量,内径的变异系数(CV)≤1.87%,外径的CV ≤1.30%。
强大的鲁棒性:CNN模型在未经校准的“未知芯片”上仍能保持 09%的分类准确率,FLC控制策略能有效应对环境干扰和误分类。
3. 应用验证
细胞封装:系统已成功应用于间充质干细胞(MSCs)的自动精准封装,即便在缺乏先验流速设置知识的情况下,也能快速稳定地生成高均一性的细胞微胶囊。
多场景适用性:由于无需复杂光学组件,该系统体积小巧,适用于空间受限或大规模自动化的生产环境。
4. 结论与前景
该研究为水凝胶微胶囊的自动化、规模化制造提供了一种高效、低成本、可编程的解决方案。此外,该闭环控制策略具有通用性,未来可扩展至其他液滴生成系统(如W/O/W型液滴)及人工细胞系统的研究。
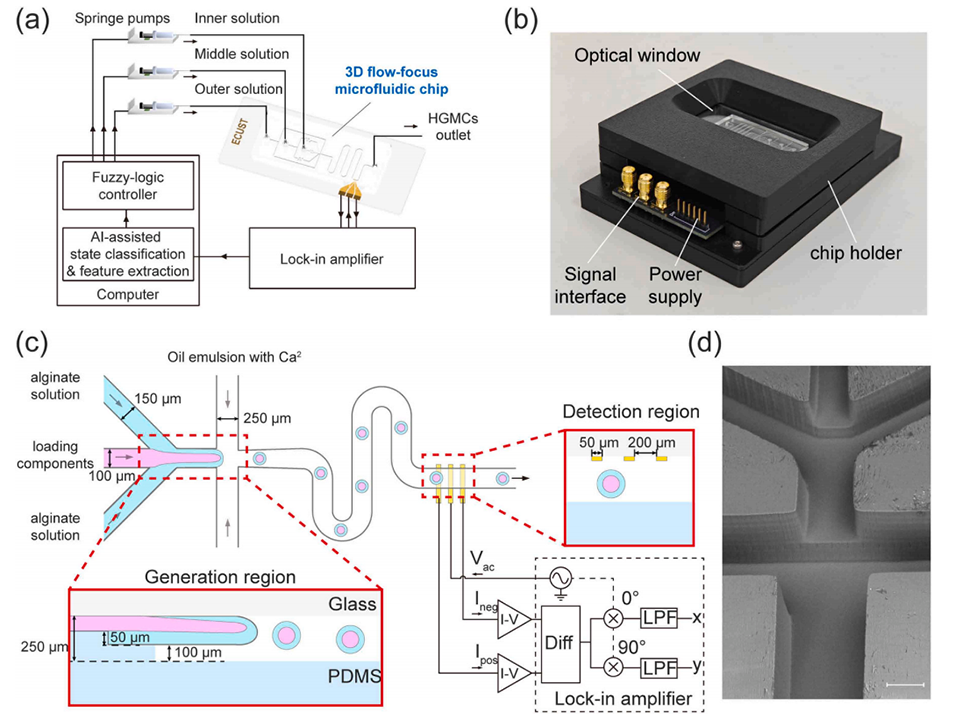
图1 特定核径的微胶囊制备系统。(a) 系统总览:计算机与锁相放大器、三台注射泵相连,驱动流体流经玻璃 - PDMS 微流控芯片;注射泵分别输送内相溶液、中间相溶液与外相溶液。(b) 3D 打印嵌磁夹具:固定倒置的微流控芯片,开设光学观测窗口,集成用于电流 - 电压转换的印制电路板,并配备专用信号与电源接口。(c) 倒置芯片细节:通道尺寸(宽 × 高),内相溶液通道 100 μm×100 μm、中间相溶液通道 150 μm×150 μm、外相溶液通道 250 μm×250 μm;玻璃基底上制备三根等距电极(宽 50 μm,间距 200 μm),通过差分锁相放大方案检测对称阻抗信号。(d) 微流控芯片制备区通道的扫描电子显微镜(SEM)图像;比例尺代表 100 μm。
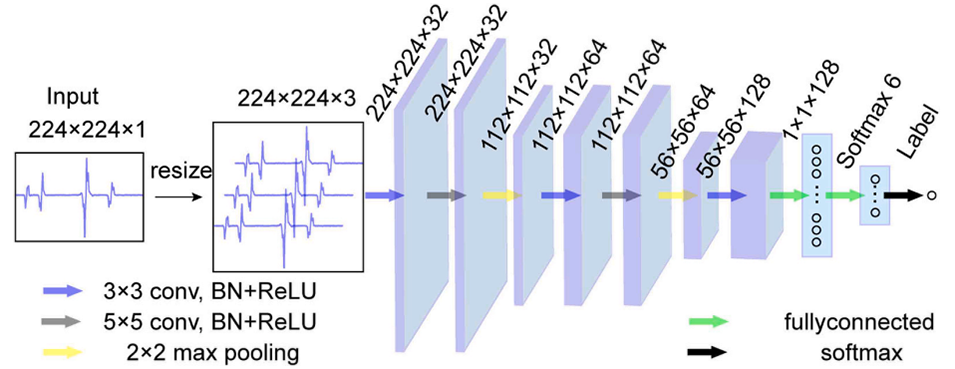
图2 卷积神经网络结构。单通道输入图像缩放至 224×224,经包含 3×3 与 5×5 卷积核、批归一化及 ReLU 激活函数的卷积块处理,穿插 2×2 最大池化层,后续接入全连接层与 Softmax 输出层,完成六分类任务。
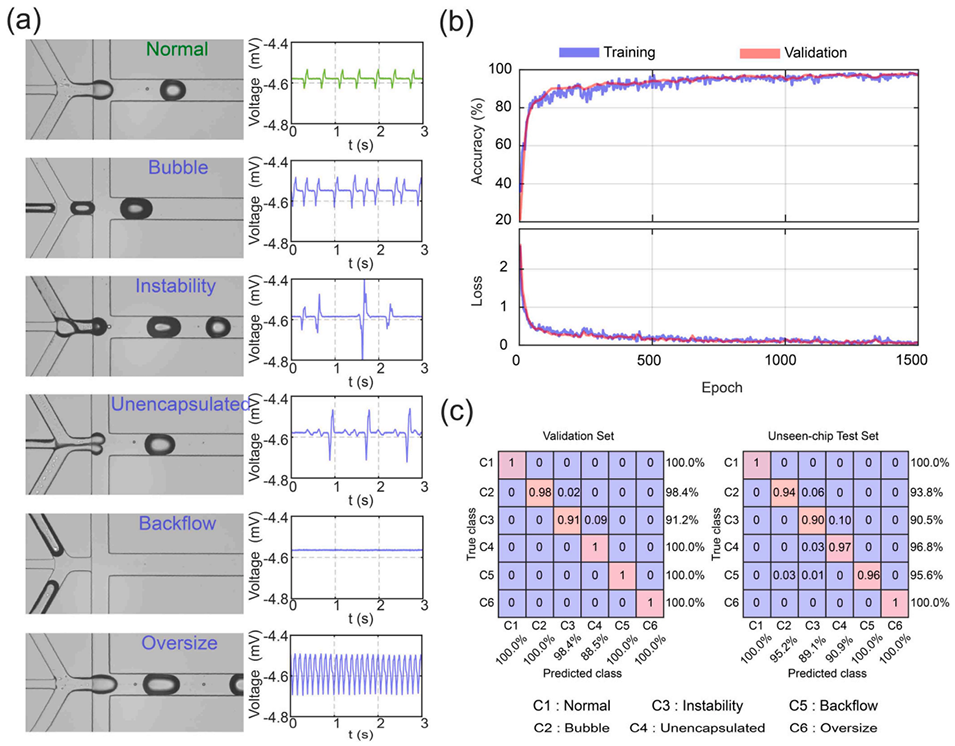
图3 基于阻抗波形的 CNN 微流控状态分类性能。(a) 微流控六种状态(正常、气泡、不稳定、未包载、回流、尺寸过大)的代表性显微镜图像(左)与对应阻抗波形(右),各状态具有特征鲜明的信号特征。(b) 轻量化 CNN 的训练/验证准确率与损失值随训练轮次的变化曲线,体现模型快速收敛与高性能特性。(c) 验证集与未训练芯片测试集的归一化混淆矩阵。
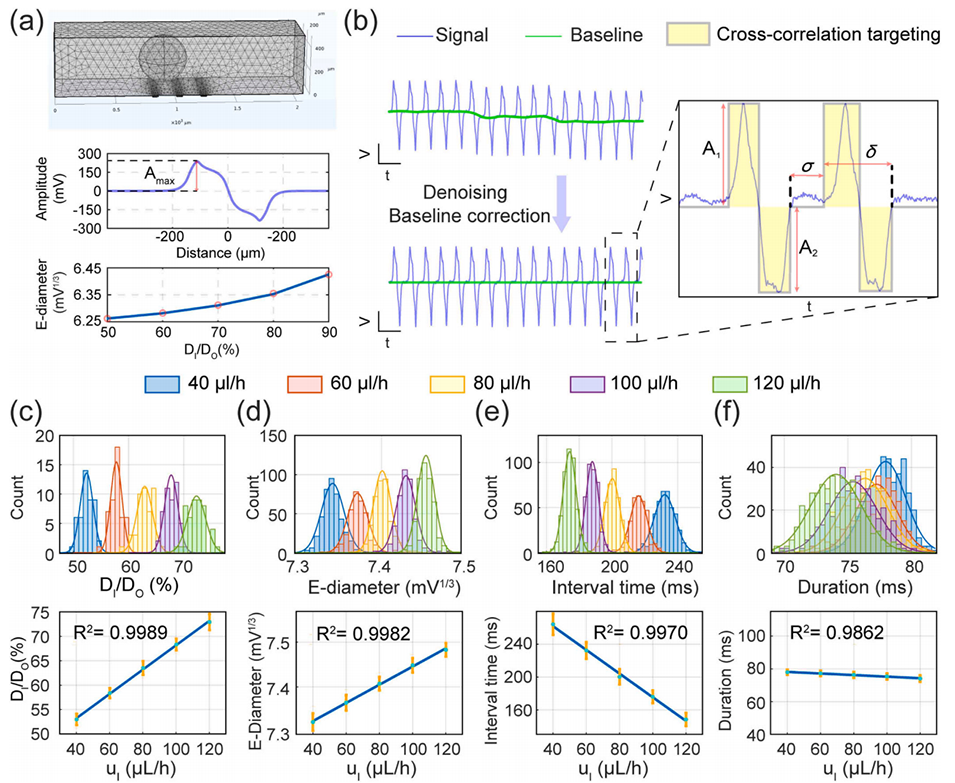
图4 基于阻抗的核壳直径表征。(a) 有限元分析(FEA)网格与仿真结果:单个微胶囊的仿真阻抗波形,以及不同内径/外径比微胶囊对应的电直径变化。(b) 阻抗信号处理流程:原始信号以 3 秒为时长采集;从单个微胶囊信号中提取四项特征:正幅值(A1)、负幅值(A2)、脉冲持续时间(δ,单组阻抗脉冲的持续时长)、脉冲间隔时间(σ,两组阻抗脉冲的时间间隔)。(c-f) 微胶囊实际尺寸与阻抗特征的统计分析:上行展示内液流速为 40、60、80、100、120 μL/h 时,微胶囊实际核径、电直径、脉冲间隔时间、脉冲持续时间的直方图,所有数据均符合高斯分布;下行展示各特征随内液流速(uI)的线性拟合结果,标注拟合决定系数(R²);所有数据点以平均值 ± 标准差(SD)表示。
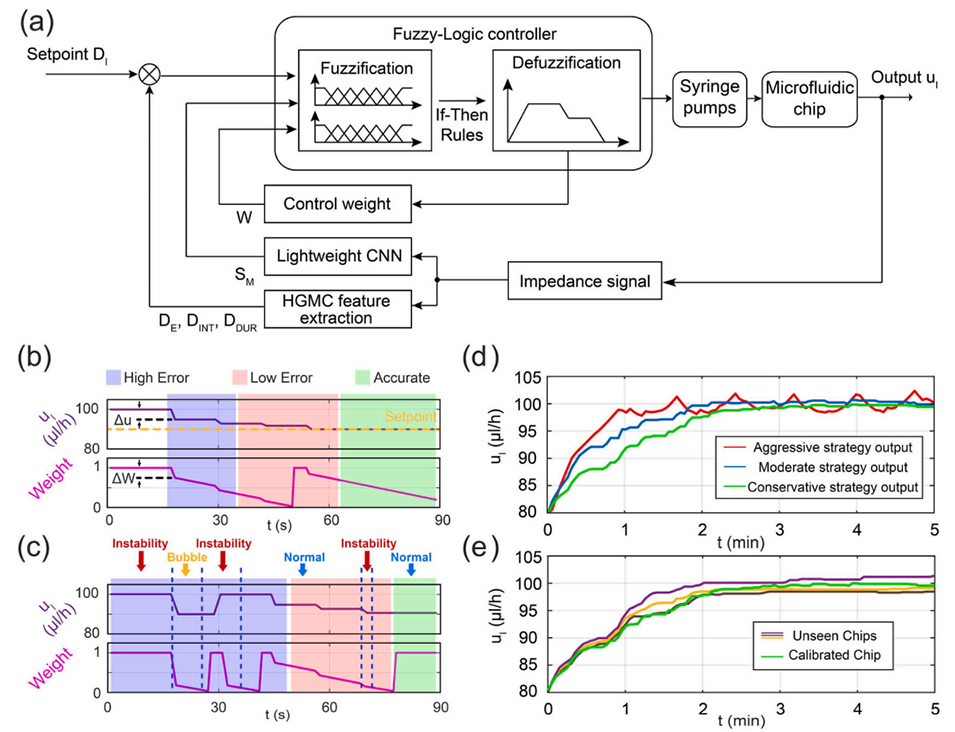
图5 所提模糊逻辑控制器(FLC)的原理与控制性能。(a) 以目标内径(DI)为设定值、内液流速(uI)为输出的 FLC 原理示意图。(b) 正常状态下内液流速(uI)与控制权重的变化,展示系统从 “高误差”“低误差” 向 “精准” 状态的过渡,标注单个控制周期内 uI 与控制权重的变化。(c) 微流控状态误分类时 uI 与控制权重的变化,证明系统可通过权重调节与可控的 uI 恢复,抵消误分类影响并重回稳定。(d) 激进型、中庸型、保守型控制策略的性能对比。(e) 未训练芯片与校准芯片的控制性能对比。
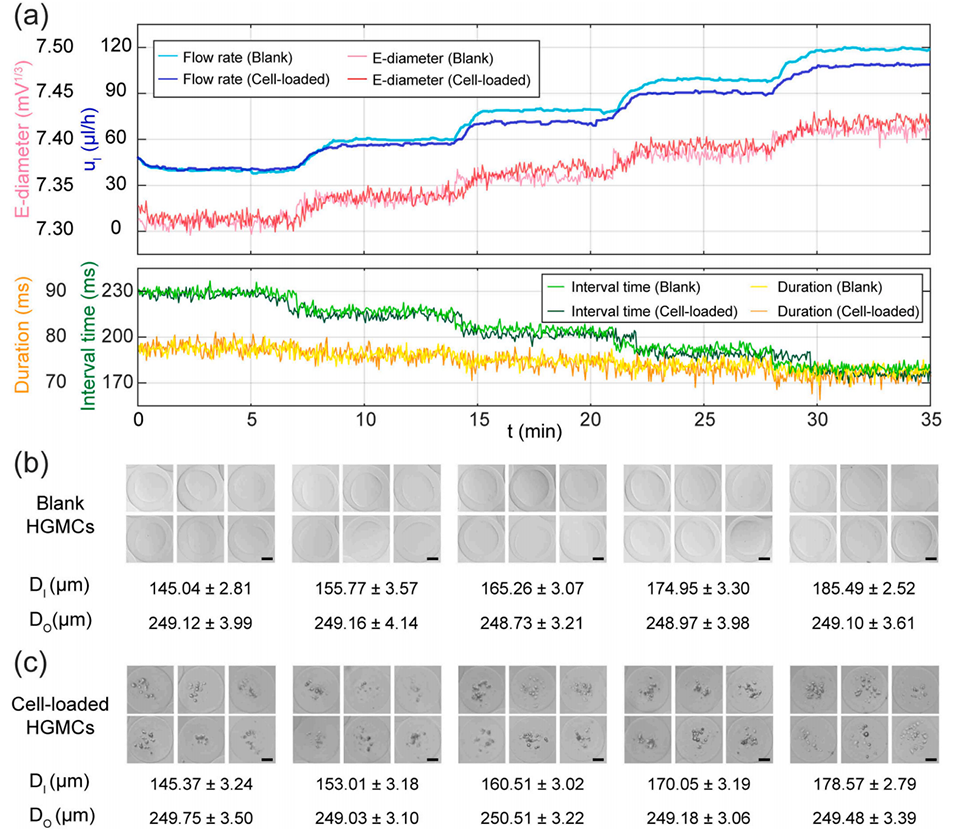
图6 空白微胶囊与载细胞微胶囊的控制曲线、阻抗特征及形貌。(a) 制备过程中空白与载细胞微胶囊的内液流速(uI)、电直径、脉冲间隔时间、脉冲持续时间的时序测量结果;控制过程采用五组阶梯式设定值,35 分钟内控制器依次驱动系统制备目标核径为 145 μm、155 μm、165 μm、175 μm、185 μm 的微胶囊。(b) 不同设定值下空白水凝胶微胶囊(HGMCs)的代表性明场图像;DI 与 DO 分别代表微胶囊的内径与外径,结果为 50 枚微胶囊明场图像的统计测量值;所有比例尺均代表 50 μm。(c) 不同设定下载细胞水凝胶微胶囊的代表性明场图像;所有比例尺均代表 50 μm。
论文链接:https://doi.org/10.1016/j.snb.2026.139964
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:一图读懂综述:液滴微流控技术在药物研发中的应用及进展
下一篇:暂无














