水凝胶颗粒作为可调控的微尺度平台,集精确结构与多样化化学、生物及物理功能于一身,正引起日益广泛的关注。在众多制备策略中,液滴微流控技术凭借对微尺度流体动力学的精确调控,已成为一种强大的技术,能够生产出尺寸、组成及内部结构均可控的单分散水凝胶颗粒。

近日,厦门大学物理科学与技术学院侯旭教授发表综述,系统阐述了液滴微流控技术在水凝胶微粒定制化制备中的核心作用。文章详细介绍了微流控芯片的加工策略、经典的流道几何结构以及驱动液滴生成的流体动力学原理。进一步探讨了适用于该技术的天然与合成聚合物材料,并归纳了物理、化学及酶促等多种交联成胶策略。通过精确调控液滴的组成与空间分布,该技术能够构建出核壳结构、各向异性及非球形等复杂形貌的功能化微粒。最后,文章展示了这些高性能水凝胶微粒在细胞培养、生物打印、药物递送及临床诊疗等前沿领域的广泛应用价值与未来发展前景。相关研究成果以“Droplet microfluidics: Enabling the tailored fabrication of hydrogel particles”为题,发表在期刊《Droplet》上。
本文要点:
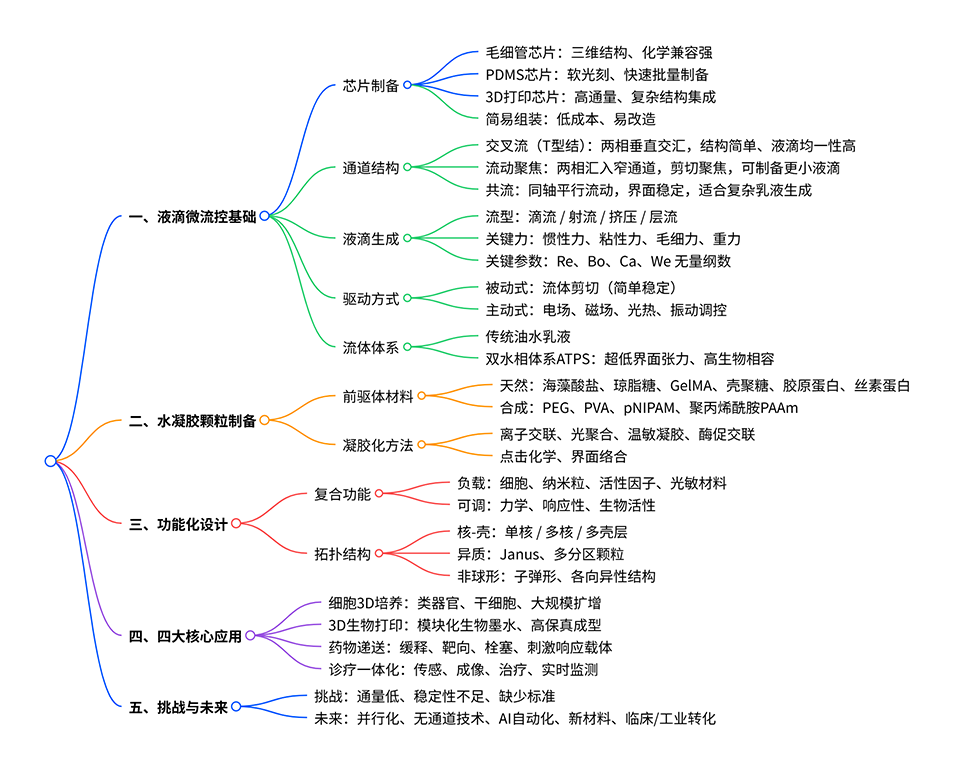
1、本综述首先概述了液滴微流控的基本原理,包括芯片制造、通道设计、液滴生成动力学、能量输入模式以及流体组成,这些要素共同支撑了可靠的颗粒制备。
2、随后重点介绍适配的水凝胶前驱体体系、凝胶化方式与功能化策略,以实现水凝胶颗粒的定制化构筑。
3、文章进一步展示了这类颗粒的广泛适用性,及其在细胞培养、3D生物打印、药物递送与诊断检测等领域的典型应用。
4、最后,本文对未来的发展方向进行了展望,包括系统并行化、过程自动化以及人工智能集成,这些举措有望提升液滴微流控水凝胶平台的可扩展性、功能性和多学科影响力。
一张图读懂全文
未来如何寻求突破
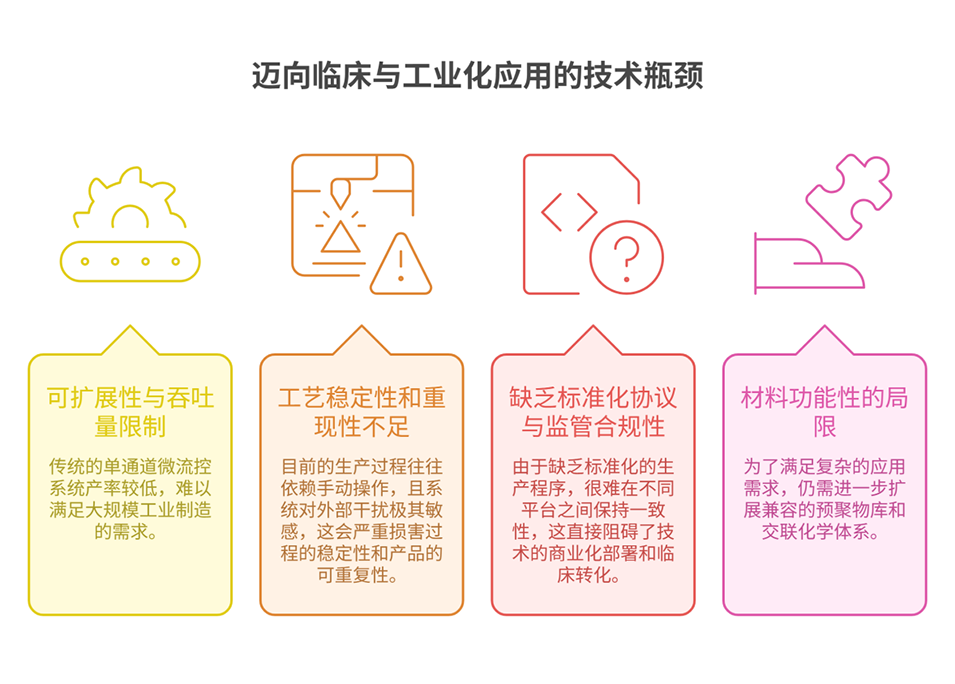
实现高吞吐量生产的硬件革新:
① 芯片并行化:通过开发并行化芯片阵列并集成高吞吐量策略,实现连续化、规模化生产。
② 离道生成技术(In-air/Channel-free):采用新兴的空气中液滴生成策略,通过诱导空气-液体界面的不稳定性来产生液滴。这种方法摆脱了微通道的空间限制,对高粘度体系具有更高的耐受性,且能通过简单的喷嘴并行化轻松实现规模化扩产。
引入人工智能与自动化控制:
① AI 实时监控:引入人工智能(AI)和机器学习(如卷积神经网络),对液滴生成过程进行实时监测和自动化调节。
② 闭环自动化:利用智能系统增强生产的一致性,减少人工劳动力,并对生产波动做出快速响应,从而提升颗粒制造的精准度和鲁棒性。
材料库的扩展与创新:
① 开发智能材料:引入更多功能性聚合物材料,如智能响应材料或导电材料,使颗粒在保持生物相容性的同时具备额外的环境响应能力或生物活性。
标准化与多学科协作:
① 建立行业标准:必须建立标准化的协议并遵循监管框架,以确保临床转化所需的重现性。
② 跨学科合作:通过微流控、材料科学、自动化工程和转化研究之间的多学科深度协作,共同推动下一代水凝胶颗粒制造技术的发展。
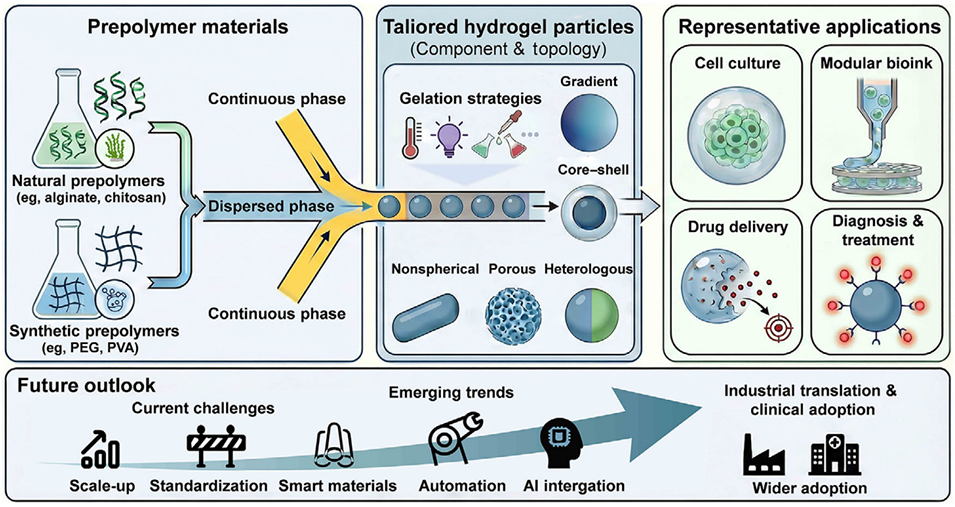
图1:液滴微流控作为工程化水凝胶颗粒多功能平台的概述。在微流控通道内,天然聚合物、合成聚合物或其混合物被乳化成单分散液滴,作为软模板。随后的化学或物理交联产生具有精确可调化学成分和拓扑形貌的水凝胶颗粒。这种可控的制备策略支持了从细胞培养、生物墨水开发到药物递送、诊断和治疗系统等广泛应用。
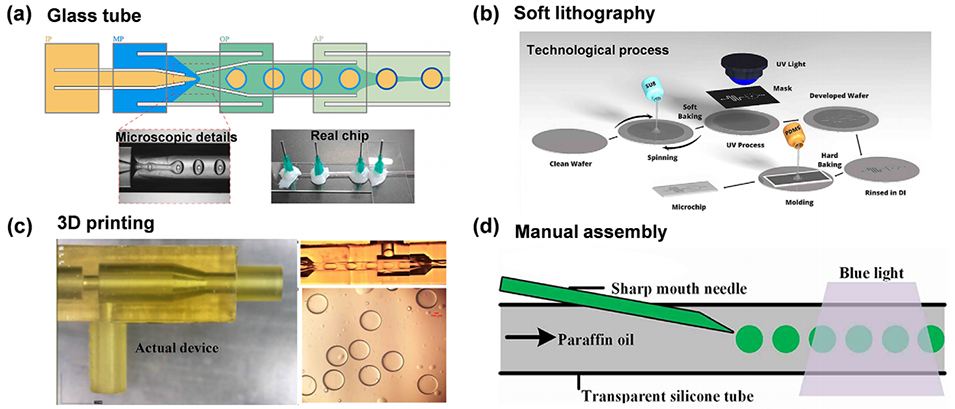
图2:制备液滴微流控芯片的常用策略。(a) 玻璃毛细管微流控装置的光学图像及双乳液生成过程。(b) 用于制造基于 PDMS 的液滴微流控芯片的软光刻技术。(c) 用于生成单乳液的 3D 打印微流控芯片。(d) 通过将商用针头插入硅胶管构建的手工组装液滴微流控装置示意图。
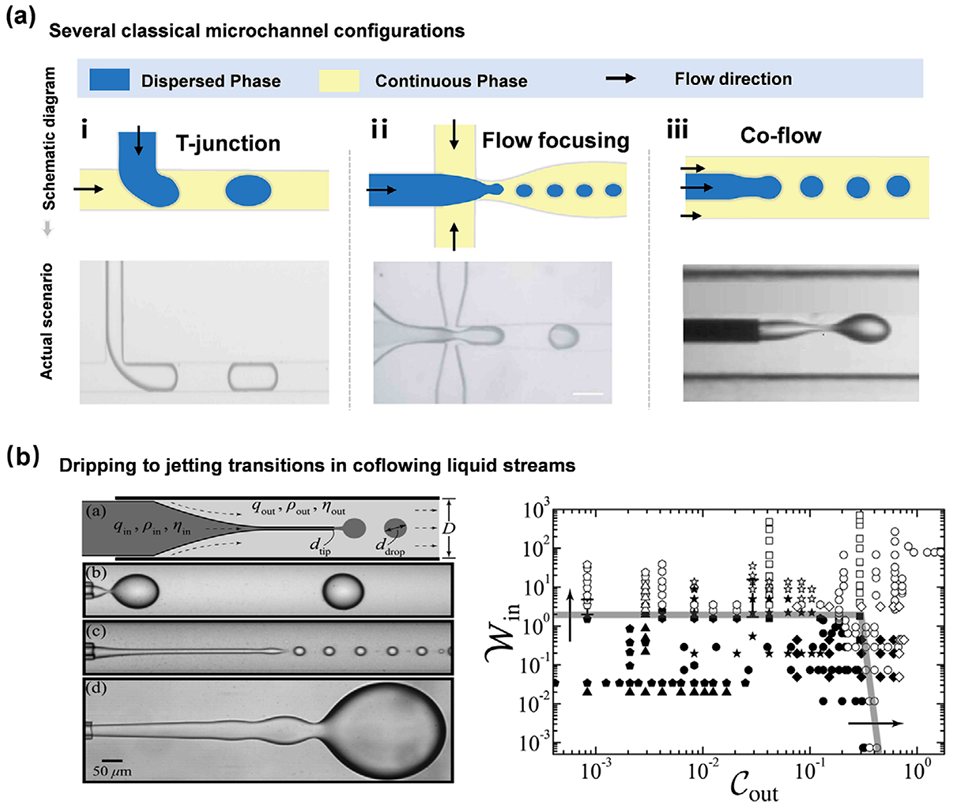
图3:液滴生成的流体动力学。(a) 液滴微流控中使用的经典微通道几何结构示意图:(i) 交叉流(Crossflow);(ii) 流动聚焦(Flow-focusing);(iii) 共流(Coflow)。每种设计都提供独特的流动特性和界面控制,从而实现对液滴尺寸、均匀性和生成速率的精确调节。(b) 锥形毛细管微流控装置内从滴落向喷射转变(dripping-to-jetting transition)的光学观察和边界分析。
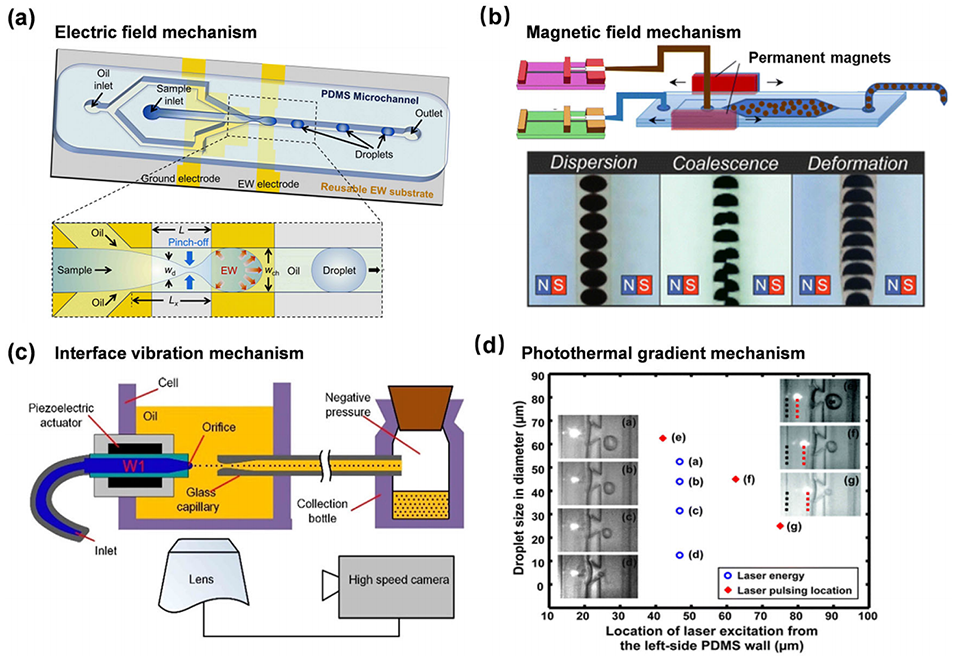
图4:微流控系统中控制液滴生成的常用主动机制。(a) 微通道中基于电润湿的主动液滴生成,通过外加电场调节润湿性,将分散流离散成液滴。(b) 横向磁场下流动聚焦微流控装置中磁流体液滴的磁场辅助生成,可实现可调的液滴尺寸/形状并抑制合并。(c) 由喷墨喷嘴驱动的受限界面振动,通过液体回撤实现比孔口更小的飞升量级液滴的主动微流控生成。(d) 光热激光驱动液滴生成(PLDG)微流控装置示意图,其中强聚焦激光脉冲产生瞬态空化气泡,驱动水通过类喷嘴开口进入油通道以形成液滴。
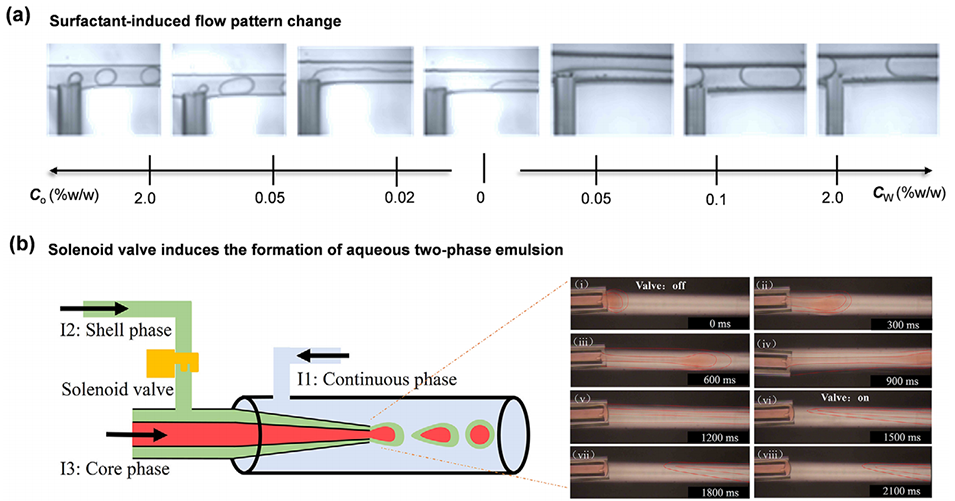
图5:液滴微流控中的经典流体组成。(a) 在不同的表面活性剂分布和浓度下,在单个微流控装置中可控生成水包油(O/W)和油包水(W/O)乳液。(b) 用于生成核壳微胶囊的全水相微流控系统,其中通过电磁阀对流体界面施加周期性扰动以促进均匀的液滴生成。
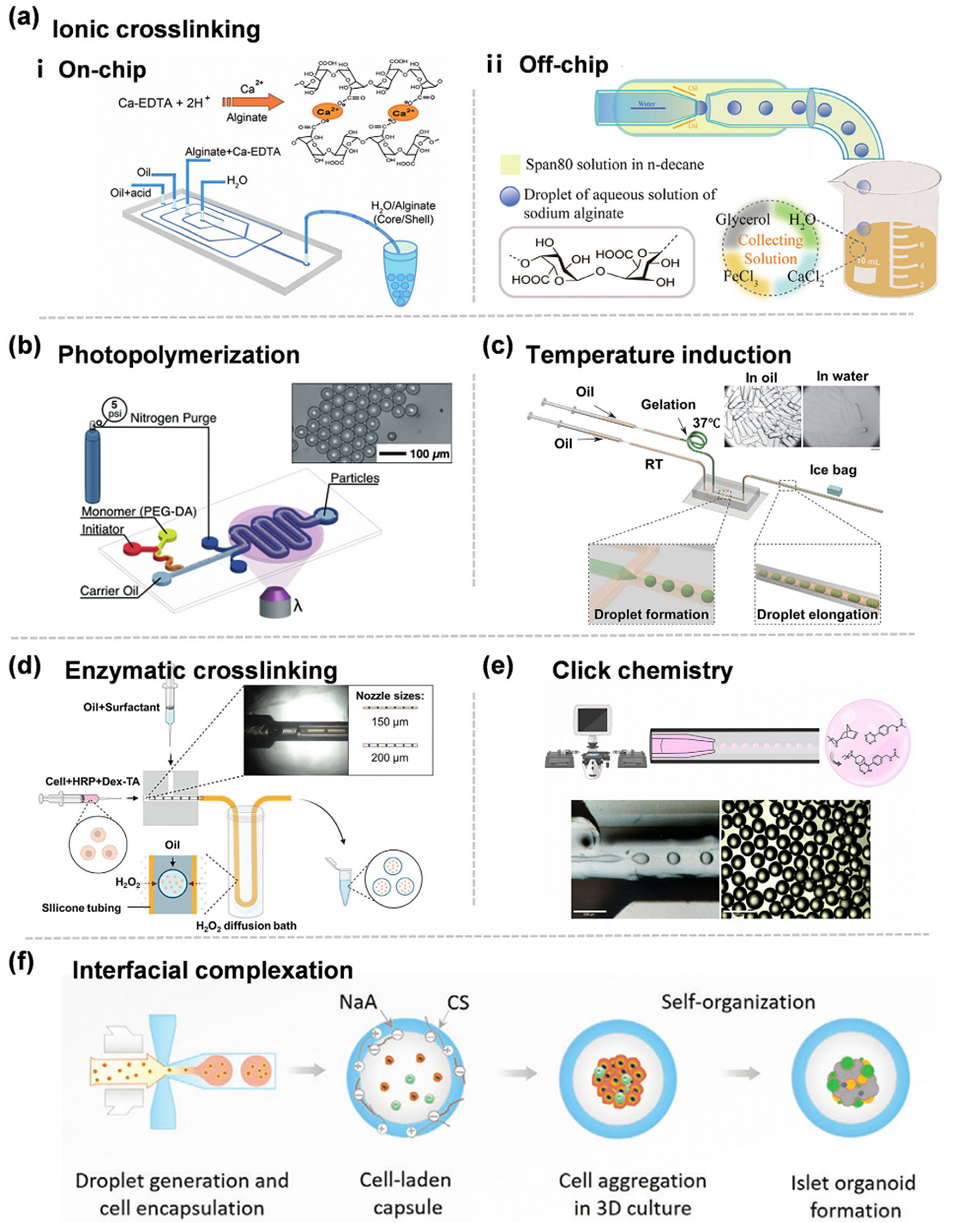
图6:适用于液滴微流控的多种交联策略。(a) 水凝胶颗粒的液滴模板离子交联:(i) 通过液滴网络内 Ca–EDTA 复合物受控释放 Ca2+ 诱导的片上交联;(ii) 通过将液滴浸入 Ca2+ 和 Fe3+ 溶液实现的片外交联。(b) 通过紫外诱导光聚合制备 PEGDA 水凝胶颗粒的氧控策略。(c) 通过低温诱导的明胶液滴固化。(d) 通过 HRP 介导的酶交联在微流控装置中形成的空心水凝胶颗粒,H2O2 通过半透管扩散引发由外而内的凝胶化。(e) 通过四嗪-降冰片烯逆电子需求 Diels–Alder(IEDDA)点击化学微流控制备水凝胶微球。(f) 聚电解质介导的交联策略,用于制备水凝胶微胶囊,为胰岛类器官培养提供支持性微环境。
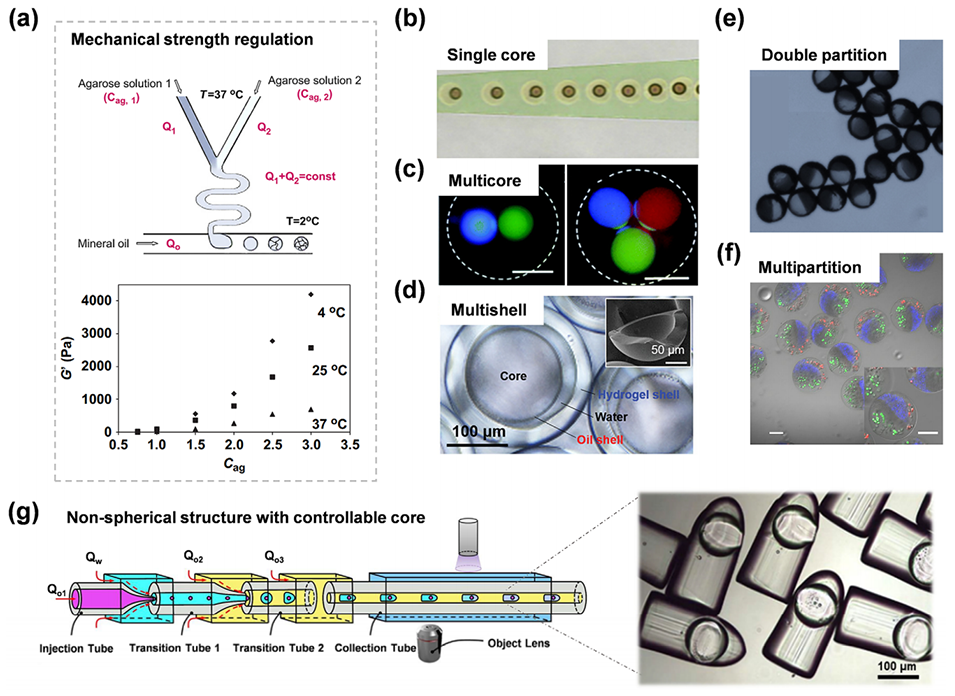
图7:各种类型的功能化水凝胶颗粒。(a) 通过在微流控装置中结合不同浓度的琼脂糖前驱体液滴,随后进行热凝胶化而生成的具有可调机械性能的琼脂糖水凝胶颗粒。(b) 单核水凝胶颗粒。(c) 多核水凝胶颗粒。(d) 多壳水凝胶颗粒。(e) 双面分区(Janus)水凝胶颗粒。(f) 多面异质水凝胶颗粒。(g) 通过将液滴模板形变与受限通道中的流体动力学流场耦合,构建具有高阶功能的非球形水凝胶颗粒。
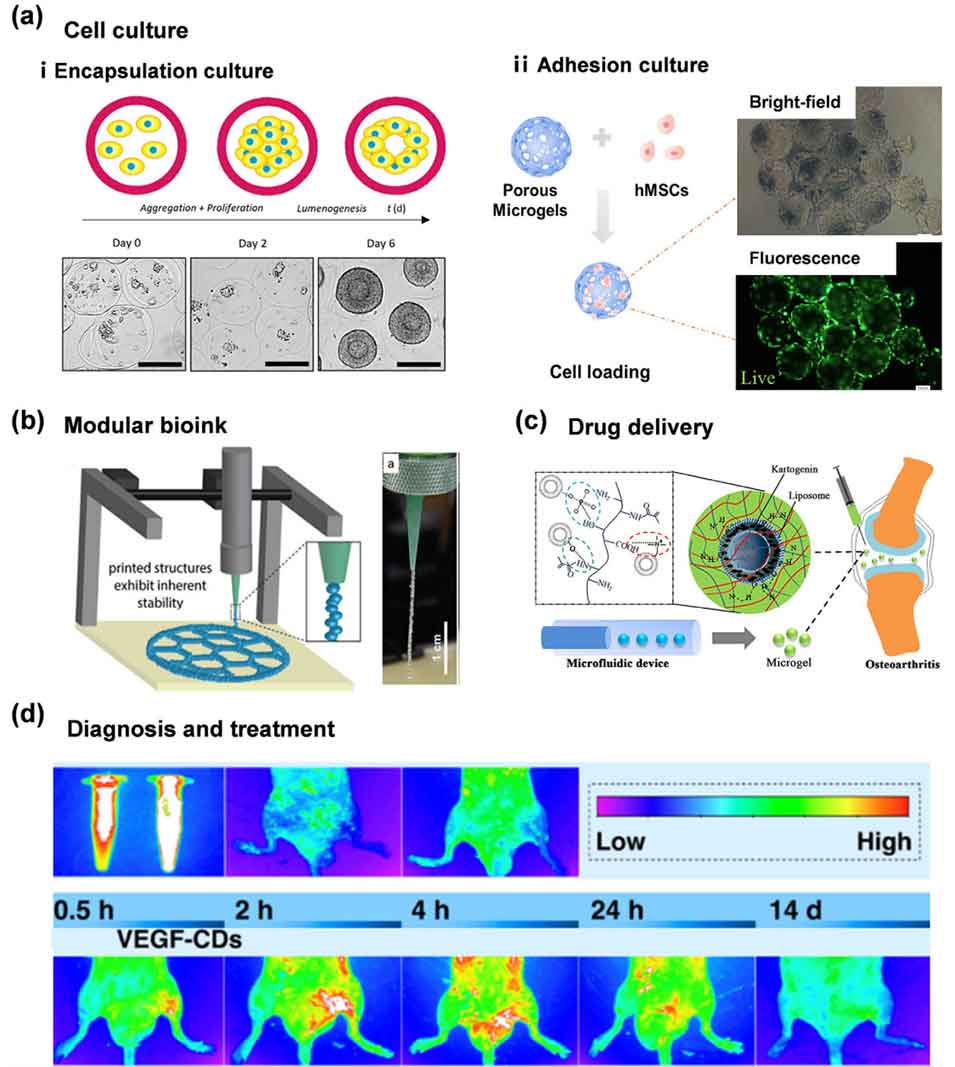
图8:水凝胶颗粒在细胞培养、生物墨水开发、药物递送及诊断与治疗中的应用。(a) 用于细胞培养的水凝胶颗粒示意图,突出了两种代表性策略:(i) 封装培养;(ii) 表面粘附培养。(b) 水凝胶颗粒作为 3D 生物打印的构建基块。(c) 作为脂质体递送药物载体以缓解骨关节炎的水凝胶颗粒。(d) 负载 VEGF 的水凝胶颗粒可同时实现治疗性血管生成和基于荧光的血管化监测。
论文链接:https://doi.org/10.1002/dro2.70068
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:70天平稳释放!微流控精准调控核壳微球壳厚,显著降低多肽药物初始突释
下一篇:暂无














