
导读:
近期,有研究人员开发了一种新型混合微流控平台,该平台通过结合等离子体活化涂层(PAC)和大气压等离子体射流(APPJ)技术,实现了生物分子的无试剂共价固定化,显著提高了内皮细胞在芯片上的附着和增殖,有望在器官芯片开发、临床诊断、药物发现等领域带来突破性进展。相关研究以“Reagent-Free Covalent Immobilization of Biomolecules in a Microfluidic Organ-On-A-Chip”为题目,发表在期刊《Advanced Functional Materials》上。
本文要点:
1、本研究开发了一种融合等离子体活化涂层(PAC)与大气压等离子体射流(APPJ)技术的新型表面处理方法,成功在微流控芯片的PDMS及玻璃材料上实现了无需添加化学试剂的生物分子共价固定化。
2、PAC和APPJ处理可以在PDMS和玻璃表面引入含氧基团和自由基,从而实现对纤连蛋白的共价固定化,优于传统的氧等离子体处理。
3、PAC处理可以更好地支持人冠状动脉内皮细胞(HCAEC)在PDMS上的粘附和增殖,而APPJ处理则更有利于HCAEC在玻璃基底上的生长。
4、将PAC处理的PDMS和APPJ处理的玻璃结合制备的混合微流控芯片,在低切应力和冠状动脉切应力条件下均表现出优异的内皮化和细胞功能。
5、该混合微流控芯片具有与传统氧等离子体处理芯片相当的结合强度,无需额外的烘烤步骤,为器官芯片和芯片实验室等应用提供了一种简单、高效且可靠的生物功能化方法。
相比传统的氧等离子体处理,等离子体活化涂层(PAC)和大气压等离子体射流(APPJ)处理的优势主要体现在以下几个方面:
1、生物分子的共价固定:
氧等离子体处理只能实现蛋白质的物理吸附,在流动或洗涤过程中很容易脱落。
PAC和APPJ处理引入的官能团和自由基能够与蛋白质发生共价键合,提供更强、更稳定的固定。
2、改善细胞粘附和增殖:
在PDMS上,与氧等离子体处理相比,PAC处理显著增强了内皮细胞的增殖。
在玻璃上,与氧等离子体处理相比,PAC和APPJ处理都促进了更好的内皮细胞粘附和增殖。
3、老化/疏水恢复更慢:
氧等离子体处理的表面在4天内就恢复了原有的疏水性,而PAC和APPJ处理的表面可以保持亲水性1-2周以上。
PAC和APPJ处理表面老化更慢,可以实现更长期的存储和使用。
4、微流控器件的结合强度等同或更好:
氧等离子体处理的器件需要额外的烘烤步骤才能达到足够的结合强度。
APPJ处理的器件无需烘烤即可达到与氧等离子体相当的结合强度。
总之,与传统的氧等离子体处理相比,PAC和APPJ技术提供了更优异的生物分子共价固定能力、增强了细胞与材料的相互作用,并带来了更稳定的表面特性,从而在微流控芯片和器官芯片应用中展现出更大的优势。
本研究提出的基于等离子体的新型表面处理技术在提高诊断工具的准确性方面具有以下优势:
1、共价固定生物分子:通过共价键合,生物分子(如酶和抗体)能够稳定地固定在微流控芯片的表面上,减少了在流体作用下或洗涤步骤中的脱附风险,从而提高了检测的可靠性。
2、改善生物分子的取向和活性:共价固定可以控制生物分子的取向,确保它们以最活跃的形式呈现,这有助于提高与目标分子的结合效率,从而提高检测的灵敏度和特异性。
3、无需额外试剂:与需要使用有毒和昂贵试剂的湿化学方法相比,这种技术无需额外试剂,减少了操作复杂性和成本,同时降低了由于试剂引入的潜在干扰。
4、优化的微环境:等离子体处理可以改善微流控芯片的表面特性,为生物分子提供一个更接近生理条件的微环境,有助于维持它们的生物活性和稳定性。
5、减少非特异性结合:通过精确控制生物分子的固定位置和密度,可以减少非特异性结合,从而降低背景噪声,提高信号与噪声比。
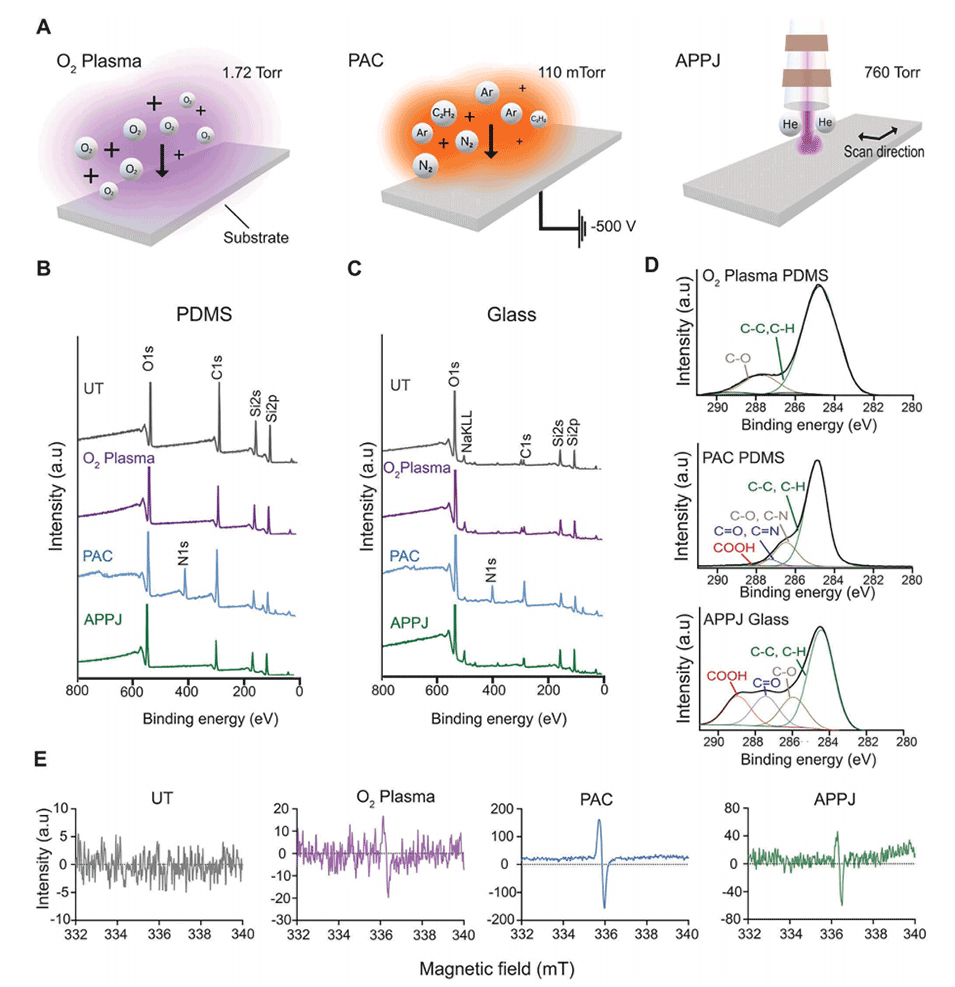
图1.PAC和APPJ诱导官能团和自由基的形成。
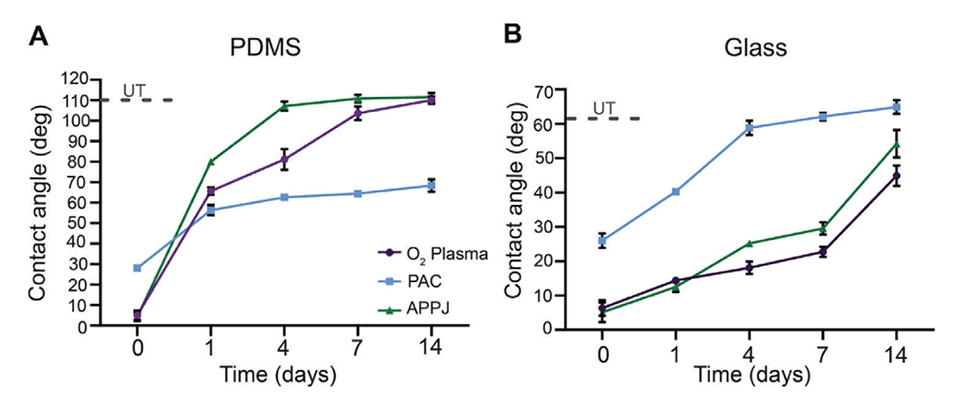
图2.经PAC处理的PDMS上的润湿性恢复较慢。
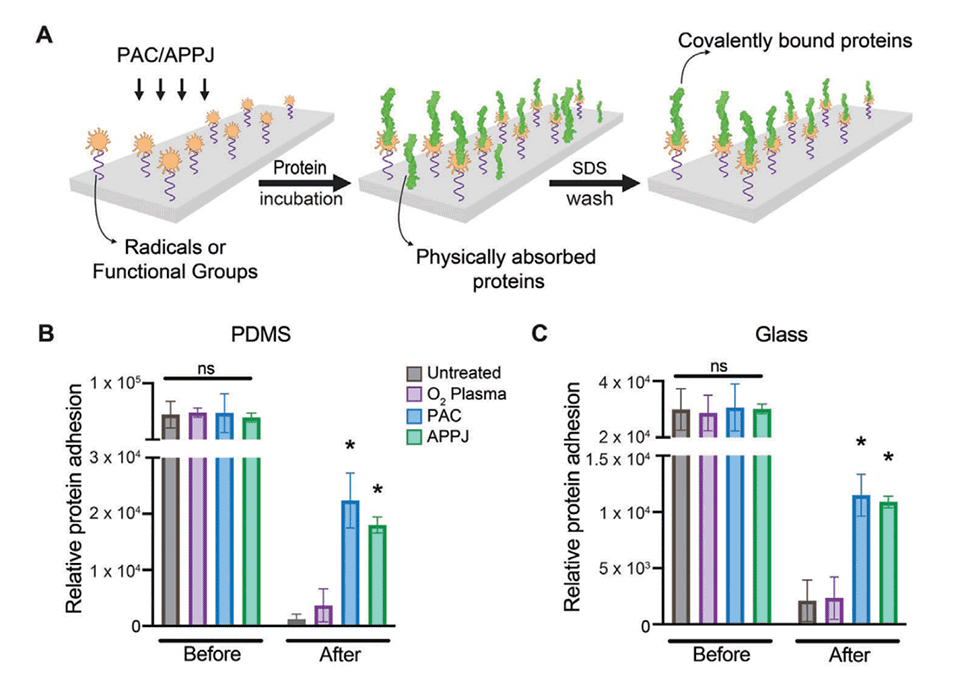
图3.PAC和APPJ可使纤维连接蛋白共价固定在PDMS和玻璃上。
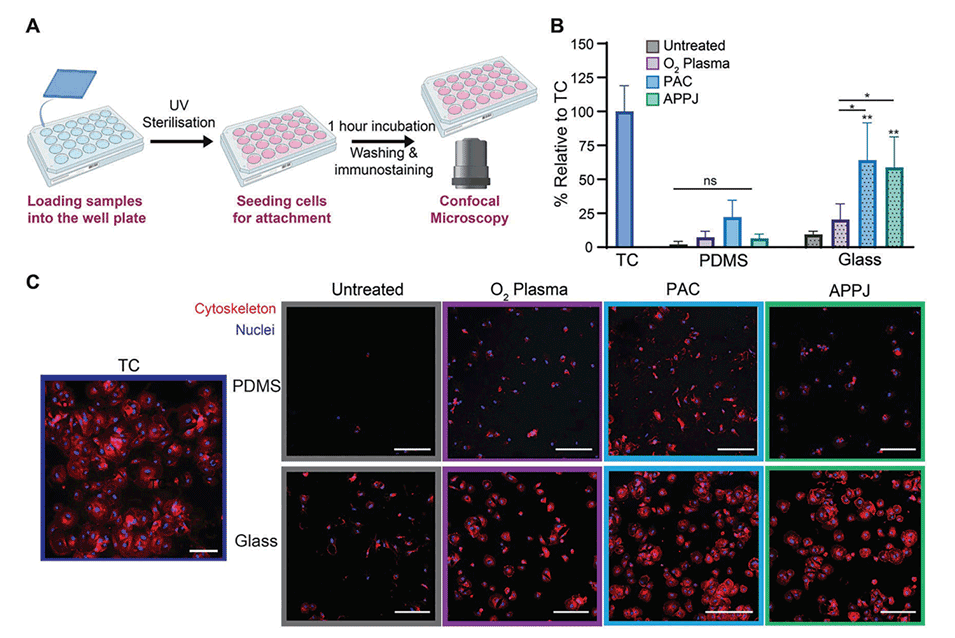
图4.PAC和APPJ处理可促进HCAEC在玻璃表面的附着。
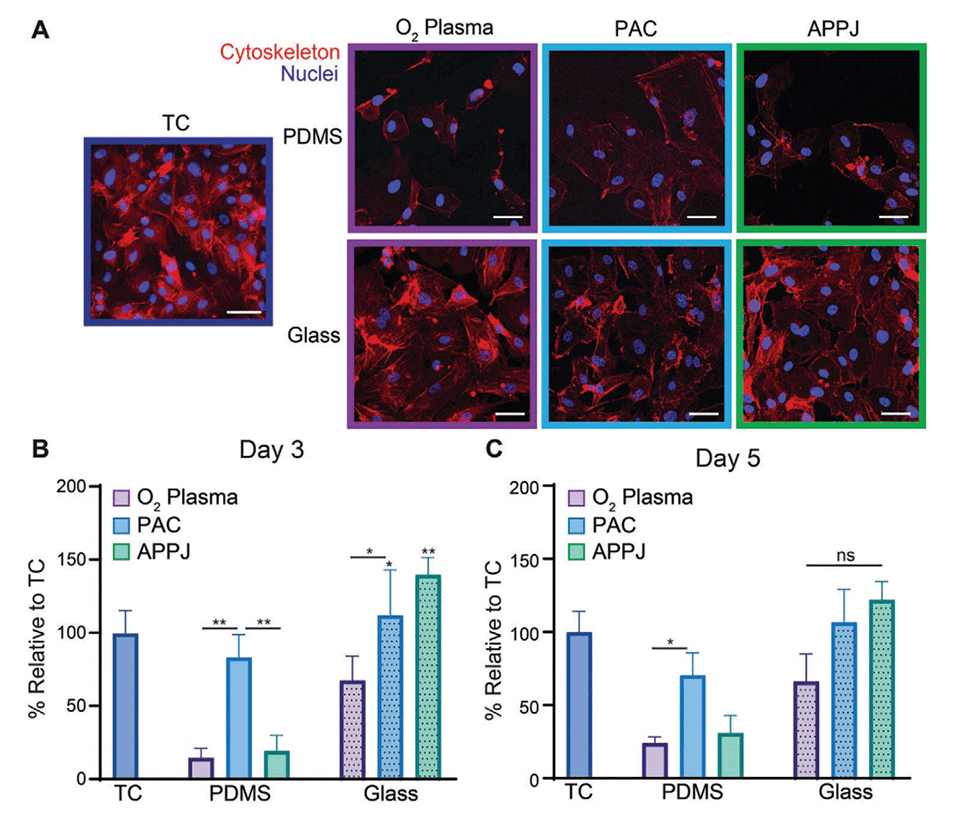
图5.PAC可促进HCAEC在PDMS和玻璃基底上增殖,APPJ可促进HCAEC在玻璃上增殖。
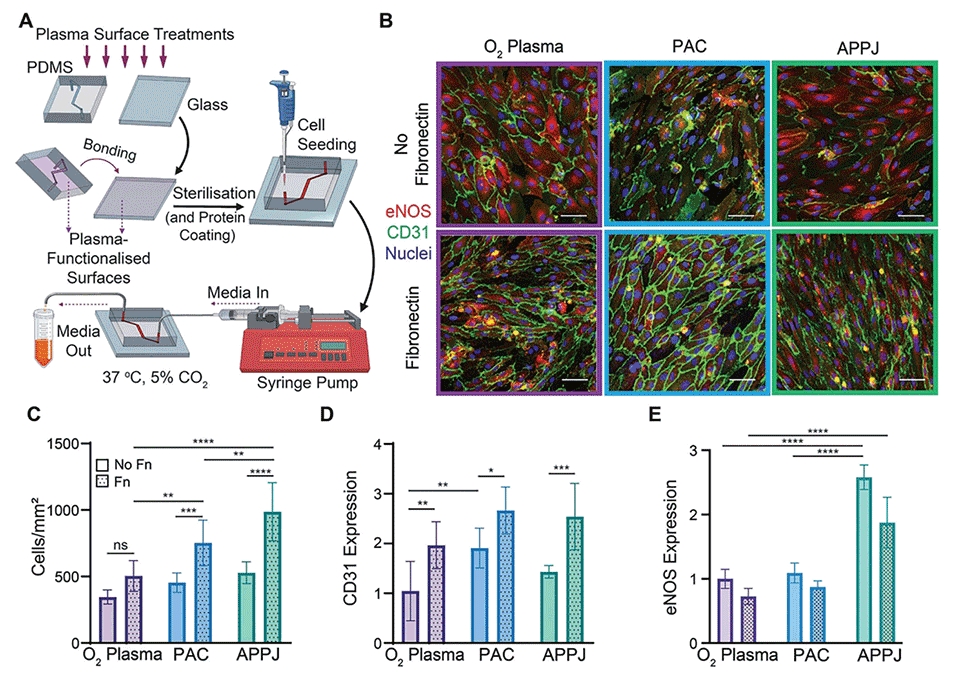
图6.PAC和APPJ处理可促进动脉芯片中HCAEC的生长和功能。
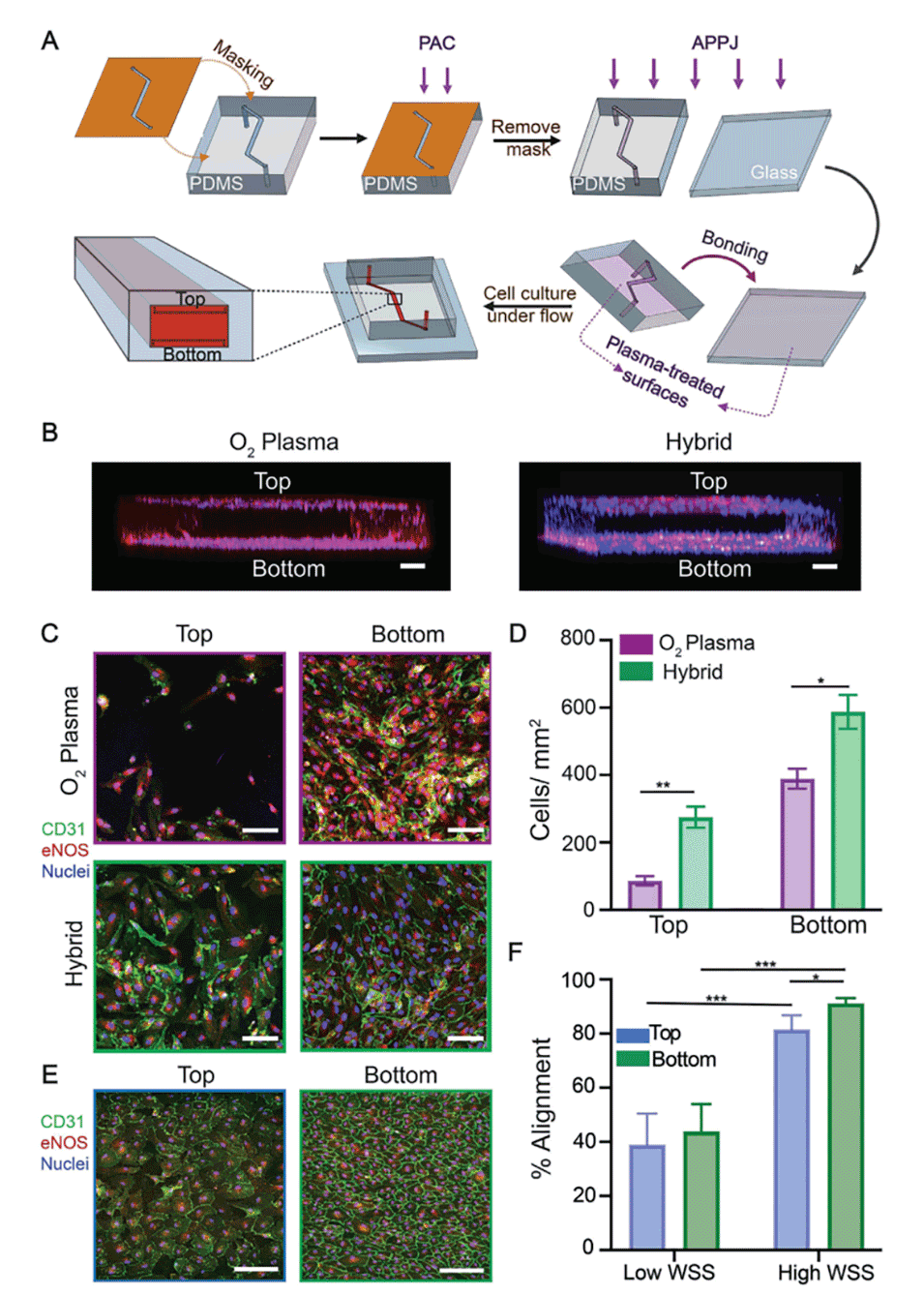
图7.混合装置可促进动脉芯片中健康内皮的形成。
原文链接:
https://doi.org/10.1002/adfm.202313664














