同时检测单个细胞外囊泡(EVs)中的蛋白质和mRNA,可以全面分析特定EVs亚群,显著推进癌症诊断。然而,开发一种灵敏且易操作的方法来同时检测单个EVs中的多维生物标志物仍然具有挑战性。

为了促进EVs多维生物标志物的分析并提高其临床适用性,近期,南方医科大学南方医院郑磊&上海科技大学刘一凡等人提出了一种基于微流控技术的数字化分析系统,用于在单个EVs水平上同时检测膜蛋白和mRNA,以提高癌症诊断的准确性。相关研究以“Simultaneous detection of membrane protein and mRNA at single extracellular vesicle level by droplet microfluidics for cancer diagnosis”为题目,发表在期刊《Journal of Advanced Research》上。
本文要点:
1、开发了一种基于微流控技术的新型数字检测系统,可以同时检测单个细胞外囊泡(EVs)中的膜蛋白和mRNA。
2、该系统结合了微流控技术的单分子灵敏度和抗体-DNA缀合物的高特异性,可以准确识别和分析特定的EVs亚群。
3、在乳腺癌患者队列中验证了该系统的临床应用潜力。通过联合检测CD9/CD63/CD81、ERBB2 mRNA和HER2蛋白,可以更好地区分乳腺癌患者和健康个体以及良性对照,尤其是对早期乳腺癌的诊断效果更优。
4、该系统可以提供更全面的肿瘤信息,包括基因转录和蛋白翻译功能,从多维度角度提高肿瘤诊断的准确性,为未来临床应用提供了有希望的策略,并且可扩展至其他疾病的研究中。
液滴微流控技术在检测EVs方面具有多项优势,具体如下:
1、高灵敏度:液滴微流控技术能够在单个EVs水平上进行分析,极大地提高了对低丰度生物标志物的检测灵敏度。
2、抗干扰能力强:通过将EVs封装在独立的微滴中,每个微滴最多只包含一个EVs,这种分离减少了信号干扰,确保了检测的准确性。
3、多重检测能力:该技术可以同时检测多个生物标志物(如膜蛋白和mRNA),提供更全面的肿瘤信息,有助于提高癌症诊断的准确性。
4、简化操作流程:与传统的分步分析方法相比,液滴微流控技术能够在一个步骤中完成对EVs的多维度分析,减少了时间和操作复杂性。
5、适应性强:该技术不仅适用于癌症诊断,还可以扩展到其他疾病的研究,具有广泛的应用潜力。
6、高特异性:通过抗体-DNA缀合物的使用,液滴微流控技术能够实现高特异性的抗原-抗体反应,提高了检测的可靠性。
7、临床应用前景:该技术在临床试验中表现出色,能够有效区分健康个体与癌症患者,尤其是在早期癌症的检测中显示出良好的性能。
该系统如何实现单个EVs蛋白质和mRNA的同时检测?
该系统利用抗体-DNA缀合物对EVs表面蛋白进行标记,将蛋白质信息转化为核酸信号。
通过微流控技术将标记的EVs和裂解缓冲液分散到独立的微滴中,每个微滴相当于一个单独的反应微载体。
在微滴内,EVs被裂解释放出其内部的mRNA,与抗体-DNA缀合物一起触发三重RT-ddPCR反应,实现了单个EVs蛋白质和mRNA的同时检测。
该系统在乳腺癌诊断中的应用优势如下:
该系统联合检测了CD9/CD63/CD81+EVs、ERBB2 mRNA+EVs和HER2+EVs,能够从多维度提供肿瘤相关信息,显著提高了对乳腺癌的诊断性能。
在区分良性和恶性病变方面,该系统的诊断效能(AUC为7119)优于传统的血清肿瘤标志物(CEA、CA125和CA153)(AUC为0.6184)。
对于早期乳腺癌(Tis-I期)的诊断,该系统的AUC值高达0.9229,敏感性85%,特异性29%,显著优于单一指标检测。
这种多维度联合检测的优势,为乳腺癌的早期诊断和鉴别诊断提供了重要的临床应用价值。
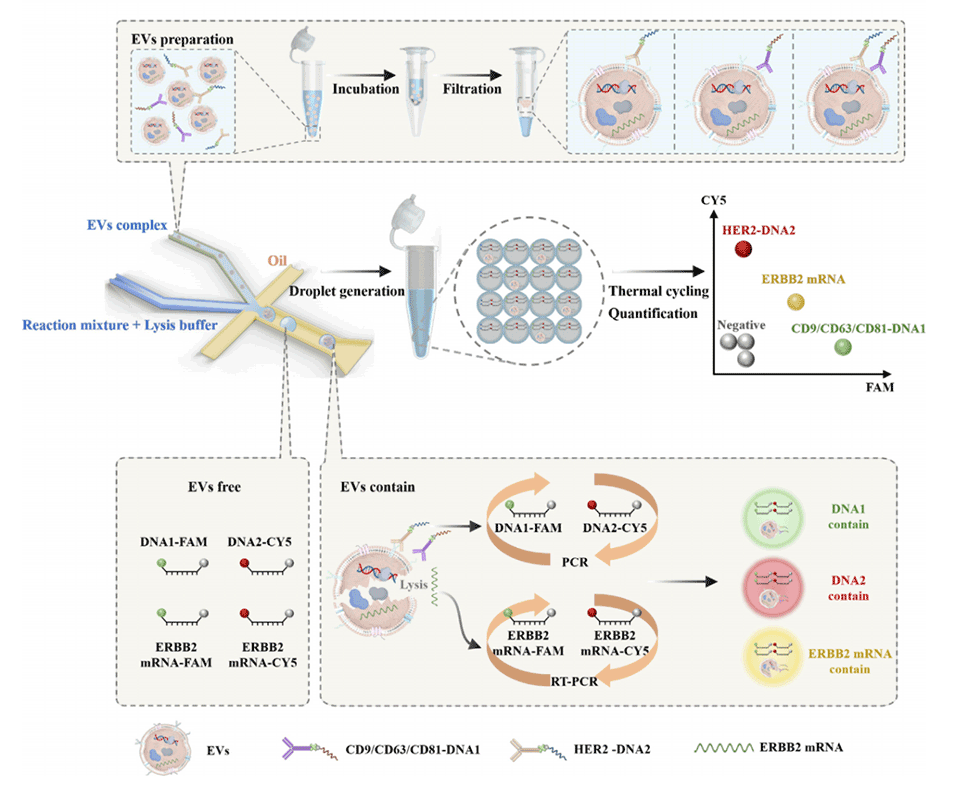
图1.在单个囊泡水平上对EVs衍生的表面蛋白和核酸进行联合数字检测的示意图。
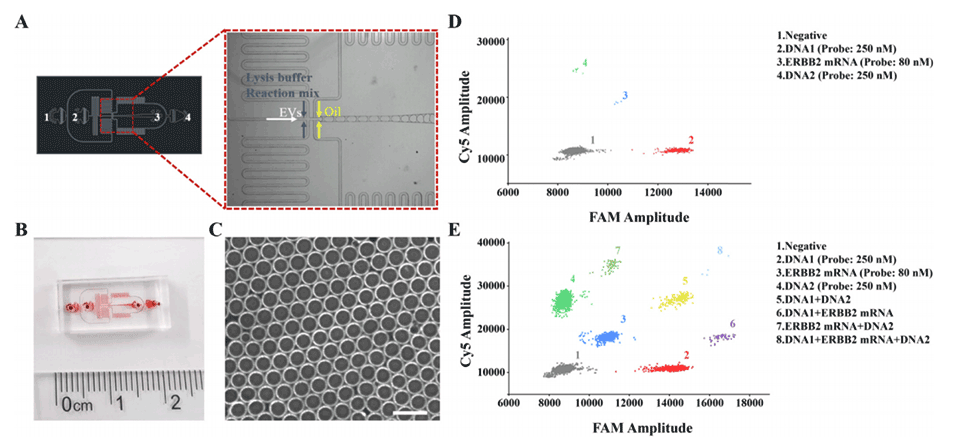
图2.针对DNA信号链和mRNA的三重液滴数字检测系统的开发。
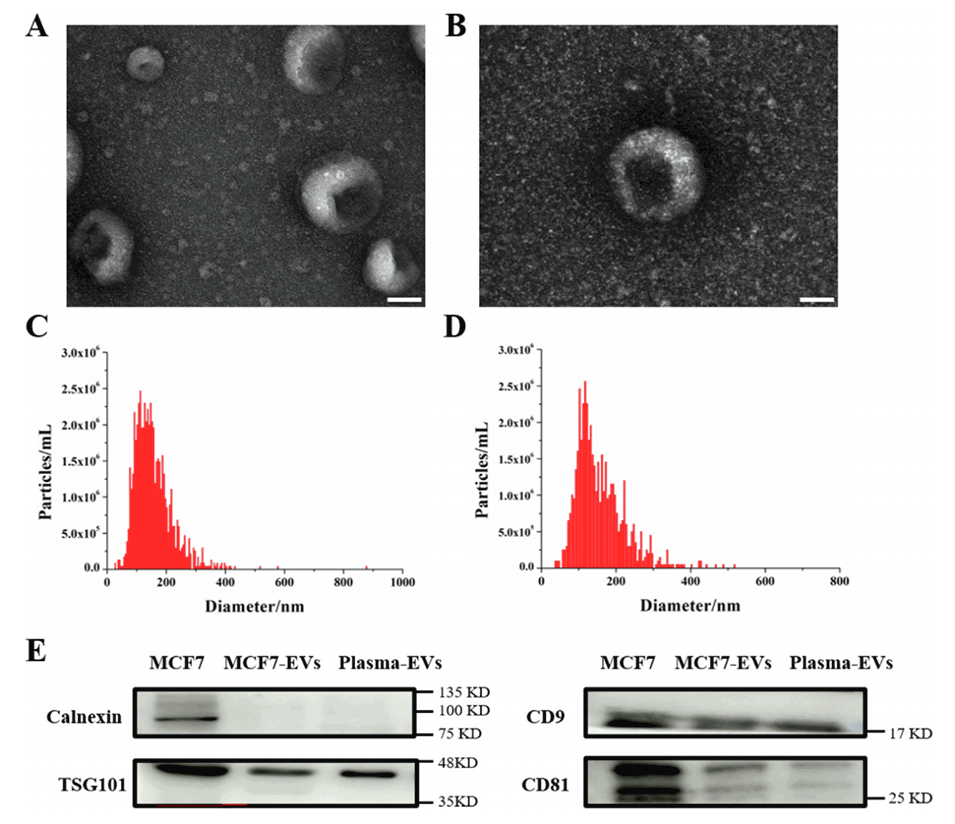
图3.EVs的表征。
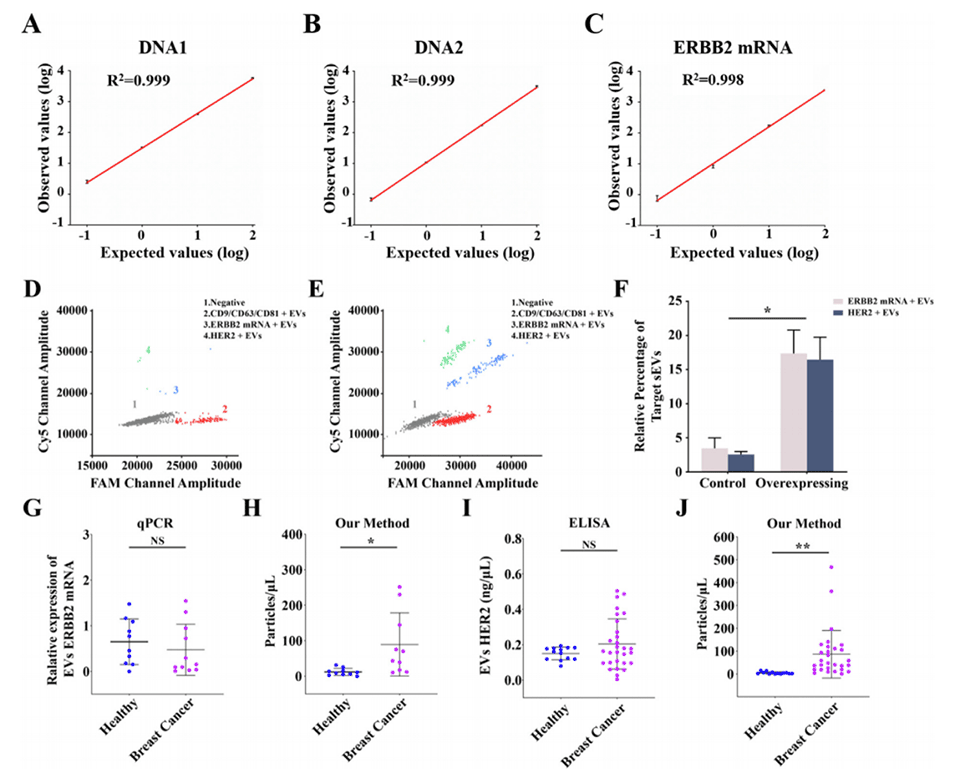
图4.液滴数字分析法在单个外囊泡水平上同时分析EVs中mRNA和蛋白质的检测性能。
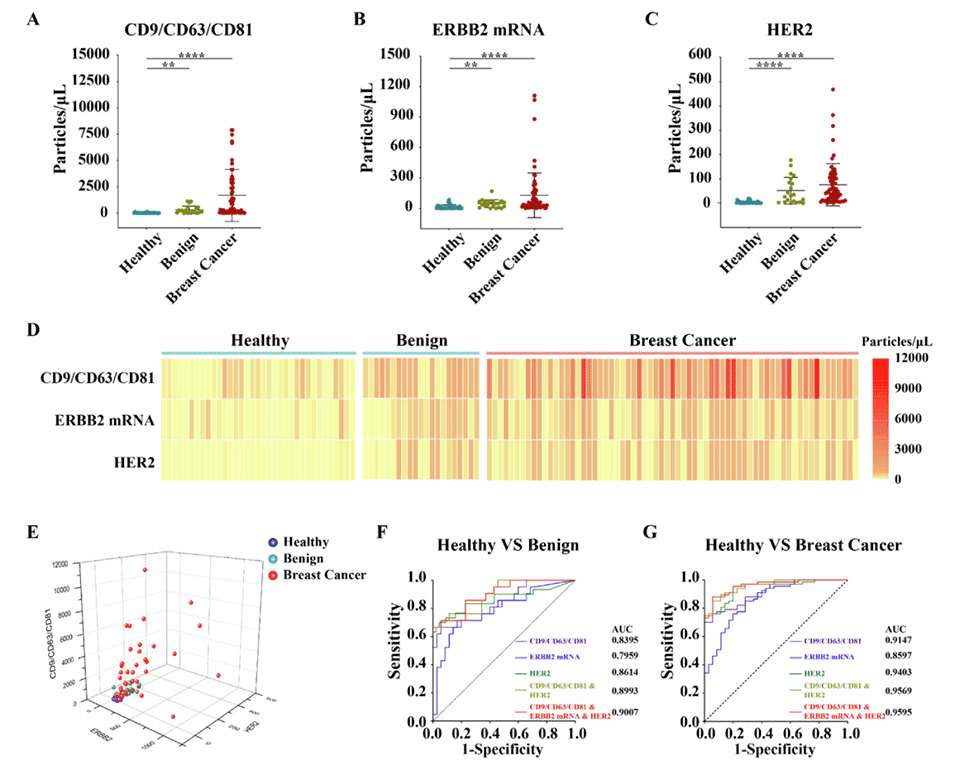
图5.联合数字检测系统在乳腺癌队列中的诊断性能评估。
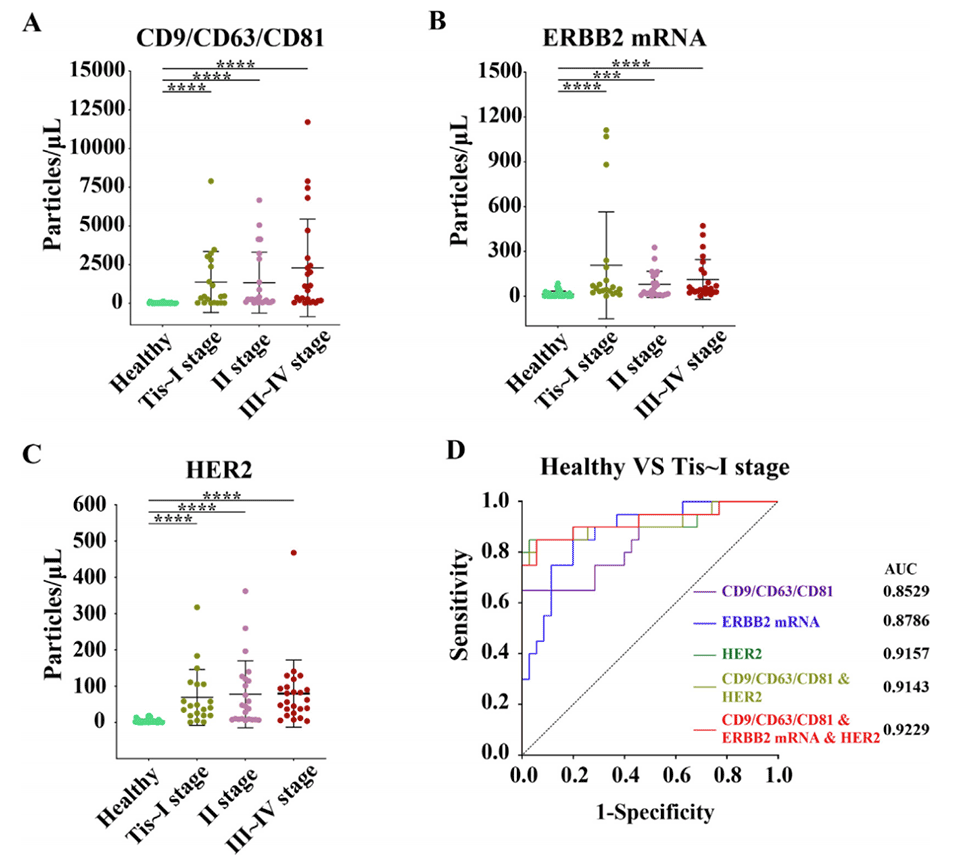
图6.联合数字检测系统在乳腺癌早期诊断中的诊断性能评估。
原文链接:https://doi.org/10.1016/j.jare.2024.08.026














