脂质体模拟细胞脂质膜的特殊能力使其成为生物膜研究和自下而上的合成生物学的宝贵工具。微流体技术为以可控方式制造巨型脂质体提供了一个很有前途的工具包。然而,与作为巨型脂质体前体的双乳液微流体形成相关的挑战,限制了对这一潜力的充分探索。

近期,有研究人员提出了一种无需表面处理的PDMS-玻璃毛细管混合微流控装置及集成分离芯片,用于高效制备和纯化双乳液模板,并通过溶剂萃取法生成巨型脂质体,为仿生膜研究和合成生物学提供了灵活可靠的工具。相关研究以“Facile and versatile PDMS-glass capillary double emulsion formation device coupled with rapid purification toward microfluidic giant liposome generation”为题目,发表在期刊《Microsystems & Nanoengineering》上。
本文要点:
1、本研究提出了一种基于PDMS-玻璃毛细管混合微流控装置的双乳液生成平台,用于高效制备巨型脂质体。
2、该装置无需选择性表面处理,简化了双乳液的生成过程,同时具备可重复使用、定制化和多功能性的特点。
3、该装置能够生成不同尺寸(直径跨越两个数量级)、壳厚和腔体数量的双乳液液滴,通过在双滴模式下操作混合芯片,实现了稳健的薄壳双乳液形成。
4、此外,还开发了一种串联分离芯片,利用流体动力学和密度差快速纯化双乳液样品,避免了传统离心分离的耗时步骤。
5、通过溶剂萃取法,成功将双乳液模板转化为巨型脂质体,展示了该平台在高通量制备巨型脂质体和合成细胞中的应用潜力,为仿生膜研究和底层合成生物学提供了新工具。
该PDMS-玻璃毛细管混合设备在双乳液的形成和纯化方面具有显著的改善,主要体现在以下几个方面:
1、无须表面处理:该设备结合了PDMS的疏水性和玻璃的亲水性,消除了传统PDMS芯片在形成双乳液时需要进行选择性表面处理的问题,从而简化了操作流程。
2、可重复使用性:设备的独特设计使其能够在多次使用后保持性能,降低了成本和资源浪费。
3、定制化设计:设备能够根据实验需求进行定制,例如不同的滴液形成几何形状和功能集成(如混合和分选),这在传统的玻璃毛细管设备中是难以实现的。
4、多功能性:该设备能够形成不同尺寸、壳厚度和腔体数量的双乳液,适用于多种溶剂,展示了其在微流控应用中的广泛适用性。
5、快速纯化方法:设备配备了一个串联的分离芯片,利用流体流动和密度差异,能够快速去除油滴污染,确保双乳液的纯度。这种在线分离方法提高了处理效率,减少了额外的离线处理步骤。
6、高通量生成:该设备能够以高达1140个双乳液每秒的速度生成双乳液,显著提高了生产效率。
通过这些改进,该设备为双乳液的形成和纯化提供了一种简单、灵活且可靠的方法,推动了巨型脂质体和合成细胞的高通量制备。
本研究展示了PDMS-玻璃毛细管混合设备在生成不同尺寸和类型的双乳液方面的多样性,主要采用了以下几种方法:
1、不同直径的毛细管:研究者使用了两种不同内径的玻璃毛细管(1mm和550μm)来生成不同尺寸的双乳液。通过调整毛细管的尺寸,成功形成了直径从1.2mm到27μm的双乳液。
2、毛细管的锥形设计:为了进一步增强尺寸调节能力,研究者对550μm内径的毛细管进行了锥形处理,形成了150μm和50μm的尖端,从而生成了更小的薄壳双乳液。
3、调节内相压力:通过改变内相(IP)的压力,能够控制双乳液的壳厚度。增加内相压力可以形成相对较薄的壳厚度,适用于微载体和合成细胞的生成。
4、形成多室双乳液:通过调整外相(OP)压力,可以形成含有2到4个水相核心的多室双乳液。这涉及到在第一个接头处形成核心油包水(W/O)液滴,然后在第二个接头处将其包裹在外相中,形成多室双乳液。
5、使用不同的脂质溶剂:测试了三种不同的中间相溶剂(矿物油、油酸和1-辛醇),成功生成了薄壳双乳液,进一步证明了设备的灵活性和兼容性。
6、不同的形成模式:研究中探讨了三种不同的双乳液形成模式,包括顺序滴落、同时滴落和双滴落,发现双滴模式在形成薄壳双乳液时最为有效。
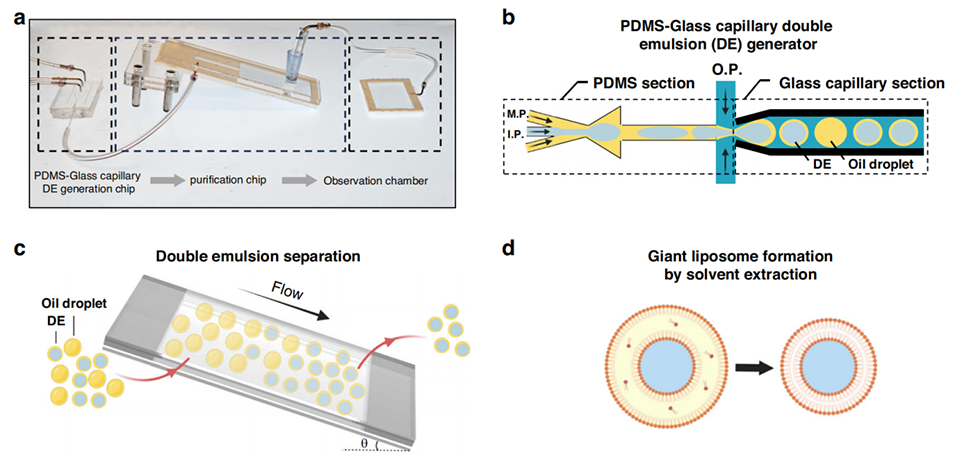
图1.展示了所提出的微流控平台的实验设置,包括PDMS玻璃毛细管双乳液生成芯片和串联纯化芯片,最终在观察室中获得分离的双乳液样品。
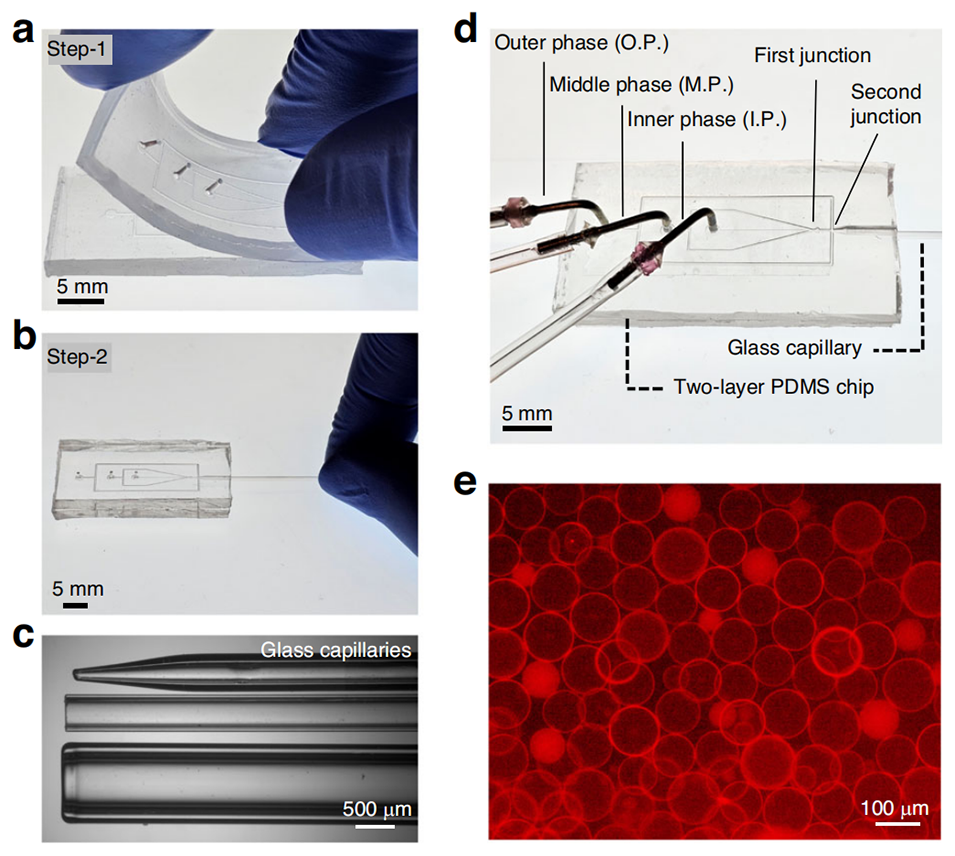
图2.描述了混合PDMS玻璃毛细管设备的组装过程,第一步是将两个相同的PDMS复制品粘合在一起,第二步是将玻璃毛细管插入PDMS芯片的出口通道。图中还展示了不同直径的毛细管用于形成不同尺寸的双乳液。
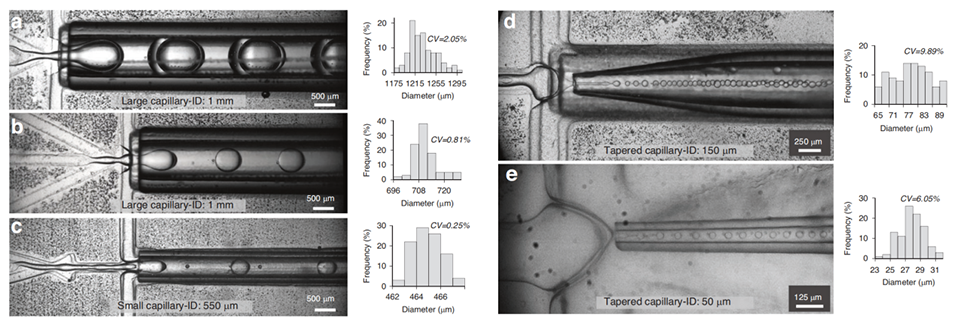
图3.展示了使用混合装置形成薄壳水包油包水(W/O/W)双乳液的尺寸可调性。包括使用大口径毛细管形成的直径为1.2mm和700μm的双乳液,以及使用小口径毛细管形成的直径为464μm、77μm和27μm的双乳液。

图4.展示了PDMS玻璃毛细管装置的可调性,包括通过内相压力控制双乳液的壳厚度、形成含有2到4个水相核心的多室双乳液、使用不同的中间相(油相)形成薄壳双乳液。
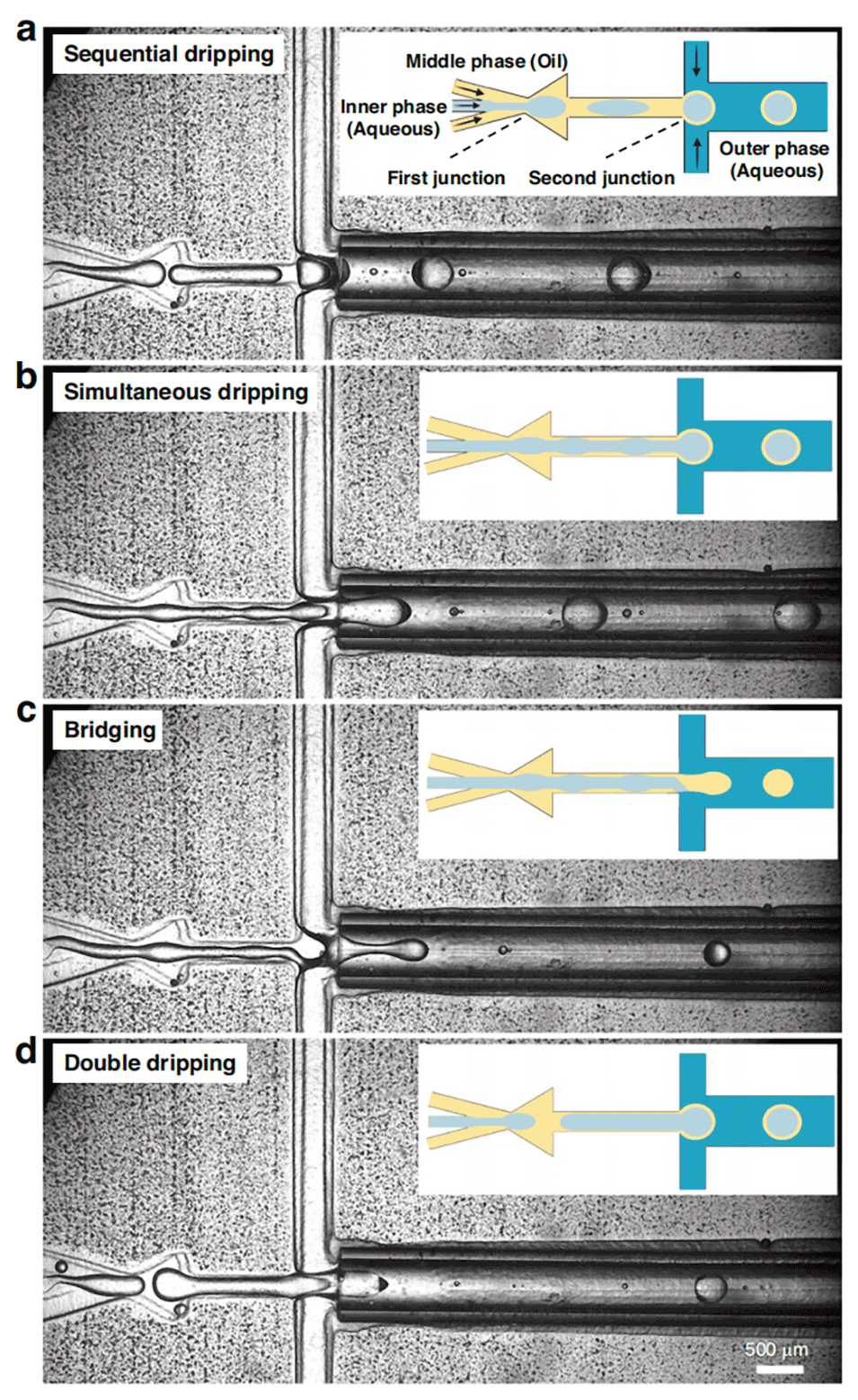
图5.展示了不同的薄壳双乳液形成模式,包括顺序滴落、同时滴落、桥接现象和双滴落模式。在示意图中,不同的相位由不同的颜色表示。浅蓝色(IP)、黄色(MP)和深蓝色(OP)。

图6.展示了从油滴中分离双乳液的方法,利用浮力和流速差异实现分离,图中展示了双乳液和油滴在通道中的位置。

图7.分离芯片成功从油滴中分离出双乳液。包括分离芯片中油滴和双乳液分布的图像,以及分离前后样品的比较,展示了该分离方法的有效性。
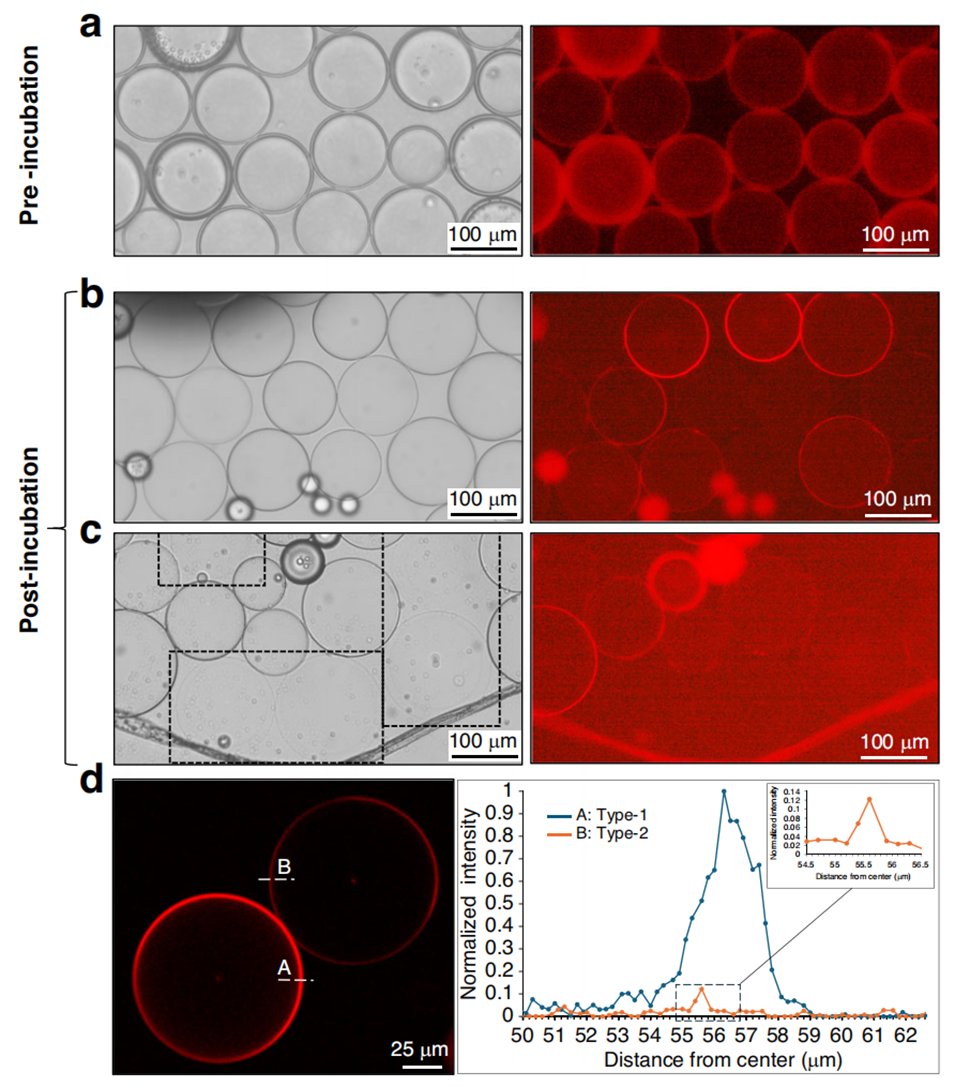
图8.通过溶剂提取法由双乳液模板形成巨型脂质体的过程。包括双乳液和形成的两种不同类型脂质体的亮场和荧光显微镜图像,脂质体的共聚焦图像及其相应的膜荧光强度剖面。
论文链接:
https://doi.org/10.1038/s41378-024-00815-0














