
导读:
近期,北京石油化工学院乔娟教授团队利用微流控液滴系统合成了以胃蛋白酶和胰蛋白酶为保护剂的金纳米粒子,并探讨其在铜离子和L-半胱氨酸检测中的应用,旨在为生物活性分子的检测提供有效策略。相关研究以“Protein@AuNPs Synthesized by Microfluidic Droplet System and Application in Cu(II) and L-Cysteine Sensing”为题目,发表在期刊《Chemical Research in Chinese Universities》上。
本文要点:
1、本研究通过微流控液滴系统合成了以胃蛋白酶(Pepsin)和胰蛋白酶(Trypsin)为保护剂的金纳米粒子(AuNPs),分别命名为Pepsin@AuNPs(Pep@AuNPs)和Trypsin@AuNPs(Try@AuNPs)。
2、与传统的烧瓶合成方法相比,微流控液滴系统合成的AuNPs表现出均匀的成核、优异的紫外线吸收性能、高稳定性和较短的制备周期(15分钟)。
3、Pep@AuNPs对Cu(II)的检测范围为1.0—100.0 μmol/L,检测限为0.3 μmol/L;Try@AuNPs对L-半胱氨酸的检测范围为0.3—250.0 mmol/L,检测限为0.1 mmol/L。
4、这种通用方法为以蛋白质为保护剂的AuNPs检测生物活性分子(如金属离子和氨基酸)提供了一种有效的策略。
微流控液滴系统在金纳米粒子(AuNPs)合成中的主要技术优势包括:
1、均匀成核:微流控系统能够精准控制微量反应液流,从而实现高度均匀的成核过程,获得更窄的粒径分布。
2、高效传质与传热:微流控液滴具有较大的表面积体积比,显著提高了反应体系中的传质和传热效率,促进了反应的快速进行。
3、快速制备:与传统的烧瓶法相比,微流控液滴系统将AuNPs的制备时间缩短至15分钟,大幅提高了制备效率。
4、环境友好:微流控技术通过封闭系统避免了氧气暴露,提高了合成的安全性和产品的稳定性,减少了对环境的影响。
蛋白质作为保护剂在AuNPs合成中发挥以下重要作用:
1、稳定性增强:蛋白质通过其丰富的功能基团(如-SH、-NH2和-OH)与金纳米粒子表面结合,形成稳定的保护层,防止纳米粒子团聚。
2、功能化:蛋白质保护剂赋予AuNPs潜在的生物相容性和特异性功能(如选择性识别特定生物分子),适用于生物医学传感和检测。
3、紫外线吸收性能优化:蛋白质的存在显著提高了形成的AuNPs的紫外线吸收性能,有利于增强后续检测的灵敏度。
金纳米粒子(AuNPs)在生物医学领域具有广泛应用,主要包括以下几个方面:
1、药物递送:AuNPs可以通过表面修饰特定分子,用于将药物递送到特定的细胞或组织,提高药物的靶向性和治疗效果。
2、生物传感器:AuNPs凭借其表面等离子体共振特性,可用于检测生物分子(如金属离子、氨基酸)或疾病标志物。
3、成像增强:AuNPs因其优异的光学和化学性能,可作为显影剂用于CT成像等医学诊断。
4、肿瘤治疗:AuNPs可用于光热疗法,通过吸收近红外光产生热量,从而破坏肿瘤组织。
5、免疫学研究:AuNPs与蛋白质(如SARS-CoV-2刺突蛋白受体结合域)的结合,用于诱导免疫应答,具有广阔的疫苗开发潜力。
AuNPs因其稳定性、尺寸可控性及功能化潜力,成为生物医学领域中重要的研究方向。
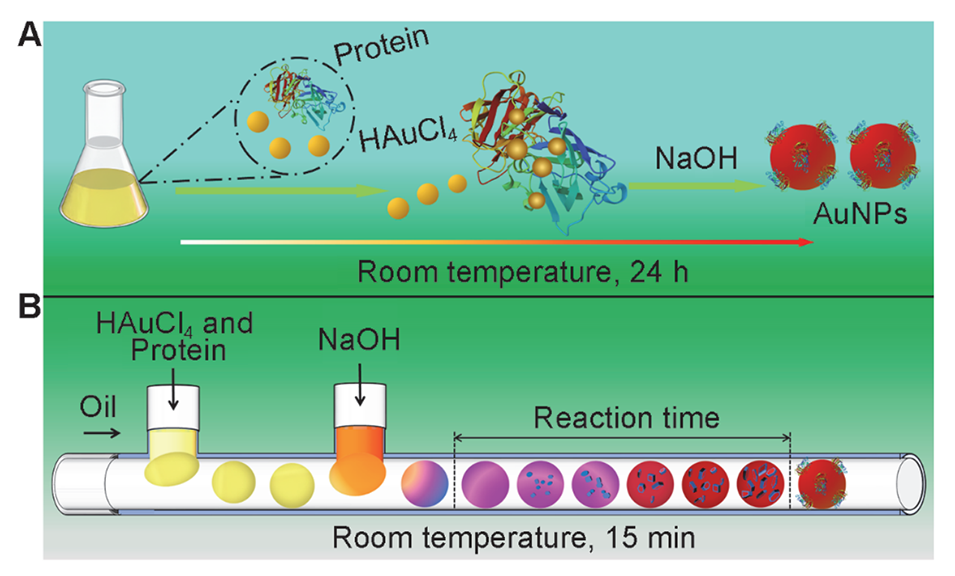
图1.在烧瓶(A)和微流控液滴系统(B)中制备蛋白质@AuNPs的过程和原理
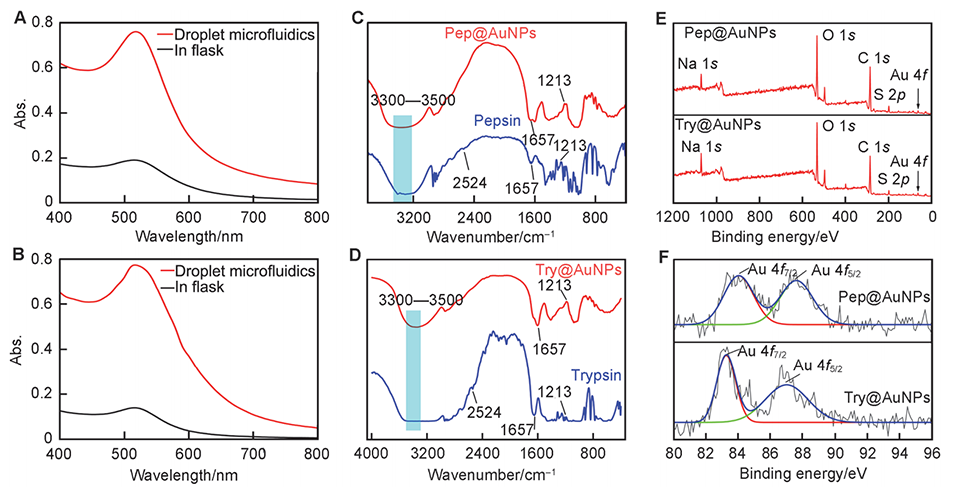
图2.通过微流控液滴系统和烧瓶合成的Pep@AuNPs(A)和Try@AuNPs(B)的吸收光谱。胃蛋白酶和Pep@AuNPs(C)以及胰蛋白酶和Try@AuNPs(D)的FTIR光谱。Pep@AuNPs和Try@AuNPs的XPS全谱(E),以及Pep@AuNPs和Try@AuNPs中Au 4f的XPS光谱(F)
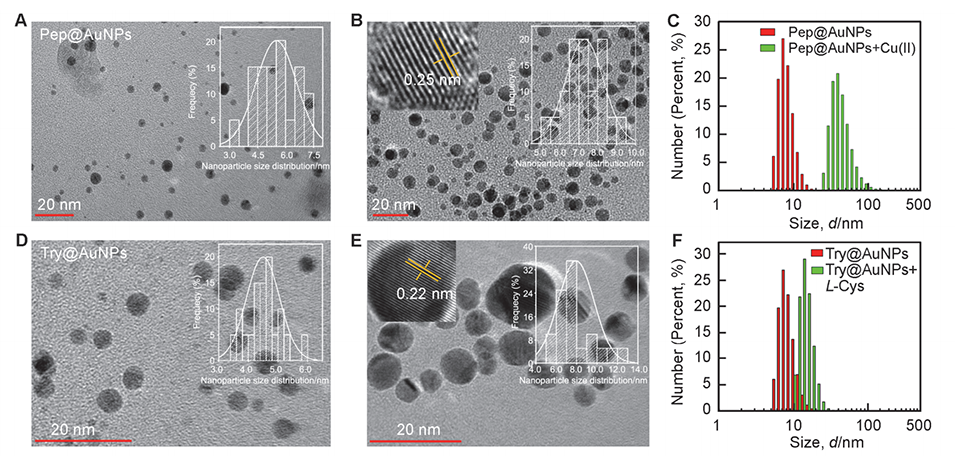
图3.Pep@AuNPs(A)和Try@AuNPs(D)的TEM图像,Pep@AuNPs(C)和Try@AuNPs(F)的DLS分析,添加Cu(II)后的Pep@AuNPs(B)和添加L-Cys后的Try@AuNPs(E)的粒径
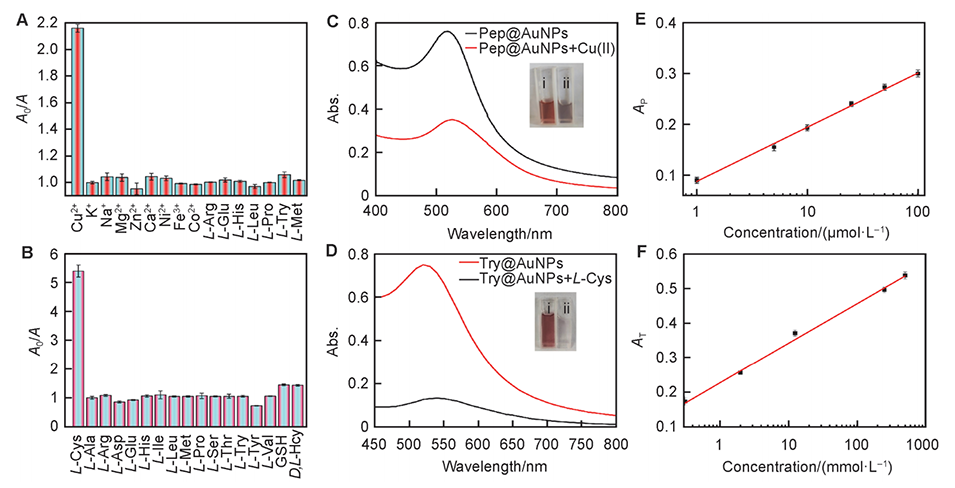
图4.存在50.0μmol/L K+、Na+、Mg2+、Zn2+、Ca2+、Ni2+、Fe3+、Co2+、L-Arg、L-Glu、L-His、L-Leu、L-Pro、L-Tyr、L-Met和5.0μmol/L Cu(II)时的A0/A值(A)。存在5.0 mmol/L L-Cys、L-ALa、L-Asp、L-Ile、L-Leu、L-Met、L-Ser、L-Thr、L-Tyr、L-Val、L-Arg、L-Glu、L-His、L-Pro、L-Try、GSH和D,L-Hcy时的A0/A值(B)。添加Cu(II)之前和之后Pep@AuNPs的吸光度值的变化(C)[插图:添加Cu(II)之前(i)和之后(ii)Pep@AuNPs的照片]。添加L-Cys之前和之后Try@AuNPs的吸光度值的变化(D)[插图:添加L-Cys之前(i)和之后(ii)Try@AuNPs的照片]。Cu(II)存在下的Pep@AuNPs(E)和L-Cys存在下的Try@AuNPs(F)的浓度标准曲线推导(每个数据点都来自三个重复的平均值和标准误差)
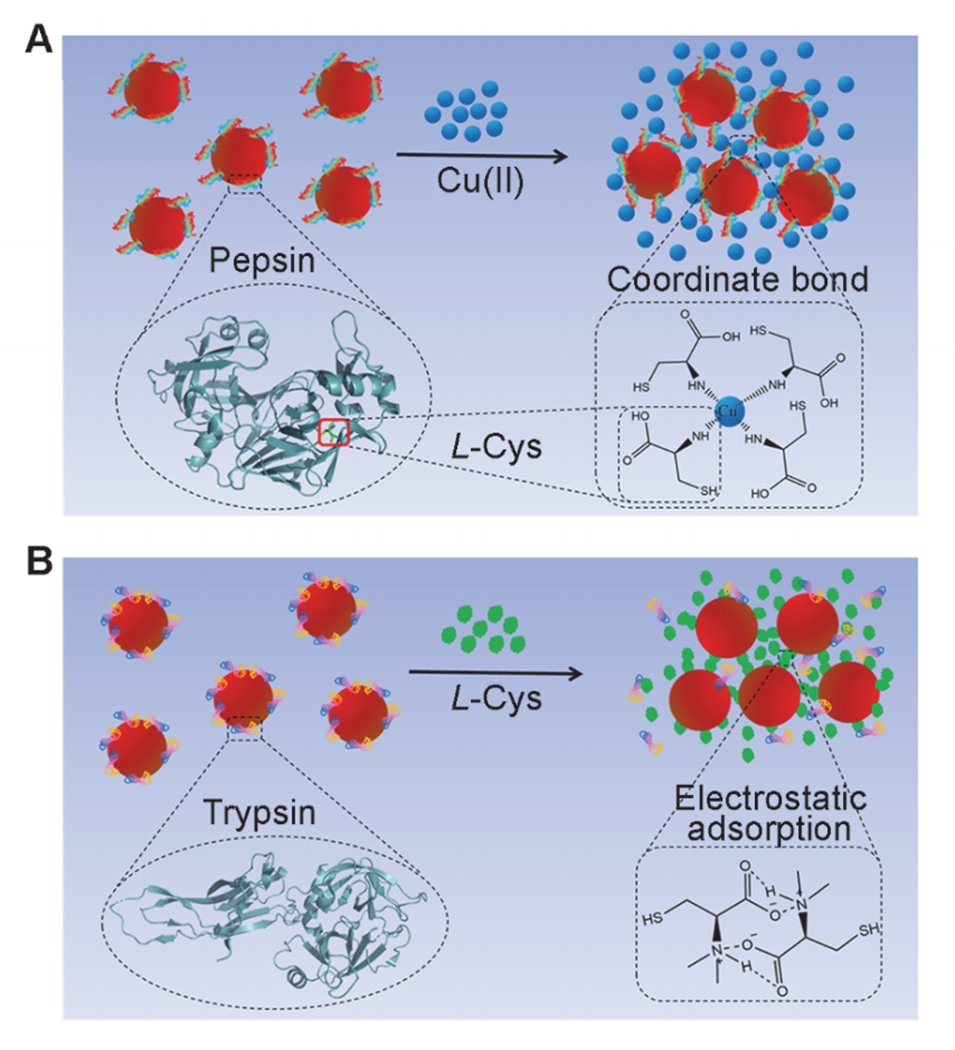
图5.Pep@AuNPs检测Cu(II)(A)和Try@AuNPs检测L-Cys(B)的原理
论文链接:https://doi.org/10.1007/s40242-025-4203-0














