人多能干细胞的微胶囊包封技术在组织工程、药物筛选及细胞治疗等生物医学应用中具有重要价值。微胶囊的作用多元,既能促进人多能干细胞聚集形成类球体,又能实现其体外规模化分化,还可在体内为细胞提供免疫隔离保护。目前已有多种细胞包封策略被报道,但胶囊的结构复杂度与制备通量之间往往难以兼顾。

鉴于此,梅奥诊所联合多单位开发了一种基于3D打印技术的高通量微流控设备,通过集成多喷嘴并行结构与主动频率调控,可在维持核壳结构微胶囊高均一性的同时将制备通量提升至1825 Hz,并成功实现了多种干细胞的高效封装与长期多能性维持。相关研究以“A 3D-Printed Compact Multi-Nozzle Microfluidic Device for Scalable Microencapsulation of Pluripotent Stem Cells”为题目,发表于期刊《Advanced Healthcare Materials》。
本文要点:
1、采用DLP 3D打印技术制备装置,相比传统PDMS软光刻技术,将设计到制备的周期缩短至2小时(单次可打印46个装置),装置占地面积缩小5倍;通过3D空间排布流体网络,打造出同轴流道结构,能稳定生成水凝胶壳-水相核的核壳微胶囊,还可通过调节流速、频率精准控制胶囊尺寸和壳层厚度。
2、单喷嘴装置微胶囊生成速率最高达181 Hz,在此基础上设计的10喷嘴并行装置,总生成速率提升至1825 Hz,理论上11-16分钟即可包封10亿个细胞,满足临床治疗的细胞量需求;引入电磁螺线管执行器实现主动频率调制,可独立于溶液粘度和流速控制液滴生成,保证微胶囊的均一性。
3、该装置成功包封肝癌细胞(HepG2、Huh7)、人胚胎干细胞(hESCs)和诱导多能干细胞(iPSCs),所有细胞类型的包封后存活率均>90%,包封效率最高达97.6%;包封的干细胞能在胶囊内快速聚集形成球状体,且在7天培养期内持续维持高多能性(Nanog、Oct4、Sox2等多能性标志物表达稳定),无明显分化。
4、选用PEG基水凝胶作为胶囊材料,相比海藻酸盐,其理化性质可精准调控,且胶囊为半透性结构,能实现营养物质和代谢物交换;采用油相交联的方式形成水凝胶壳,全程无油相残留影响细胞培养,还通过在壳相添加乙醇优化交联效率,解决了高流速下胶囊成型不佳的问题。
5、该3D打印微流控装置兼具高通量、小型化、可定制的特点,突破了传统微流控技术规模化的瓶颈,且包封过程不影响干细胞的多能性和细胞活性;未来可应用于干细胞的规模化分化、免疫隔离移植等再生医学领域,为细胞治疗的临床转化提供核心技术支撑。
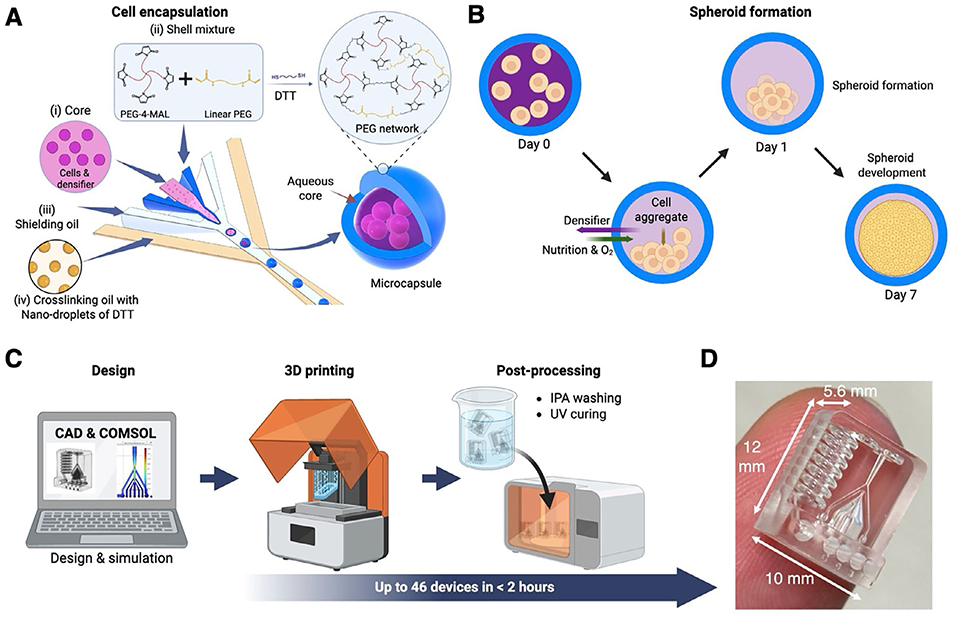
图1 本研究所采用的微胶囊封装及设备制造策略
微胶囊的制备过程主要分为以下几个关键步骤:
1、多相流体共流与液滴形成
微胶囊的制备在一个3D打印的同轴流道微流控设备中完成。设备具有四层同轴流道,分别输送:
核层液:含有细胞、密度梯度介质Optiprep及惰性PEG,用于调节粘度与密度;
壳层液:含有可交联的PEG前体(四臂聚乙二醇马来酰亚胺与丙烯酰胺-聚乙二醇-丙烯酰胺);
屏蔽油:含表面活性剂Span-80的矿物油,用于稳定核-壳结构液滴;
交联油:含二硫苏糖醇交联剂的矿物油,用于引发壳层凝胶化。
四相流体在喷嘴处形成稳定的共流结构,核-壳液滴被屏蔽油包裹,在油相中生成油包水包水(W/W/O)双乳液液滴。
2、壳层交联与微胶囊固化
液滴离开喷嘴后进入蛇形混合通道,交联油中的DTT分子通过界面扩散进入壳层,与PEG前体发生迈克尔加成与点击化学反应,迅速形成PEG水凝胶外壳,而核心保持液态。蛇形通道提供了约10秒的停留时间,确保壳层充分交联后再收集。
3、主动频率调制优化液滴生成
在喷嘴处集成了电磁阀执行器,可对屏蔽油流施加周期性脉冲(最高100 Hz)。这一设计使液滴剪切过程独立于溶液粘度和流速,即使在高粘度或高流速的射流模式下也能实现均匀、可控的液滴生成,显著提升胶囊的均一性。
4、收集与后处理
制备完成的微胶囊从设备出口收集于油相中,随后经100 μm细胞筛过滤,用无菌PBS洗涤三次去除残留油相和未反应试剂,最终转移至细胞培养基中进行培养。
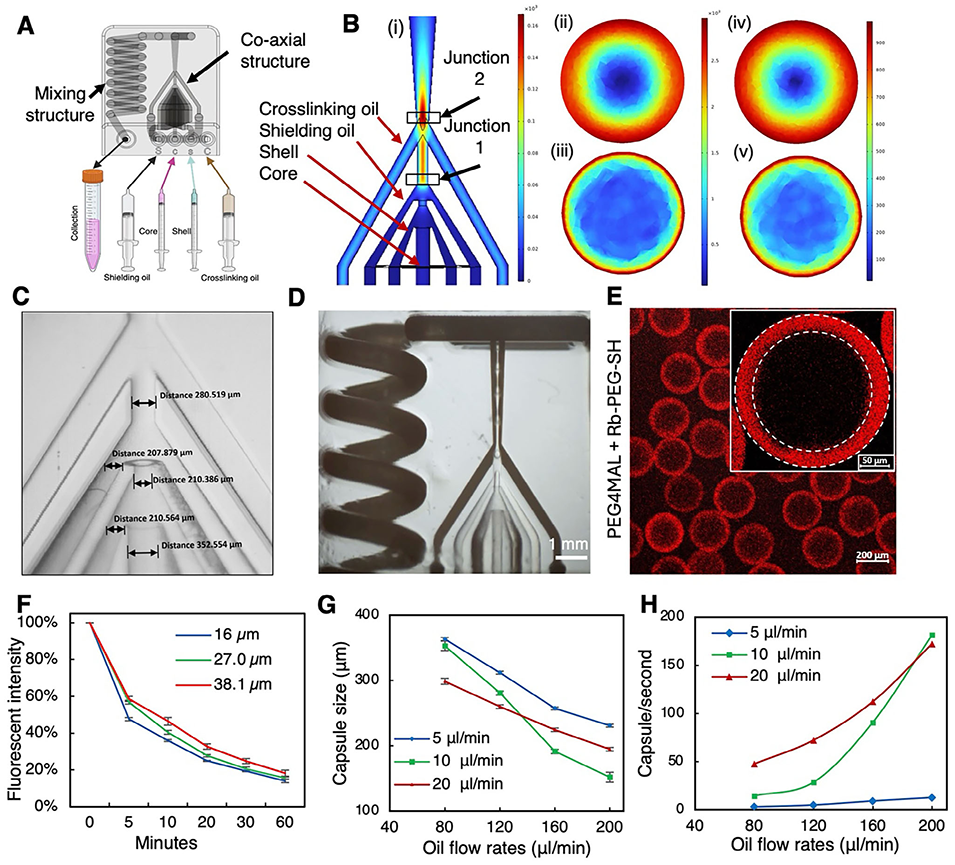
图2 探索3D打印封装装置中控制胶囊生成的操作条件
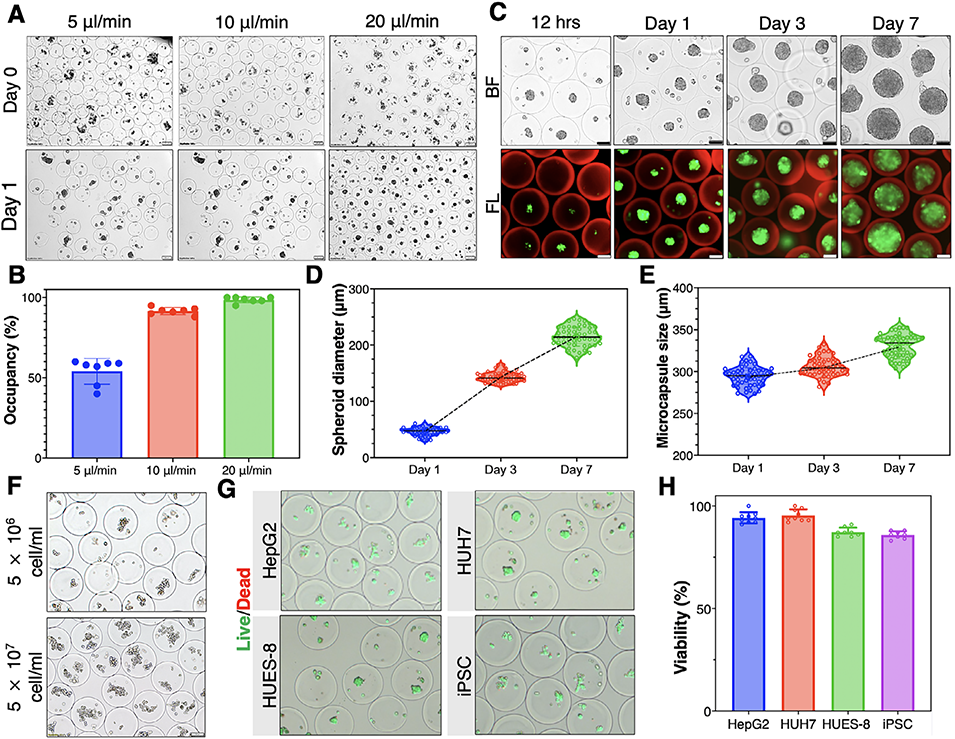
图3 封装效率、细胞球体形成及细胞活力评估
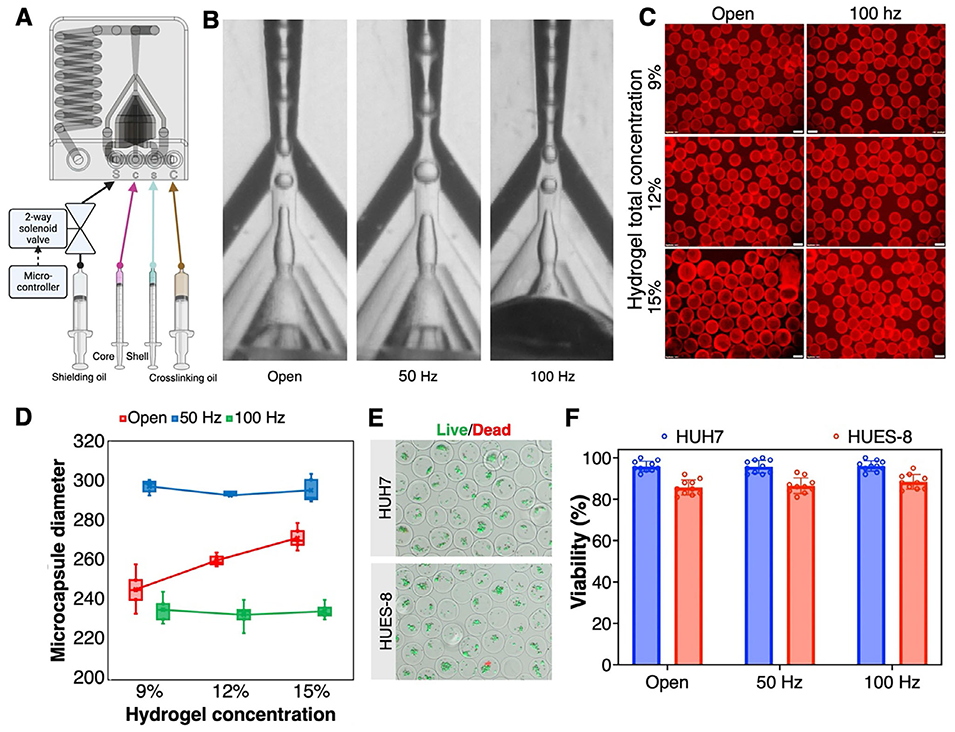
图4 主动频率调制对3D打印微流控系统中微胶囊形成的影响
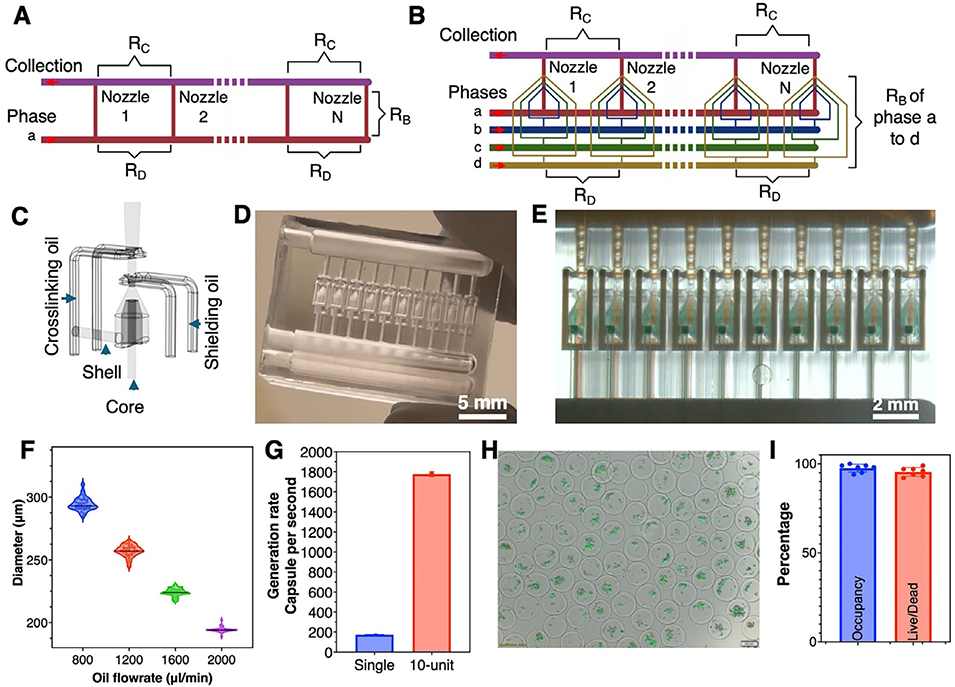
图5 利用并行化微流控装置实现核壳微胶囊的规模化制备
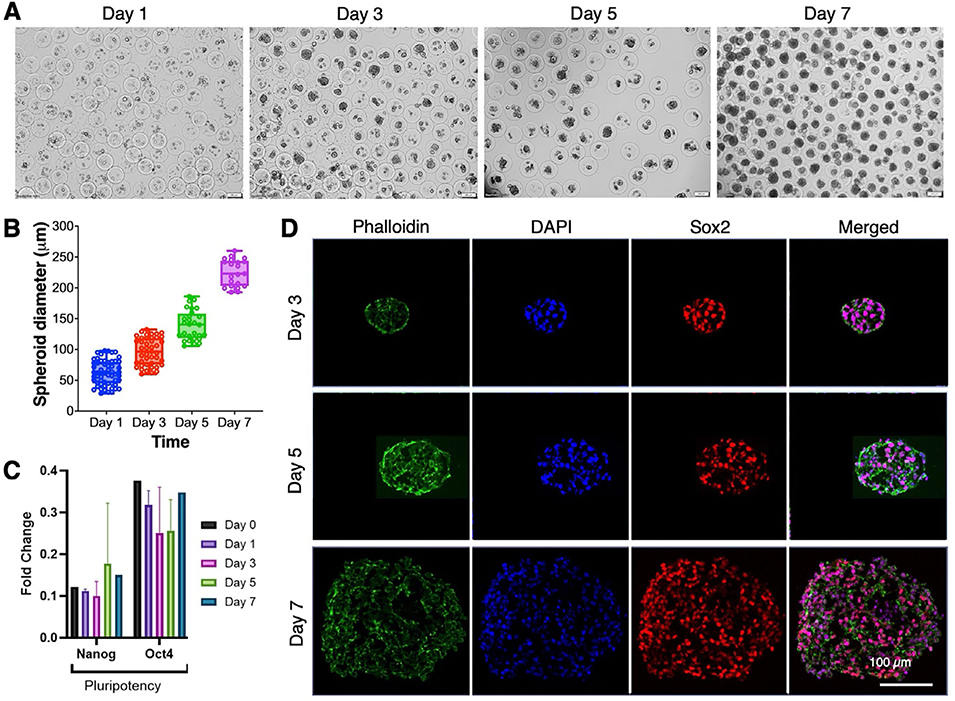
图6 封装人胚胎干细胞(hESC)球体形成及多能性维持评估
论文链接:https://doi.org/10.1002/adhm.202600018














