
导读:
这项研究详述了一种利用微流控技术制备肠溶包衣液芯胶囊的创新平台,旨在实现益生菌(大肠杆菌Nissle 1917)的结肠定向递送。研究者通过水相两相系统(ATPS)构建了具有液态核心和水凝胶外壳的微胶囊,并结合计算流体动力学(CFD)模拟阐明了单核与双核形态的形成机理及其与包封性能的内在联系。实验证明,添加了壳聚糖和Eudragit S100涂层的胶囊能有效抵御胃酸侵蚀,在模拟胃肠道环境中保持极高的菌株存活率。
该系统利用结肠特有的碱性pH值和微生态酶(葡聚糖酶)触发释放,成功实现了益生菌的高效包裹与精准部位释放。这种集成化的微流控方案为治疗胃肠道疾病提供了一种具备高保护性、环境响应性且可扩展的递送策略。相关研究以“Microfluidic fabrication of enteric-coated liquid-core ATPS capsules for colon-targeted probiotic delivery”为题目,发表在期刊《Food Hydrocolloids》上。
本文要点:
1. 核心创新与胶囊结构
多层保护架构:开发了一种三层结构的微胶囊,包括:
液体核心:基于 PEG 的液体核心,用于装载益生菌,相比固体基质能提供更温和的环境并支持快速释放。
水凝胶外壳:由葡聚糖(dextran)、海藻酸盐和 Ca-EDTA 组成,在芯片上通过离子交联形成。
功能化涂层:采用层层沉积(LbL)技术,涂覆壳聚糖(chitosan)以延缓酸渗透,并涂覆 Eudragit S100 纳米颗粒作为肠溶屏障。
释放机制:胶囊结合了 pH 响应(Eudragit S100 在中性/碱性环境下溶解)和微生物酶触发(葡聚糖酶降解外壳中的葡聚糖)双重机制,确保在结肠部位精准释放。
2. 微流控平台与数值模拟
数值模拟辅助设计:研究利用计算流体力学(CFD)模型阐明了流体粘度和通道约束(confinement)对液滴形成的影响。
形态控制:模拟发现,通道高度决定了内部循环模式:
受限几何形状会促进双核心形态的形成,但由于内部涡流可能将细菌推向外壳边缘,其包封率较低(3%)。
非受限几何形状则倾向于形成稳定的单核心结构,包封率显著更高,达到 1 ± 0.9%。
3. 生物学性能验证
卓越的胃肠道保护:
胃液环境:未涂层的胶囊在模拟胃液(SGF)中 2 小时后完全失去活力,而经过壳聚糖和 Eudragit 双重涂层的胶囊存活率保持在 2%。
小肠环境:在模拟小肠液(SIF)中暴露 4 小时后,总存活率仍能维持在 93%左右。
靶向释放性能:
胶囊在胃液中释放量极小,在小肠液中释放量也有限(6 小时约为 7%)。
在含有葡聚糖酶的模拟结肠液(SCF)中,由于外壳降解,7-8 小时内释放率达到 95–100%。
4. 研究结论
该研究证明了一个可扩展的微流控平台,能够通过精确控制胶囊的微观形态和多层化学特性,有效保护益生菌通过上消化道,并在结肠部位实现高效、精准的触发释放。
单核胶囊包封率显著高于双核胶囊的核心原因是什么?
核心源于通道限域诱导的内部流体动力学差异;约束通道下双核胶囊形成分区内部环流与中间剪切停滞层,会将部分 EcN 菌推至核 - 壳界面,被困于壳层中受交联环境损伤;而无约束通道下单核胶囊形成整体连续环流,益生菌被稳定保留在液核内,因此包封率更高(94.1±0.9% vs 85.3±2.6%)。
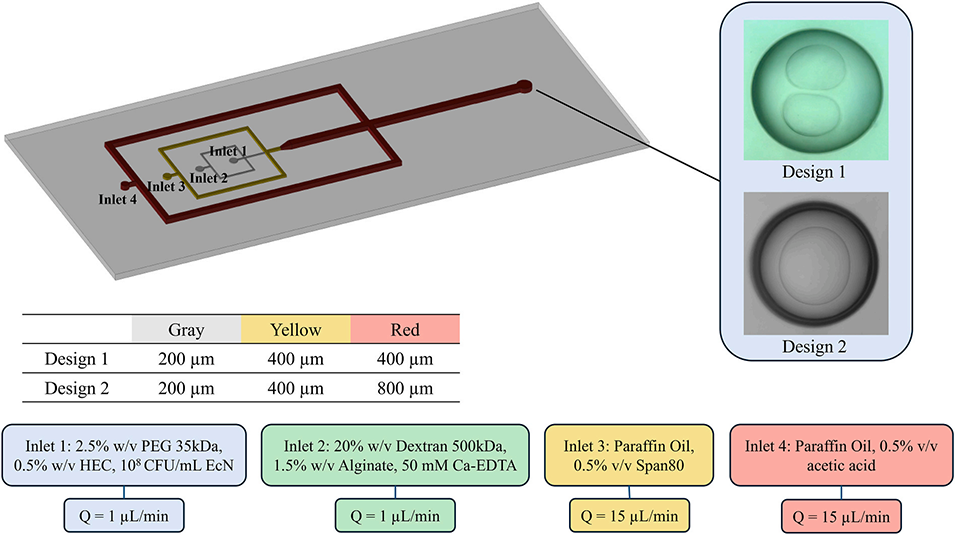
图1. 用于生成 ATPS 核壳液滴的流动聚焦微流控平台。
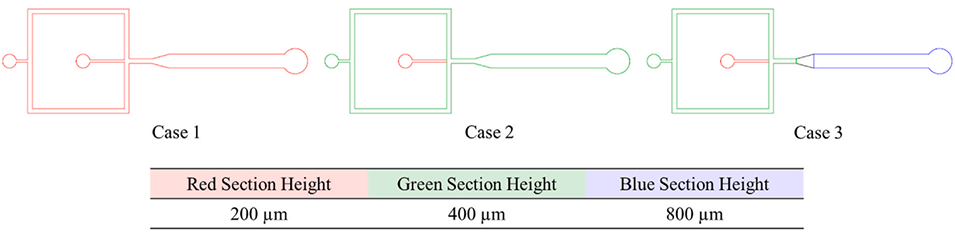
图2. 用于研究约束/高度变化对液滴形成影响的 CFD 几何形状。
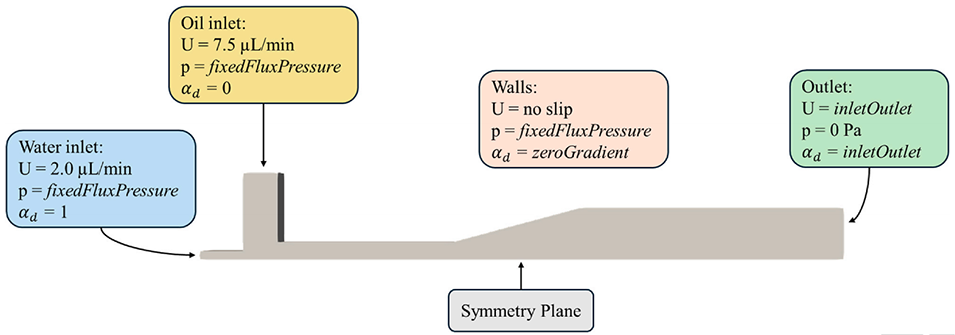
图3. VoF 模拟边界条件(入口流速、压力出口、无滑移/接触角壁面、对称性)。
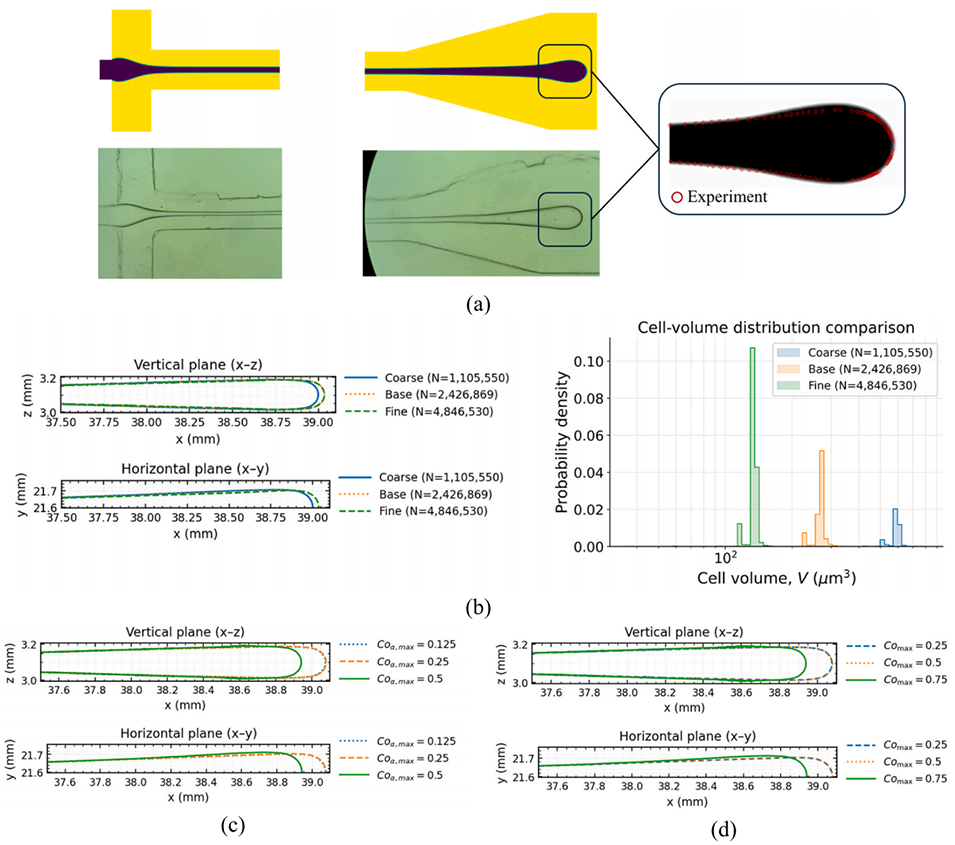
图4. 模型验证与数值灵敏度分析:(a) 模拟与实验结果的对比;(b) 网格独立性检查;(c–d) 通过 Courant 数和相 Courant 数限制进行的步长灵敏度分析。
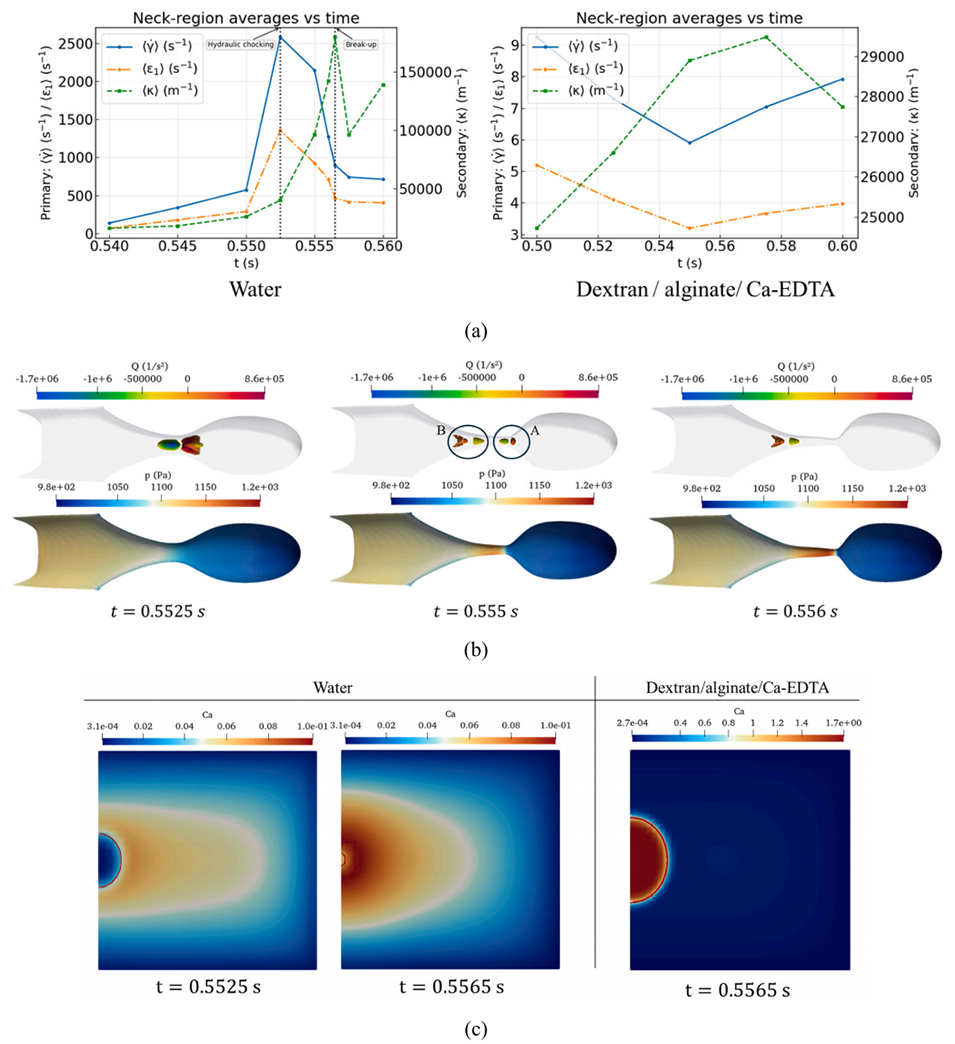
图5. 分散相粘度对流动聚焦接头处液滴形成的影响:(a) 水与葡聚糖/海藻酸盐/Ca-EDTA 溶液的颈部平均剪切速率、主伸展速率和曲率;(b) 穿过水力阻塞(hydraulic choking)和断裂开始时的 Q 准则(Q-criterion)等值线图及相应的压力场;(c) 突出颈部附近外部主导(水)与内部主导(葡聚糖/海藻酸盐)粘性阻力的毛细管数(Capillary-number)等值线图。
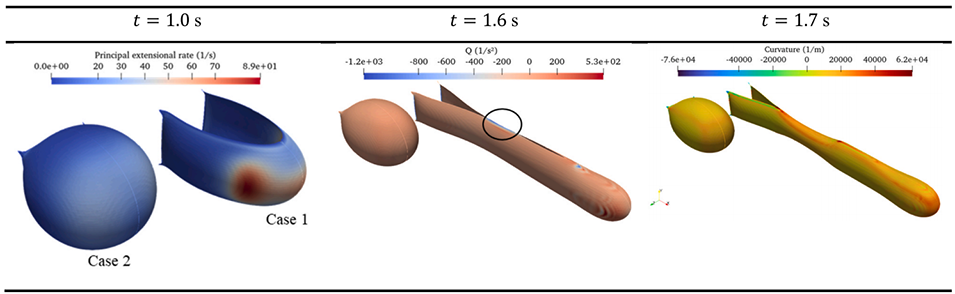
图6. 受限几何形状(案例 1)的缩颈动力学(未发生断裂):主伸展速率、Q 准则和曲率的等值线图。
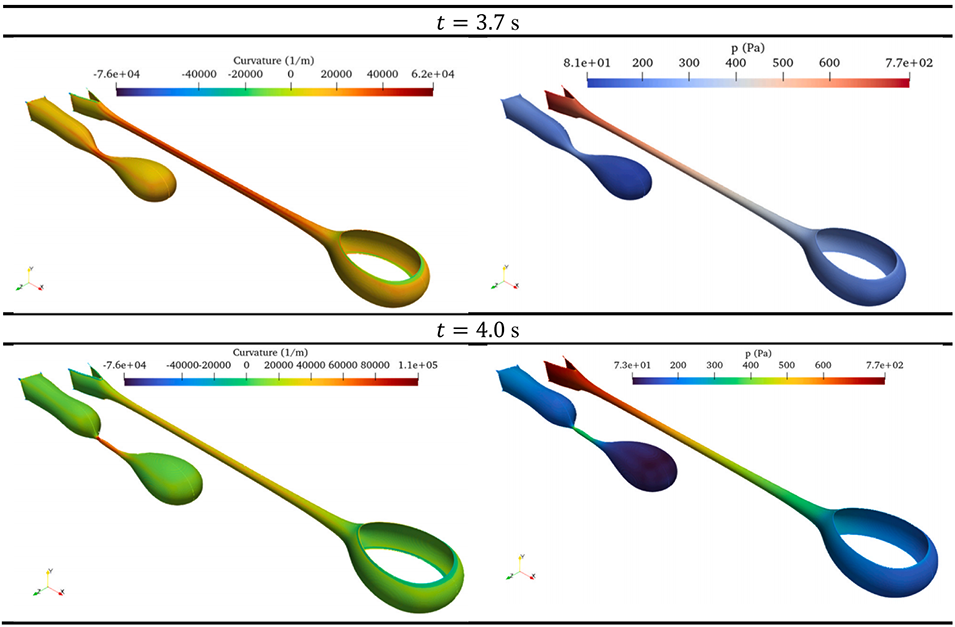
图7. 非受限几何形状(案例 2)的断裂机制:曲率场和压力场的演变,显示局部曲率-压力耦合不断加强并最终导致断裂(pinch-off)。
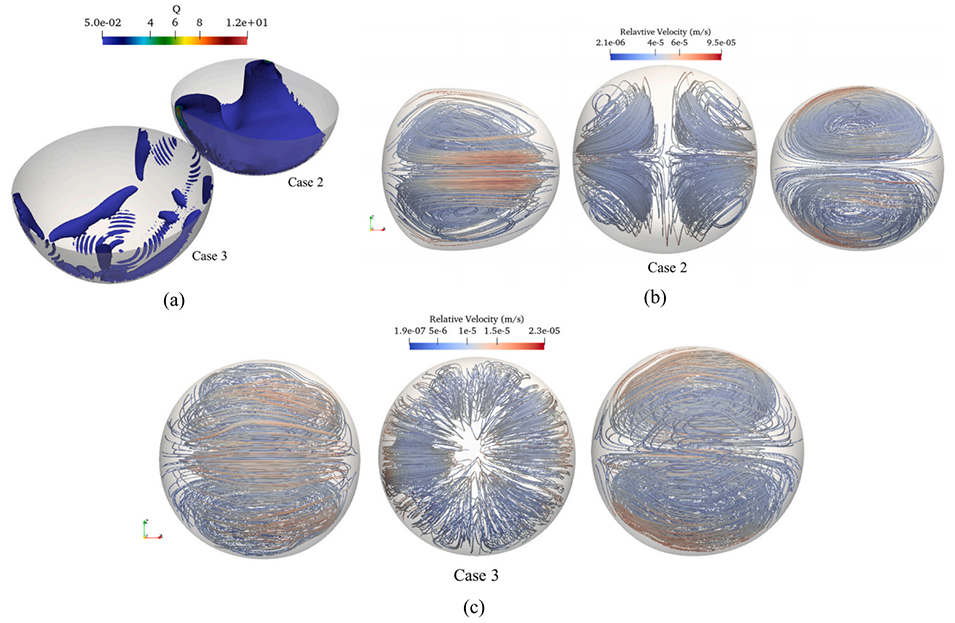
图8. 约束对涡旋结构和液滴内循环的影响:(a) 液滴周围的 Q 准则分布;(b–c) 三个正交视角的相对速度流线图。
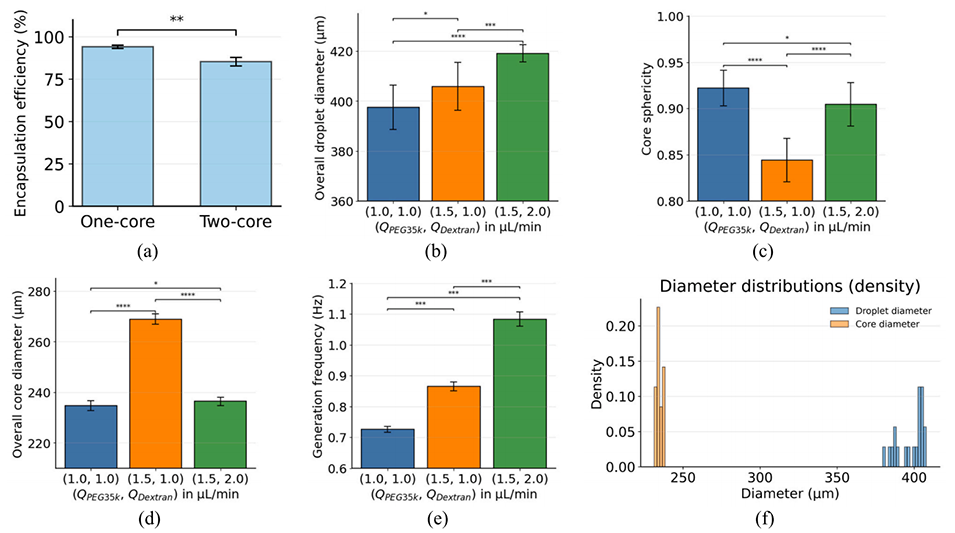
图9. (a) 单核与双核设计的包封率比较。PEG (35k) 和葡聚糖流速对 (b) 液滴总直径、(c) 核心球形度、(d) 核心直径、(e) 液滴生成频率的影响;(f) 在 QPEG (35k) 和 QDextran = 1μ L/min 时的核心和液滴尺寸分布。所有案例的油流速均为 15μL/min。
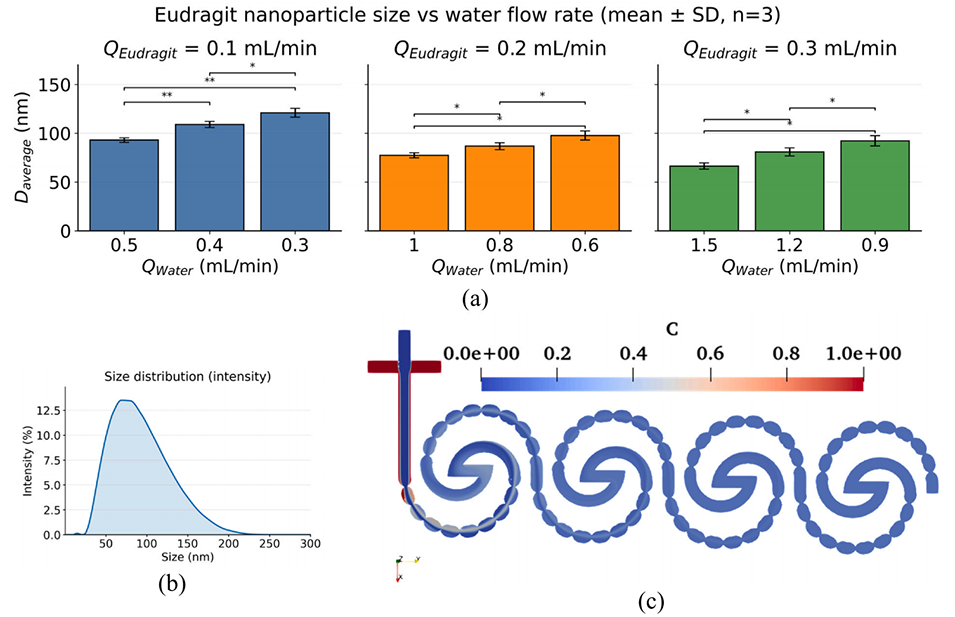
图10. (a) Eudragit 和水流速对纳米颗粒直径的影响;(b) QWater = 1.5μL/min 且 QEudragit = 0.3μL/min 时 Eudragit 纳米颗粒的强度加权 DLS 粒径分布;(c) 显示微混合器内浓度场的混合过程 CFD 模拟。
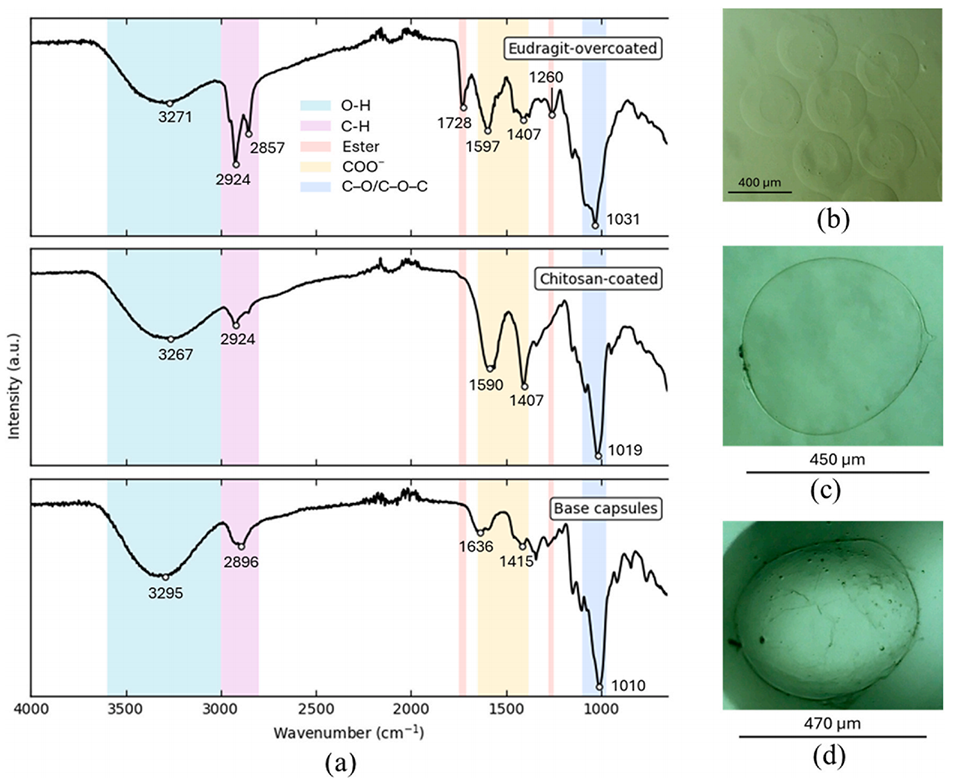
图11. (a) 未涂层、壳聚糖涂层和 Eudragit-壳聚糖涂层纳米颗粒的 FTIR 光谱;(b) 未涂层胶囊、(c) 壳聚糖涂层胶囊和 (d) Eudragit-壳聚糖涂层胶囊的共聚焦显微镜图像。
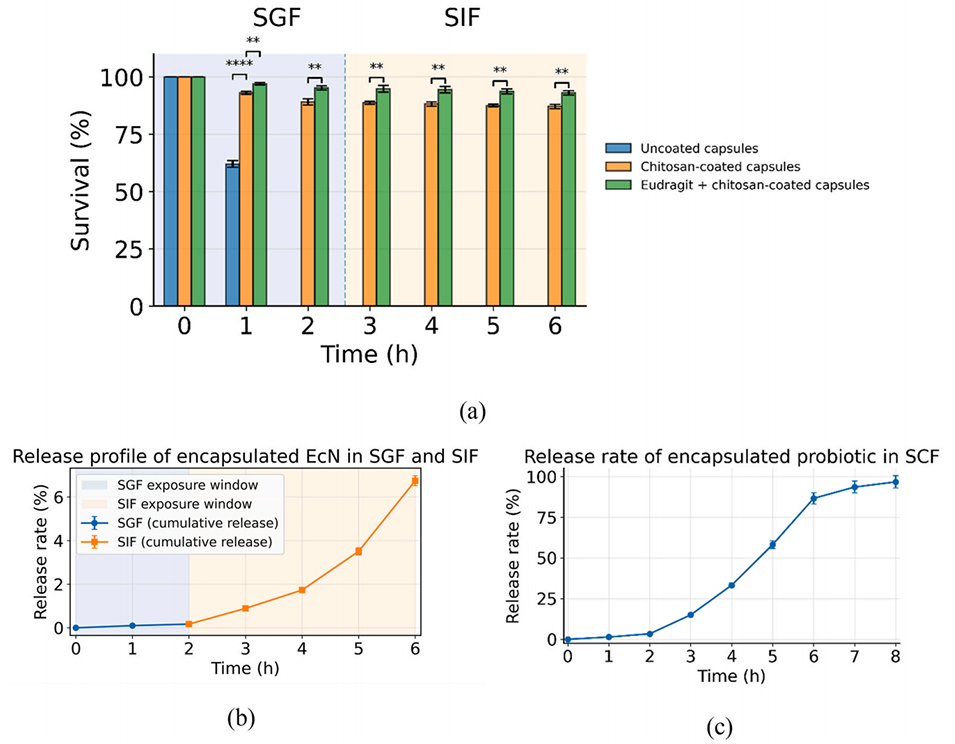
图12. (a) 封装的 EcN 在先后暴露于 SGF 和 SIF 过程中的存活率;(b) EcN 在 SGF 及随后 SIF 中的累积释放量;(c) 壳聚糖–Eudragit 涂层胶囊在含有葡聚糖酶的 SCF 中的释放曲线。
论文链接:https://doi.org/10.1016/j.foodhyd.2026.112828
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)
上一篇:液滴微流控技术构筑磁控软体微型机器人,用于精准药物输送
下一篇:暂无














