背景介绍:
关节软骨(AC)是一类特殊的结缔组织,它通过分散运动相关负荷和最小化相邻骨骼之间的摩擦来实现关节的平滑运动。然而,受损或退变的关节软骨修复仍然是一个重大的临床挑战,这主要归因于软骨的无血管和无神经特性,这些特性限制了其固有的愈合能力。值得注意的是,轻微的软骨损伤可能导致严重的关节退变,最终诱发骨关节炎。目前的治疗方法,如自体软骨细胞移植术、微骨折术和马赛克移植术,通常无法完全复制健康关节软骨的结构和功能,并且受到组织稀缺性、供体部位并发症、力学缺陷和宿主免疫反应等问题的困扰。因此,制定标准化的软骨损伤治疗方案和开发创新疗法极为艰难,这要求我们深入理解软骨生物学和其修复机制的复杂性。

导读:
近期,解放军总医院骨科医学部郭全义教授、唐佩福教授团队开发了一种创新性的关节软骨修复策略,通过模拟软骨陷窝结构设计了一种富含生长因子的复合微球(GFs@μS),能够实现顺序免疫调节和内源性关节软骨再生。相关研究以“Cartilage lacuna-biomimetic hydrogel microspheres endowed with integrated biological signal boost endogenous articular cartilage regeneration”为题目发表于期刊《Bioactive Materials》。
本文要点:
1、本研究开发了一种集成生物信号的软骨陷窝样水凝胶微球系统,能够实现顺序免疫调节和内源性关节软骨再生。
2、通过将软骨生长因子TGF-β3载入介孔二氧化硅纳米颗粒(MSN)中,并与胰岛素样生长因子1(IGF-1)一起封装在聚多巴胺(pDA)微球中,再与含血小板衍生生长因子-BB(PDGF-BB)的壳聚糖(CS)水凝胶混合,利用微流控技术生成了负载生长因子的复合微球(GFs@μS)。
3、pDA的加入降低了初期的急性炎症反应,而PDGF-BB的早期强效释放有助于吸引内源性干细胞。在随后几周中,IGF-1和TGF-β3的持续释放增强了软骨形成和基质沉积。
4、将该微球体系嵌入脱细胞软骨细胞外基质(ACECM),并与聚多巴胺修饰的聚己内酯(PCL)结构结合,成功构建了一种具有类软骨陷窝结构的组织工程支架,有效促进了软骨修复和髌骨软骨保护。
5、这项研究为优化生长因子输送和确保长期微环境重塑提供了一条战略途径,从而实现有效的关节软骨再生。
全文总结/概括:

为什么选择聚多巴胺(pDA)作为微球的封装材料?
1、抗炎特性:pDA具有一定的抗炎作用,能够减轻植入微球后的急性炎症反应,有助于为软骨修复创造一个更有利的局部环境。
2、抗氧化能力:pDA具有抗氧化性质,能够中和活性氧物质(ROS),保护细胞免受氧化应激损伤,这对于维持细胞健康和促进组织修复非常重要。
3、改善亲水性:pDA的修饰可以提高支架的亲水性,从而增强细胞对支架的粘附,为细胞增殖和分化提供支持。
4、免疫调节功能:pDA有助于诱导巨噬细胞向M2型极化,这种抗炎型的巨噬细胞对于促进组织修复和抑制炎症至关重要。
5、生物相容性:pDA具有良好的生物相容性,能够与多种生物分子和细胞相互作用,而不引起明显的免疫排斥反应。
6、机械性能改善:pDA的引入可以增强微球及其所构成支架的机械强度和稳定性,以适应关节软骨在日常活动中承受的力学负荷。
微流控技术在制备GFs@μS复合微球中发挥了哪些关键作用?
1、精确控制:微流控技术能够精确控制微球的尺寸、形状和组成,确保了产品的一致性和重复性。
2、多组分封装:该技术使得在微球中集成多种生物活性分子成为可能,例如同时封装TGF-β3、IGF-1和PDGF-BB,为实现复杂药物递送系统提供了技术基础。
3、提高效率:微流控技术提高了生产效率,能够快速、连续地制备大量微球,适合规模化生产。
4、优化释放特性:通过微流控技术,可以精确设计微球的内部结构,优化生长因子的释放动力学,实现控释效果。
5、定制化设计:微流控技术能够根据不同的治疗需求定制微球的物理和化学特性,为个性化医疗提供了可能。
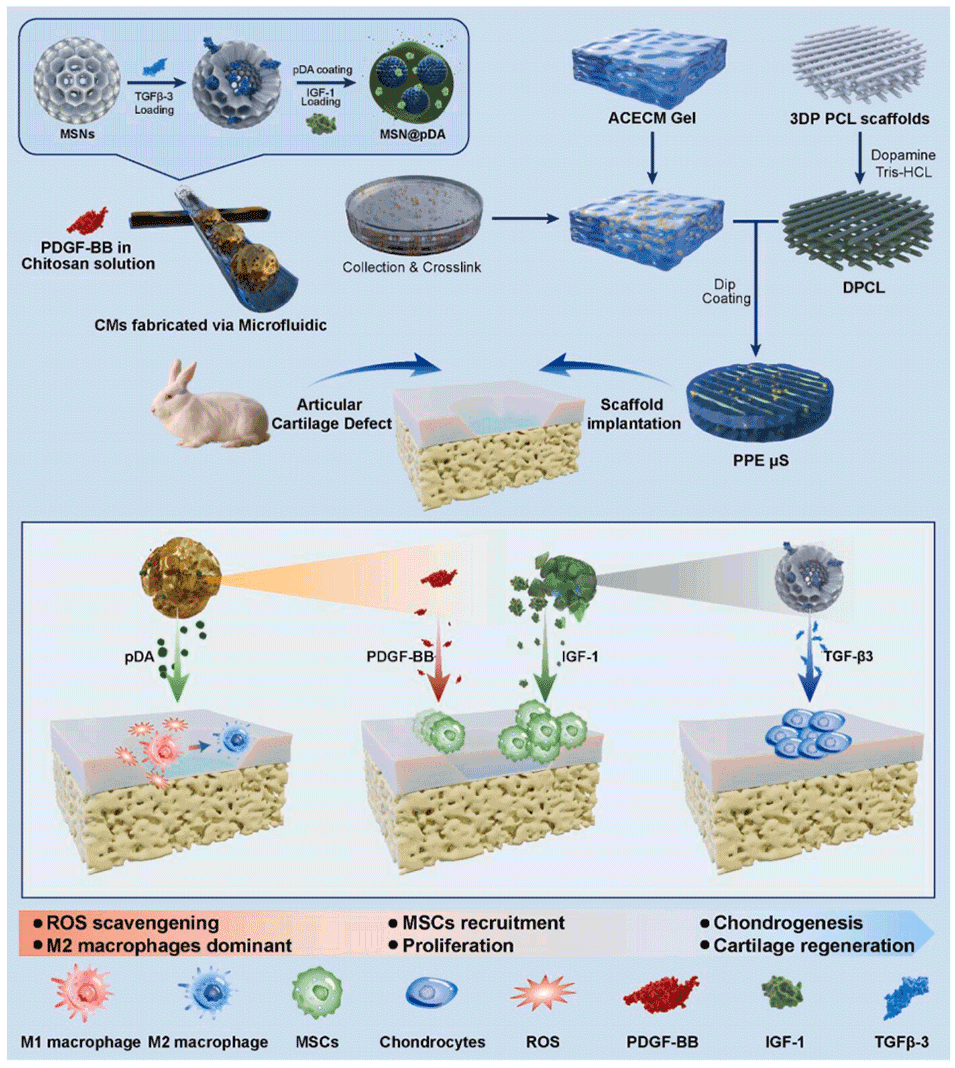
Scheme 1.软骨陷窝-仿生水凝胶微球支架及其作为软骨再生多功能治疗剂的应用示意图。
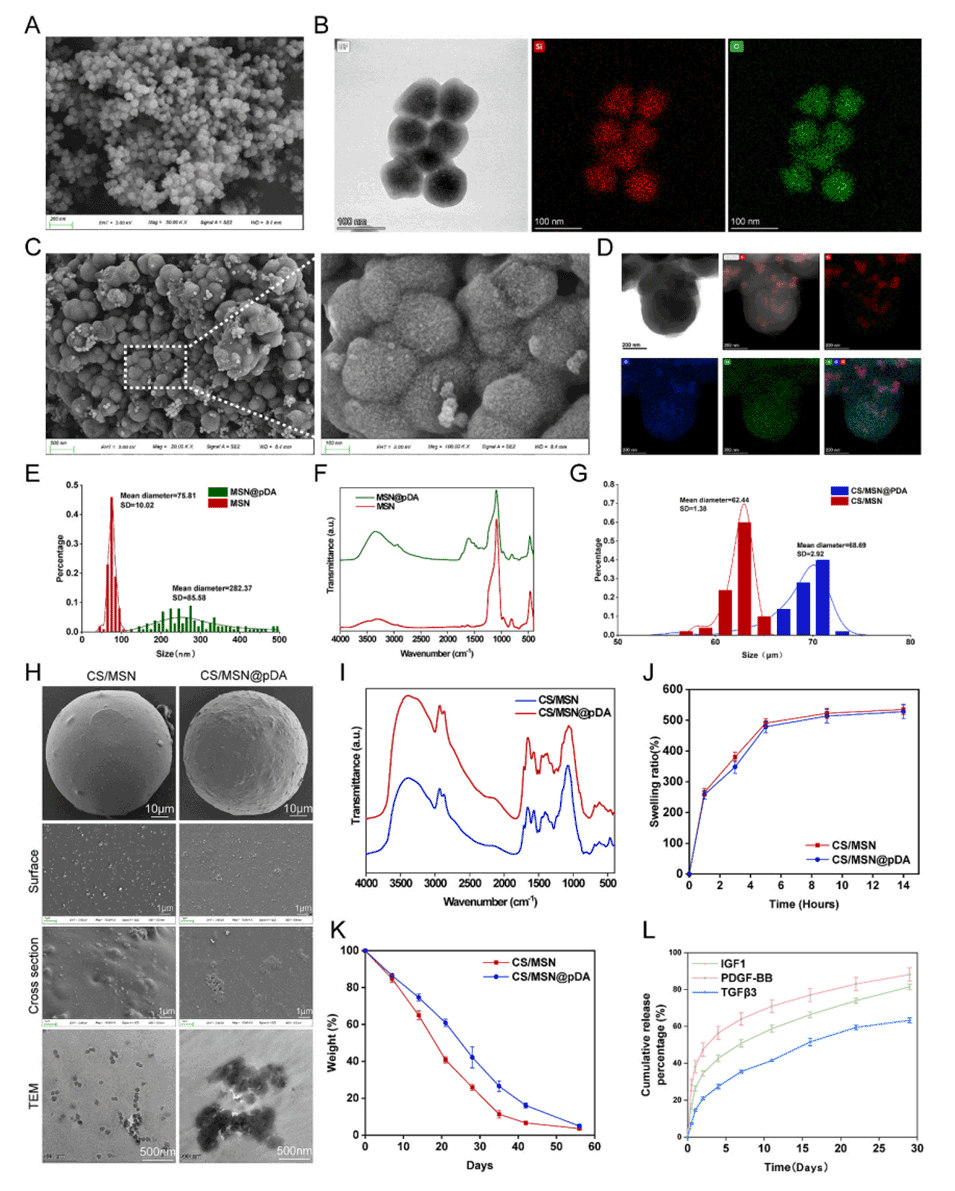
图1.μS的表征。
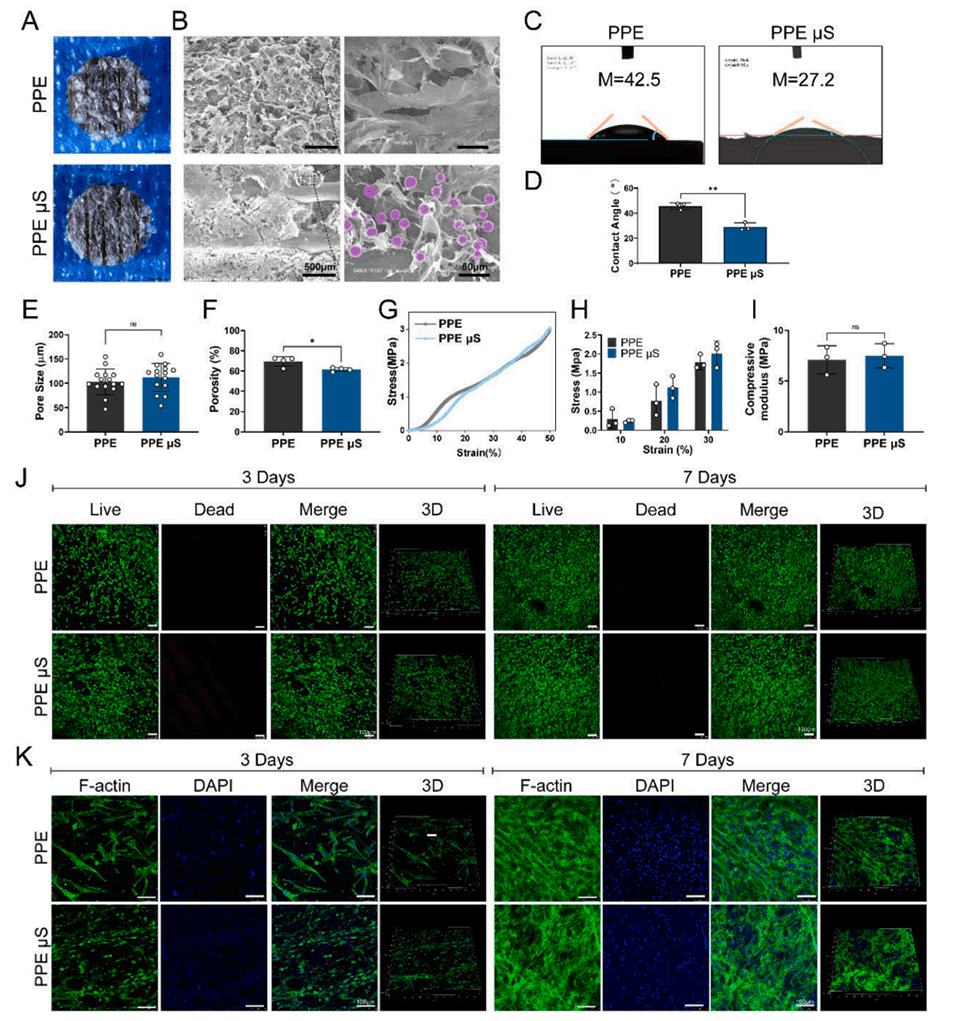
图2.复合支架的表征。
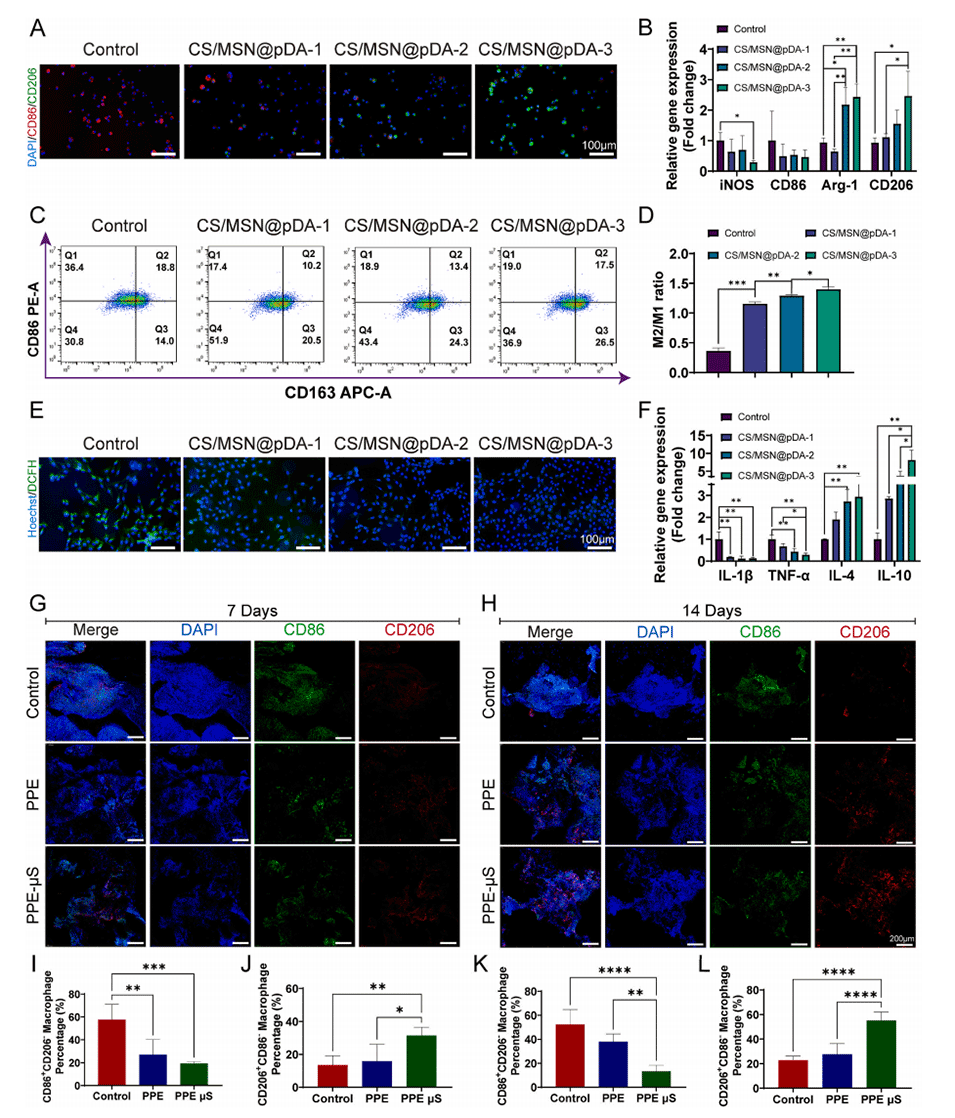
图3.μS和支架在体外和体内的剂量依赖性和免疫调节作用。
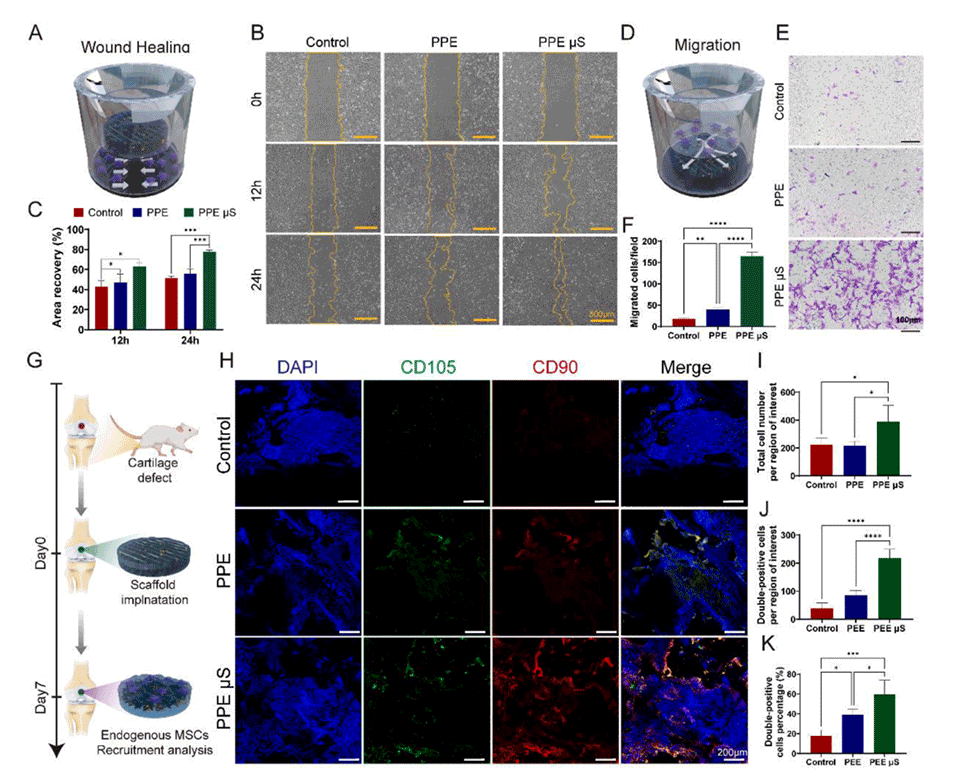
图4.负载GFs@μS的支架在体外和体内均促进了细胞迁移。
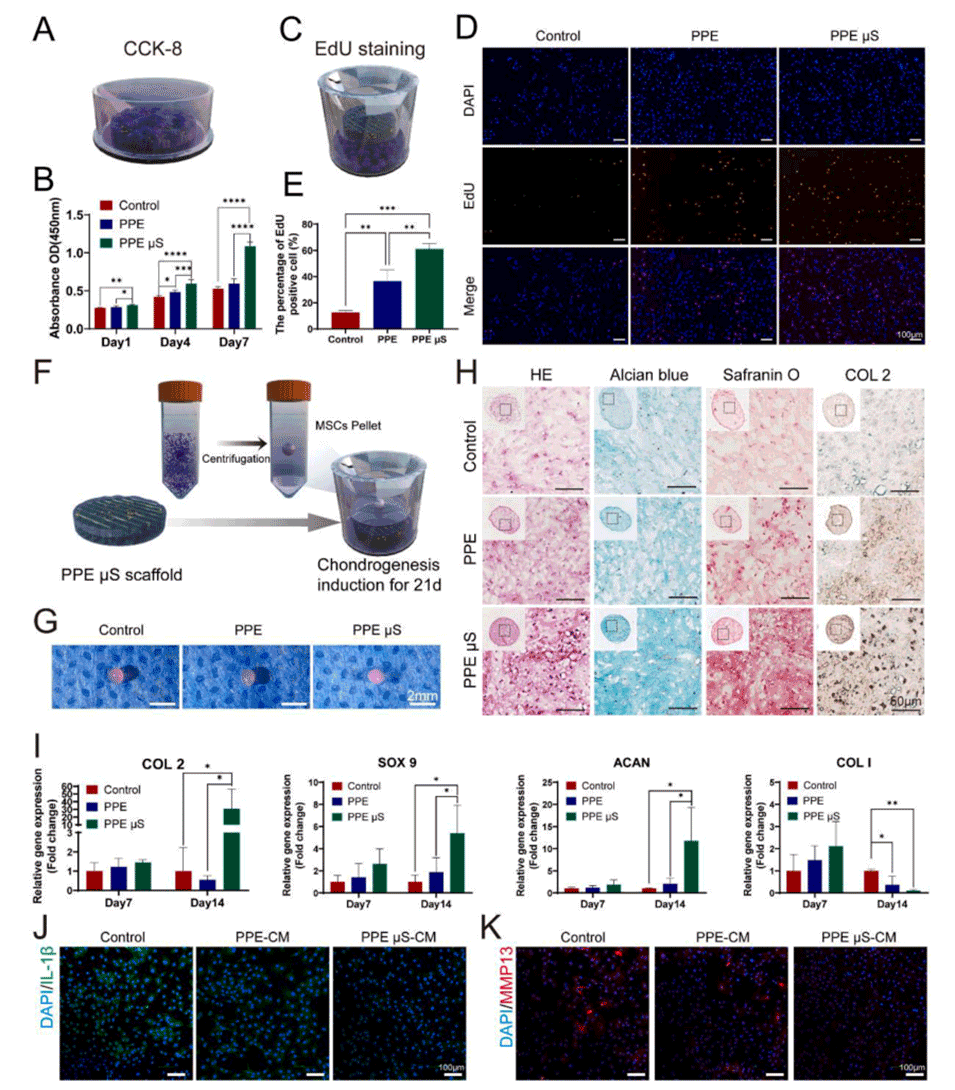
图5.增强体外细胞增殖和软骨生成。
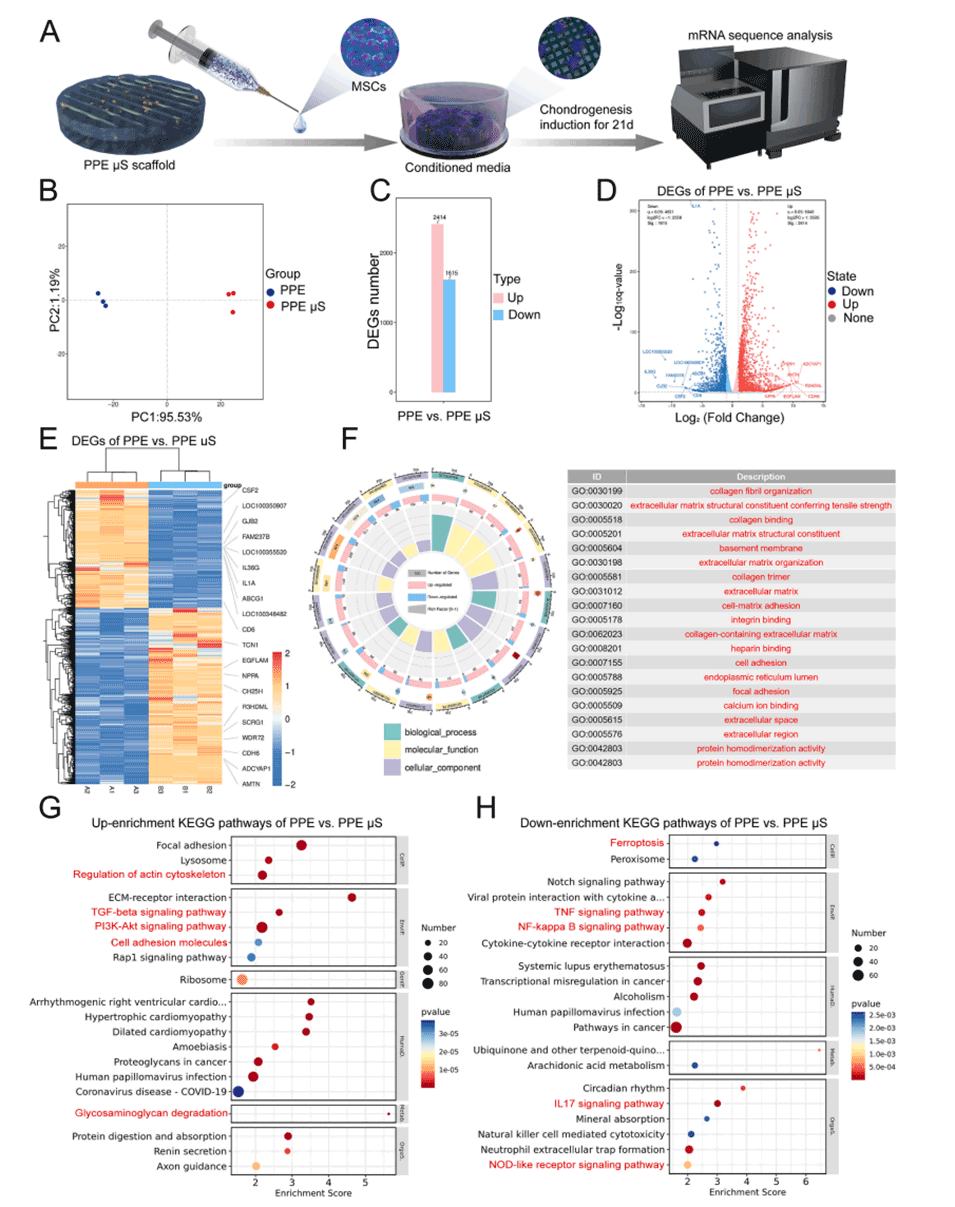
图6.在不同支架上培养21天的SMSCs的mRNA-seq数据和差异表达基因分析。
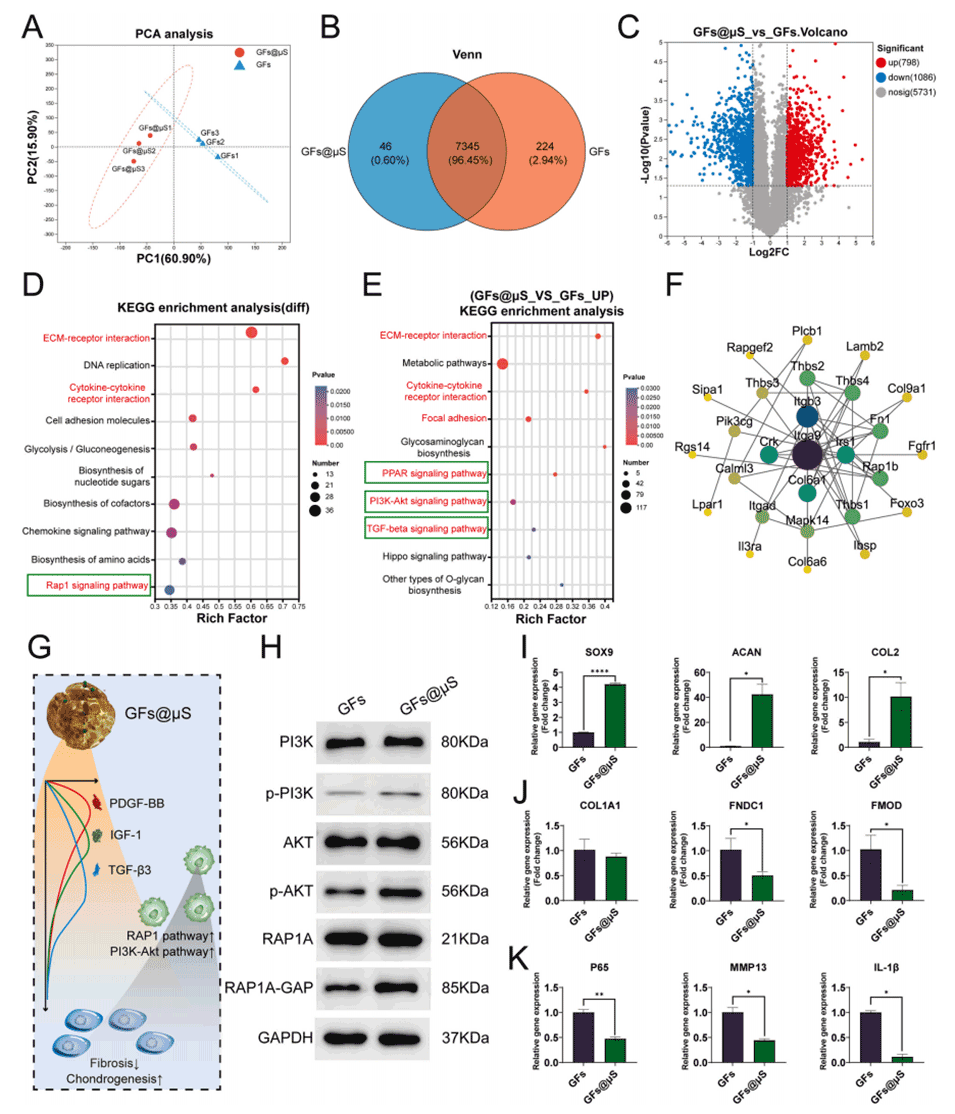
图7.GFs@μS可提高修复软骨组织的质量。
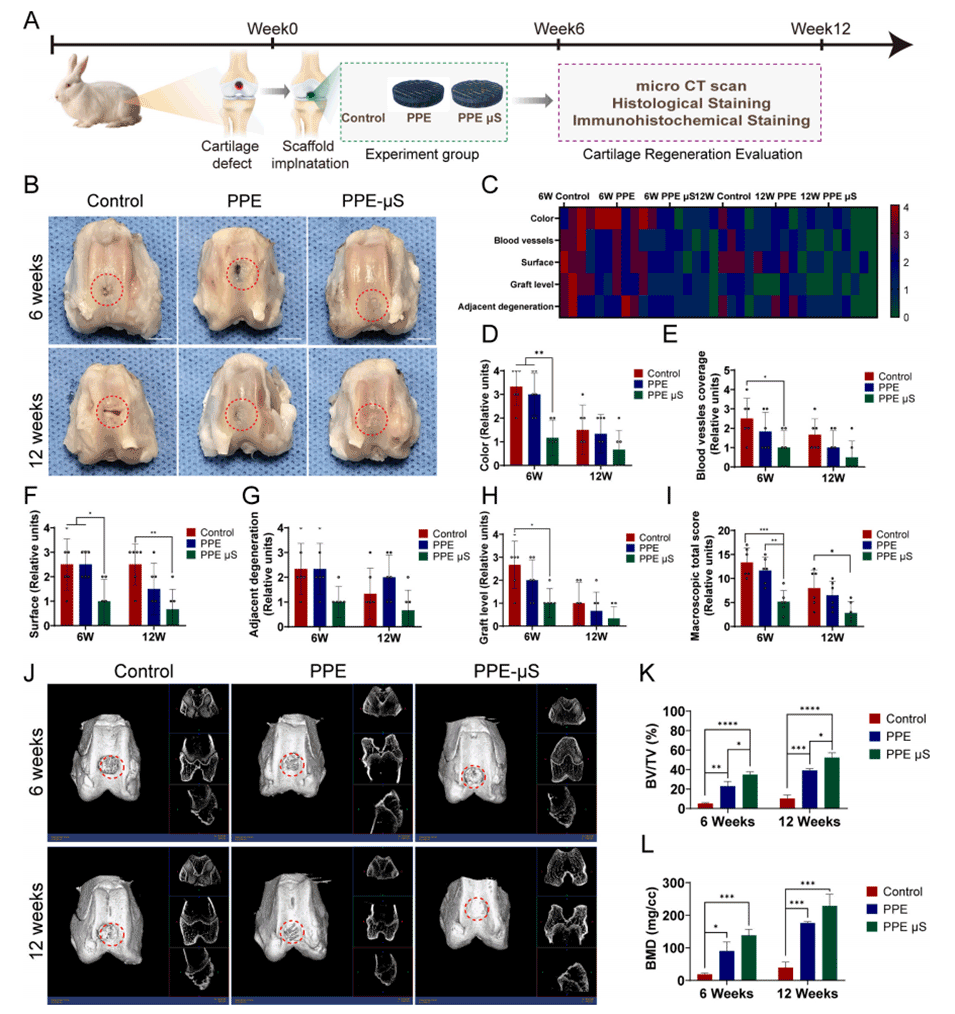
图8.PPE和PPE μS支架治疗软骨缺损后6周和12周软骨修复的宏观和微观CT分析。
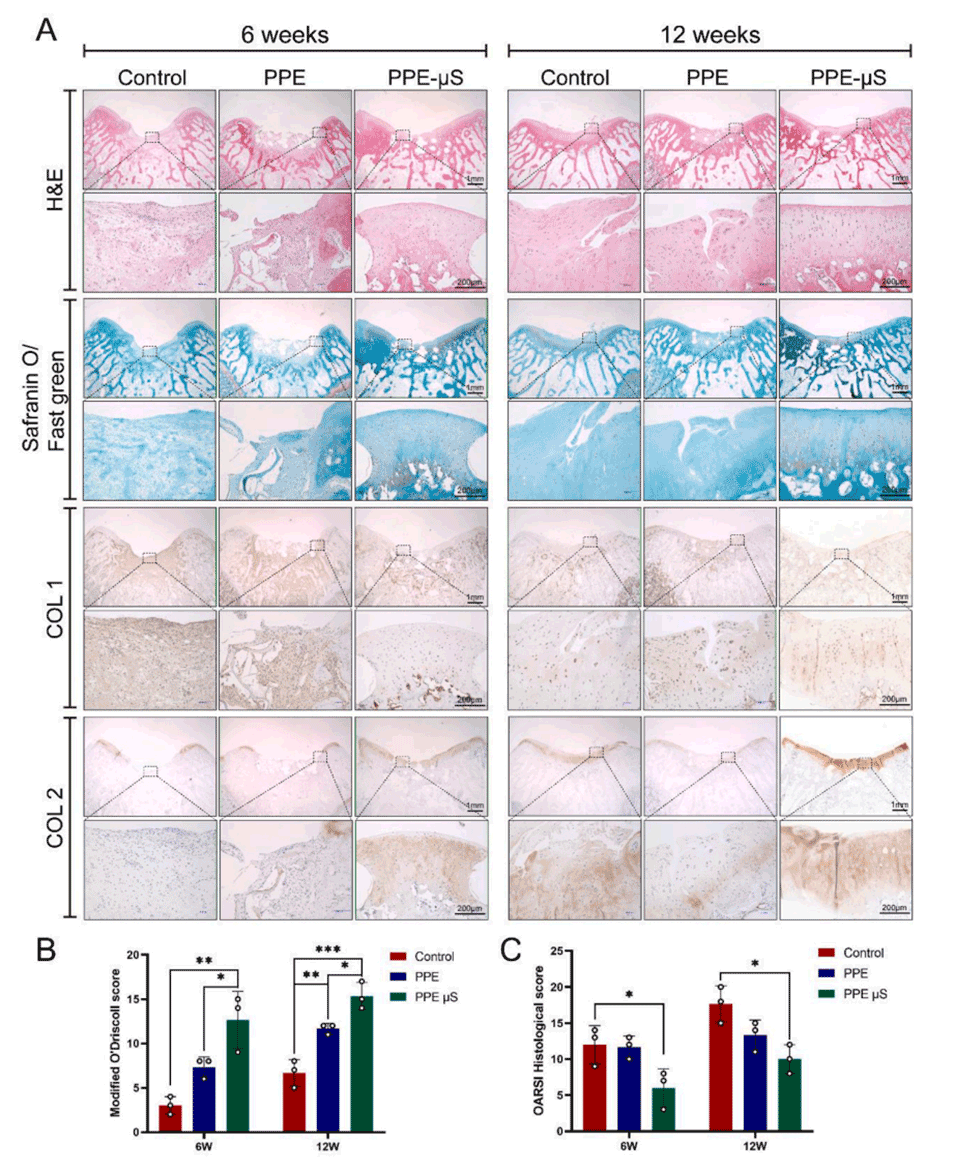
图9.对照组、PPE支架组和PPE μS支架组体内修复组织的组织学和免疫组化评估。
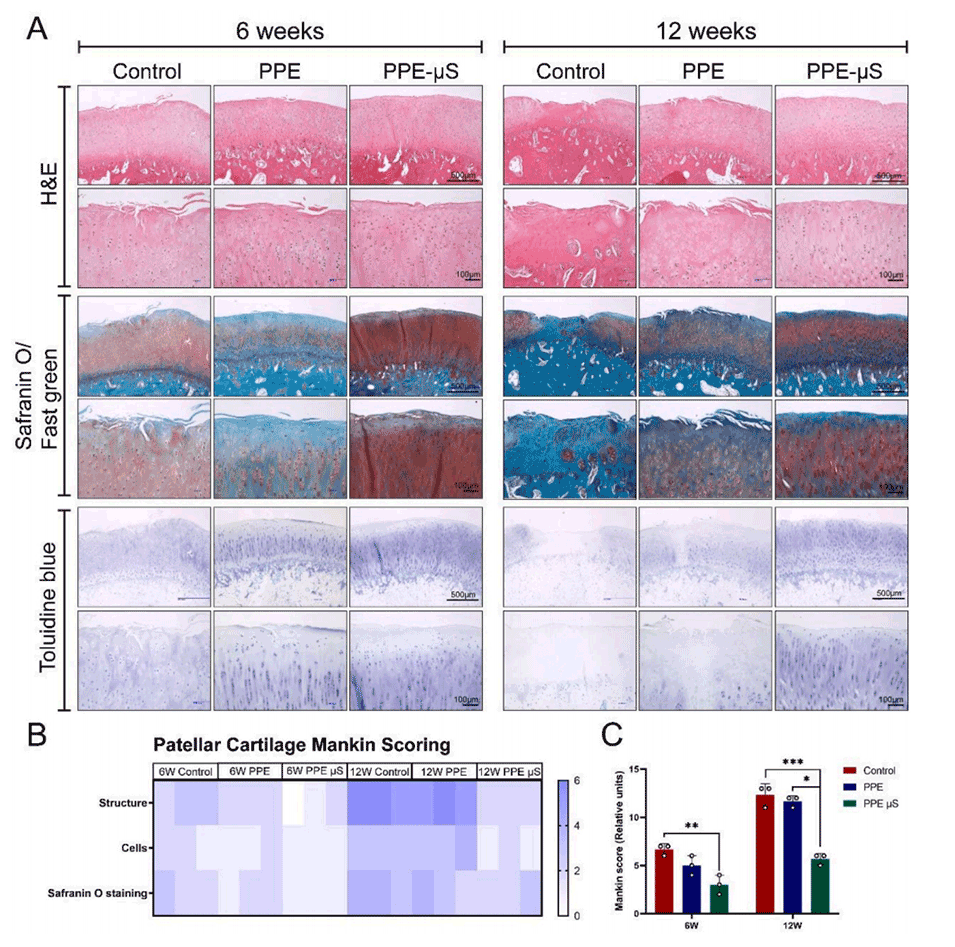
图10.PPE μS支架对全层软骨缺损兔膝关节的保护作用分析。
原文链接:https://doi.org/10.1016/j.bioactmat.2024.06.037














