间充质干细胞(MSCs)在再生医学中是一种重要的选择,但它们在维持细胞系和存活率方面面临挑战,因此其治疗潜力仍有待验证。由于直接注射的MSCs会被宿主免疫系统迅速清除,将活细胞封装在3D半透水凝胶基质中可以延长其在体内的滞留时间,这在提高治疗效果方面显示出巨大潜力。然而,水凝胶封装对MSC的不同亚群的影响尚不完全清楚。

近期,中国石油大学(华东)张丽媛教授、哈佛大学David A. Weitz院士等人使用液滴微流控技术制造了薄壳层海藻酸盐水凝胶微囊,通过调整海藻酸盐分子量来控制壳层的机械特性。相关研究以“Stiff hydrogel encapsulation retains mesenchymal stem cell stemness for regenerative medicine”为题目,发表在期刊《Matter》上。
本文要点:
1、本研究使用液滴微流控技术制造了薄壳层海藻酸盐水凝胶微囊,通过调整海藻酸盐分子量来控制壳层的机械特性。
2、结果发现,较硬的外壳比较软的外壳更能促进MSCs的增殖,并支持MSCs在体内的滞留。
3、单细胞RNA测序证实,坚硬的3D水凝胶还可以促进干性的维持。
4、本工作证明了水凝胶封装干细胞在长期治疗应用中的潜力,为调节MSC亚群以实现特定功能提供了新的见解。
全文总结/概括:
液滴微流控技术在制造海藻酸盐水凝胶微囊时如何实现对微囊壳层厚度的精确控制?
1、调整流速比:通过改变内相(水相)和中相(含海藻酸盐的溶液)的流速比,可以调节微囊壳层的厚度。较高的流速比有助于形成更薄的壳层。
2、控制酸浓度:在微流控过程中,通过调节用于触发海藻酸盐交联的酸浓度,可以影响壳层的形成速度和最终厚度。增加酸浓度通常会导致更快的交联和更薄的壳层。
3、优化收集通道长度:微囊在收集通道中的停留时间会影响壳层的厚度。较长的收集通道可以提供更多的时间用于壳层的形成和增厚。
4、使用Ca-EDTA作为交联剂:Ca-EDTA在酸性条件下释放Ca2+,触发海藻酸盐的交联反应。通过控制Ca-EDTA的浓度和反应时间,可以精确控制壳层的厚度。
5、后处理步骤:微囊形成后,可以通过如透析、离心等后处理步骤进一步调整壳层的厚度和均匀性,确保微囊的质量和一致性。
液滴微流控技术通过这些精确的控制手段,实现了对海藻酸盐水凝胶微囊壳层厚度的精确调控,为细胞封装和组织工程提供了强有力的工具。
使用硬质水凝胶微囊对间充质干细胞(MSCs)的好处:
1、增强细胞存活:硬质水凝胶微囊可以提供一个相对稳定的微环境,减少细胞受到的物理和化学损伤。这种保护性环境有助于减少宿主免疫系统的攻击,从而延长细胞在体内的存活时间。
2、维持干性:间充质干细胞的多能性是其重要的生物学特性之一。硬质微囊通过模拟细胞外基质的硬度,有助于维持MSCs的干性,减少它们向特定细胞系的分化,从而保持其再生和修复的潜力。
3、促进细胞粘附:细胞粘附是细胞与细胞外基质相互作用的重要过程,对于细胞的稳定和功能执行至关重要。硬质微囊通过提供类似细胞外基质的硬度,增强了MSCs的粘附能力,有助于它们在体内的稳定和功能执行。
4、调节细胞微环境:微囊的物理特性,如孔隙率和硬度,可以影响营养物质和信号分子的扩散。这为MSCs提供了适宜的生长条件,有助于调节细胞微环境,促进其功能发挥。
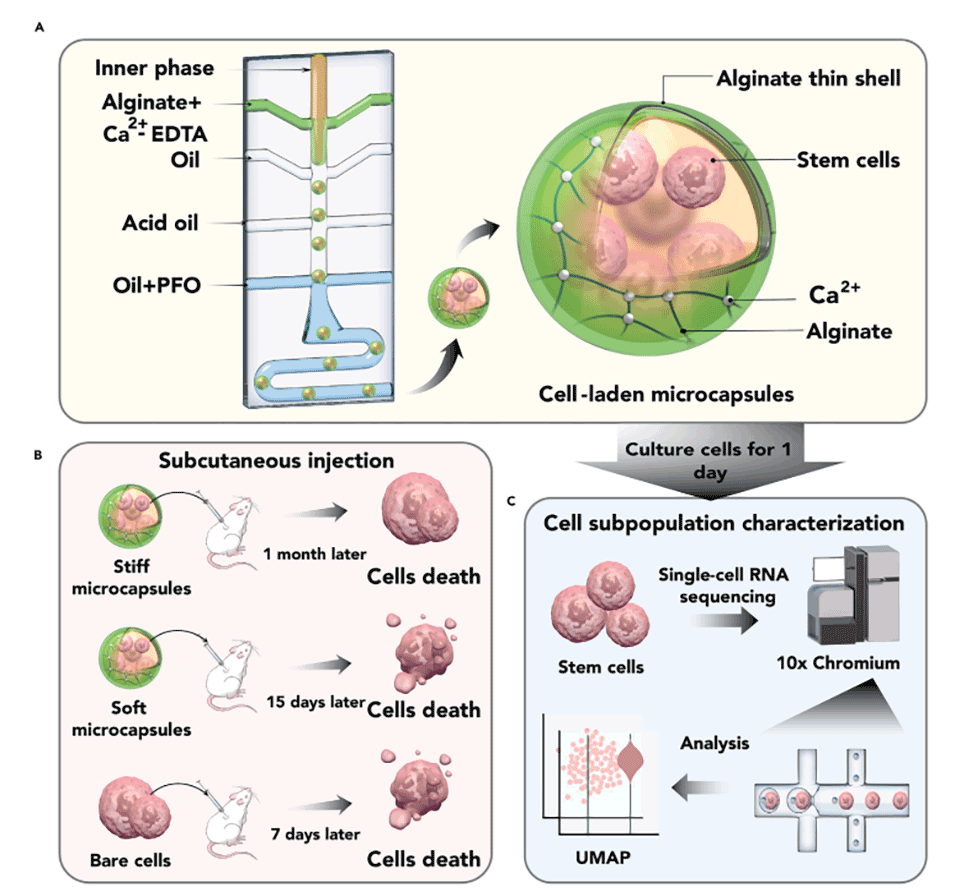
图1.水凝胶封装对再生医学用间充质干细胞亚群的影响
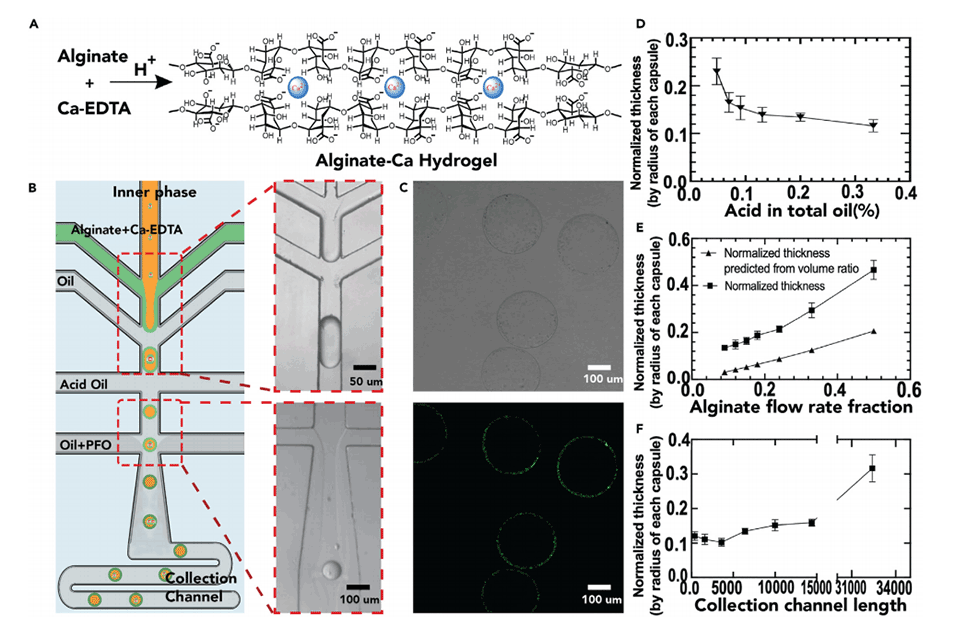
图2.基于液滴微流控方法制备海藻酸盐微胶囊
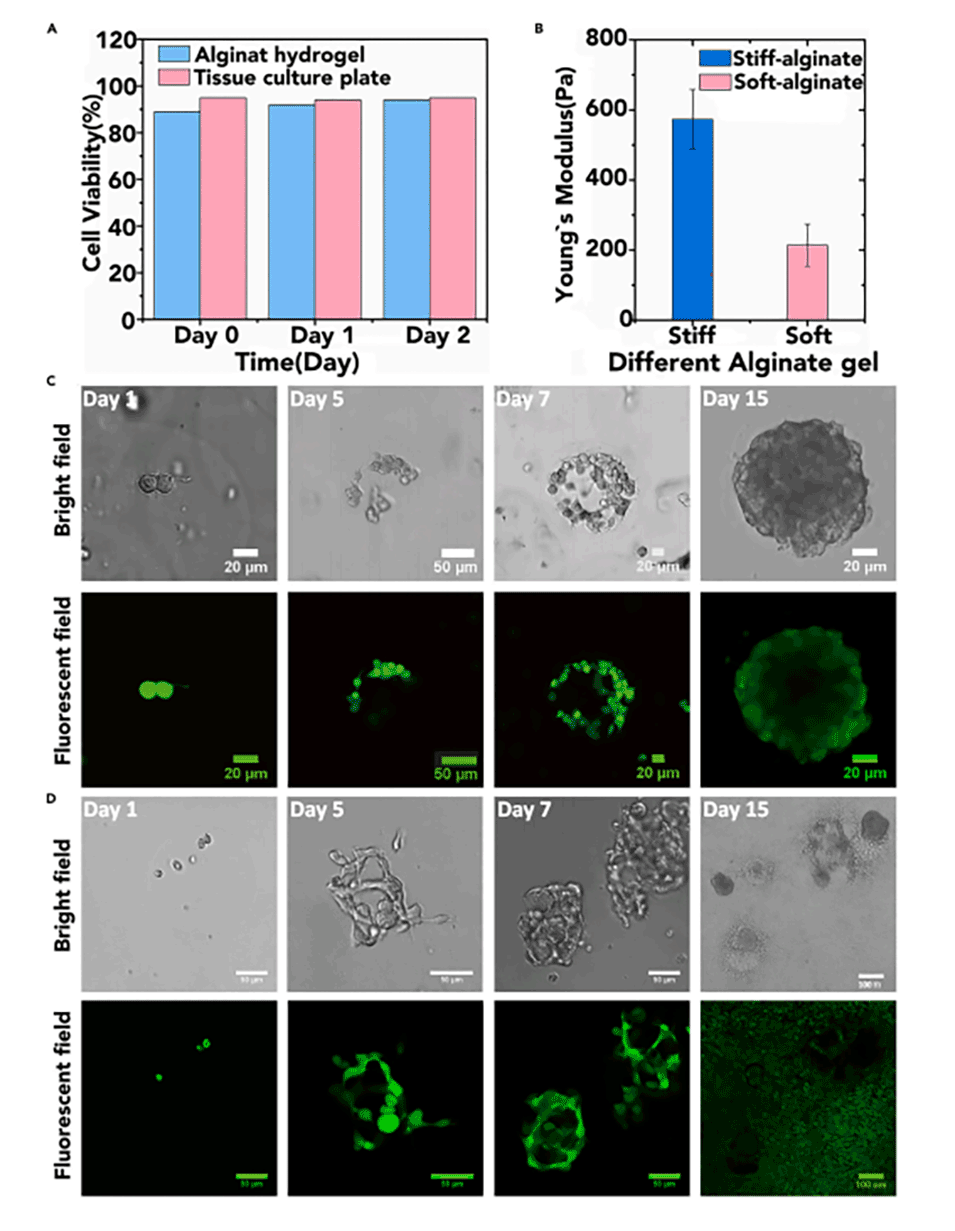
图3.海藻酸盐微胶囊的机械性能对体外干细胞行为的影响
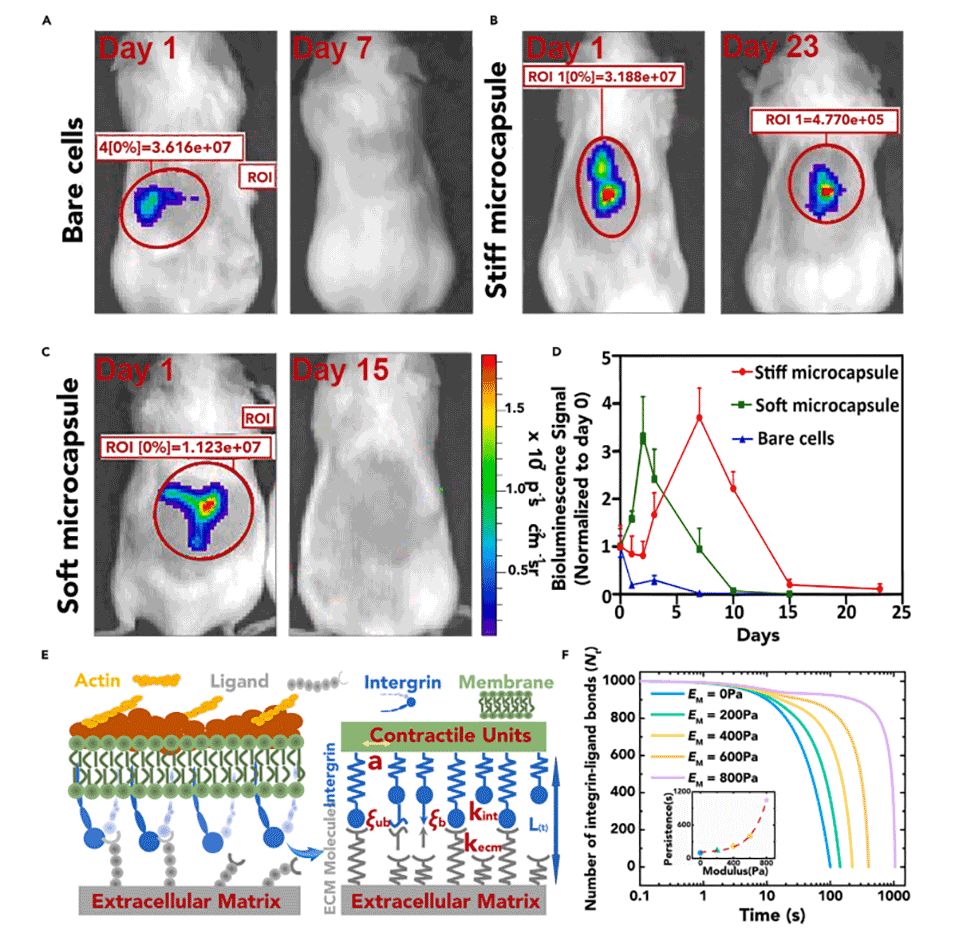
图4.微胶囊延长干细胞在体内的停留时间
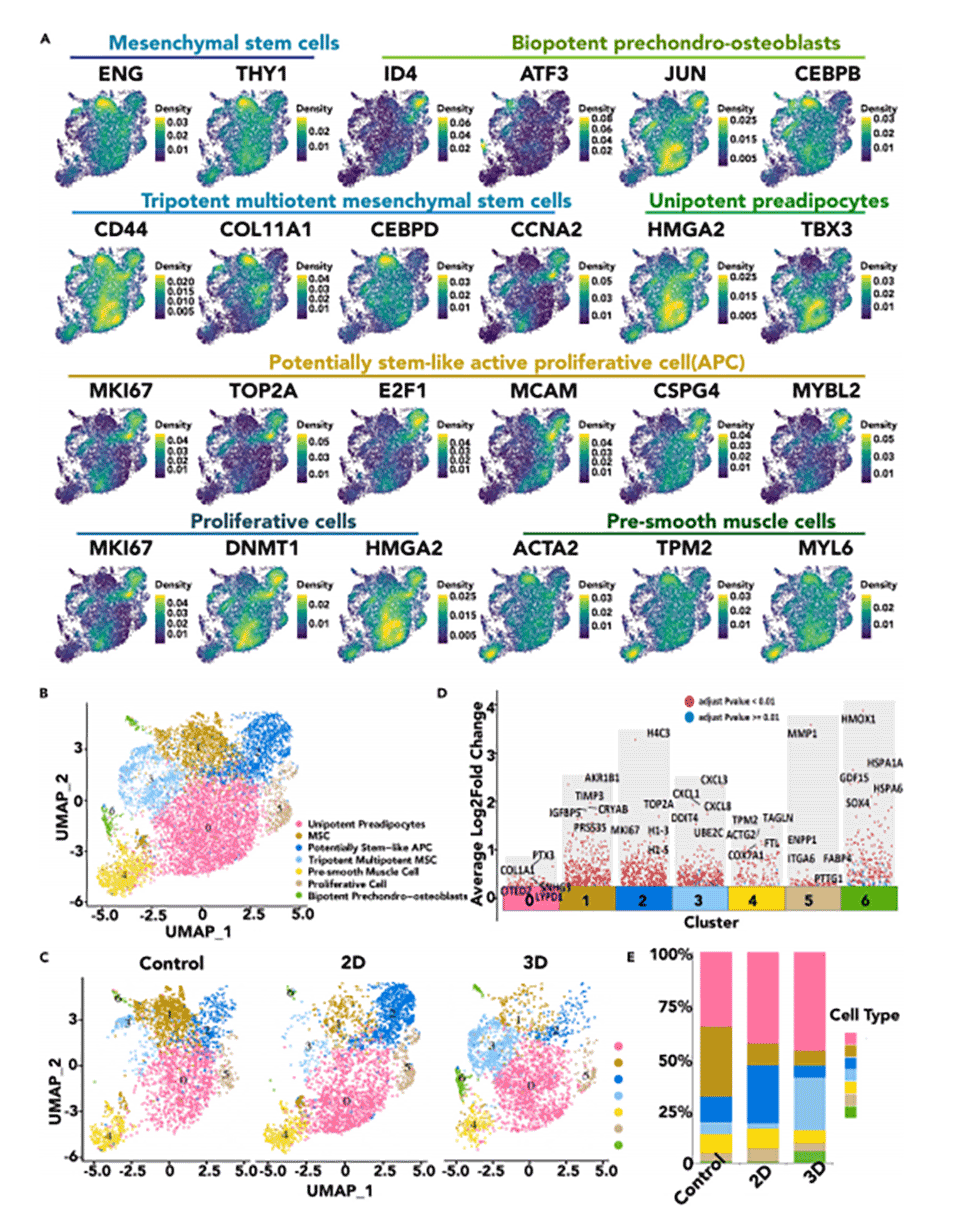
图5.水凝胶封装对hMSCs的影响
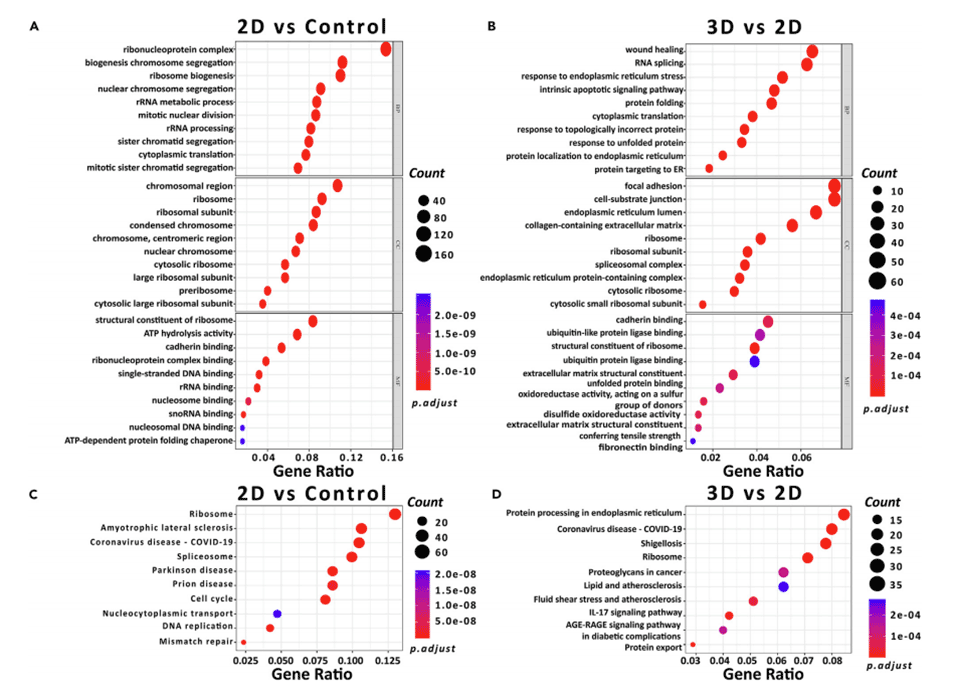
图6.hMSCs的GO和KEGG富集分析
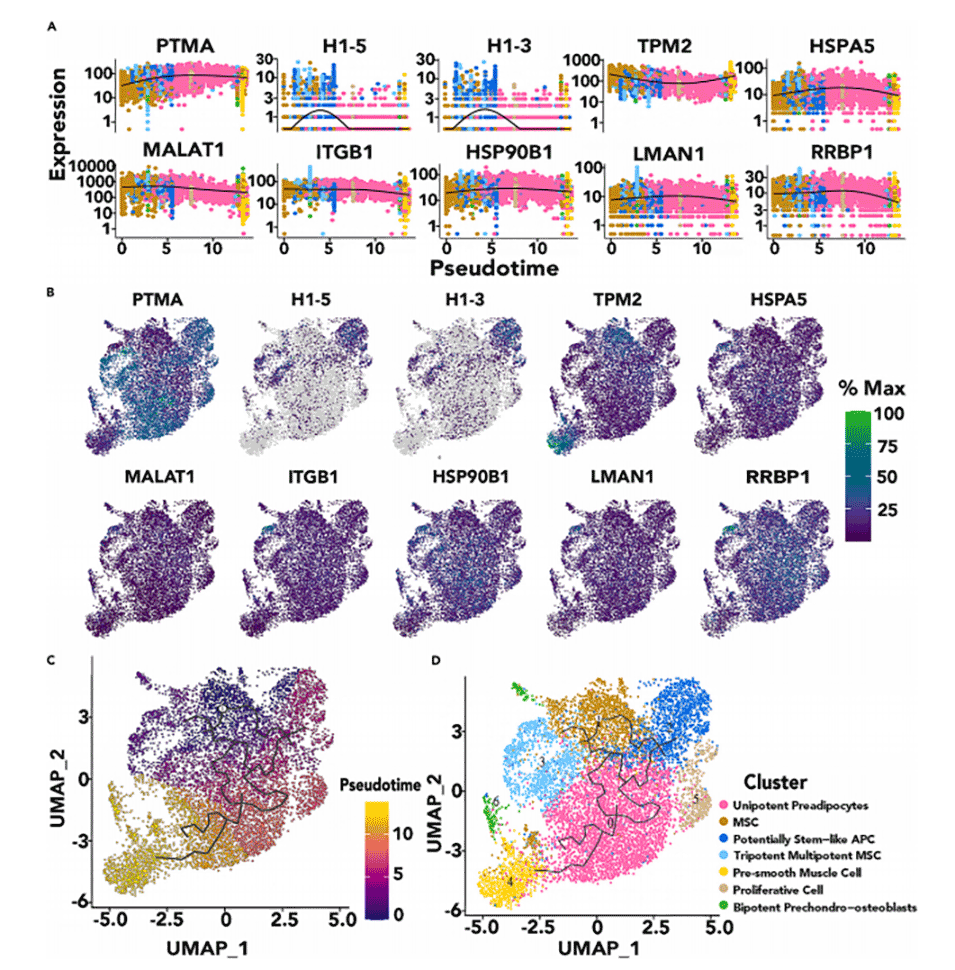
图7.hMSCs中前10个基因的单细胞轨迹
原文链接:https://doi.org/10.1016/j.matt.2024.05.041














