纳米载体对于靶向和增强药物递送至关重要。然而,使用有毒溶剂和复杂的化学功能化过程严重限制了其临床应用。当前的药物载体主要依赖于共沉淀法,常常需要使用有毒溶剂,这不仅增加了制备过程的复杂性,还影响了最终产品的安全性。因此,迫切需要开发一种绿色、简便的方法,以制备具有可调表面功能的纳米载体,从而提高药物递送的效率和安全性。核-壳结构的纳米胶囊因其独特的层次结构,能够有效解决药物溶解性问题,并在控制药物释放、提高细胞摄取和减少副作用方面表现出色。因此,探索一种单步制备具有可调表面功能的生物相容性核壳纳米胶囊的策略显得尤为重要。

近期,浙江大学陈东研究员、梁廷波教授团队提出了一种通过微流控技术单步制备具有可调表面功能的生物相容性核壳纳米胶囊的方法,以提高药物递送的效率和靶向性。相关研究以“Self‐Assembly of Biocompatible Core‐Shell Nanocapsules with Tunable Surface Functionality by Microfluidics for Enhanced Drug Delivery”为题目,发表在期刊《Advanced Functional Materials》上。
本文要点:
1、本研究开发了一种一步策略,利用微流控技术指导具有可调表面功能的生物相容性核壳纳米胶囊的自组装,以提高药物递送的效率和靶向性。
2、该方法避免了使用有毒溶剂和复杂的化学功能化,在微流控设备中,通过快速混合乙醇和水并进行溶剂交换,实现了药物、油、聚合物以及聚合物-聚乙二醇(PEG)功能基团的共沉淀,随后自组装成具有所需表面功能的核壳纳米胶囊。
3、制备的PCL-PEG-FA核壳纳米胶囊展现出高包封效率和载药能力,并通过纳米胶囊表面的官能团与肿瘤细胞膜上的相应受体结合,在体外和体内表现出优异的肿瘤靶向药物递送性能。
4、通过流式细胞术和多重免疫组织化学染色详细研究了肿瘤微环境中的免疫激活,揭示了增强抗肿瘤性能的潜在机制。
5、该策略绿色、简便、通用、可扩展,为设计具有分层结构和期望功能的先进纳米载体提供了一个有前景的平台,以增强药物输送。
使用微流控技术在纳米胶囊制备中的优势:
1、一步合成:微流控技术能够实现药物、油、聚合物和聚合物-PEG功能团的一步共沉淀和自组装,简化了制备过程。
2、精确控制:通过微流控设备的精确流体控制,可以精确调节纳米胶囊的大小和壳层厚度。
3、绿色化学:避免了使用有毒溶剂,整个制备过程更加环保和安全。
4、高效率:微流控技术可以实现快速混合和溶剂交换,提高了纳米胶囊的制备效率。
5、可扩展性:该技术具有很好的放大潜力,适合大规模生产。
核壳纳米胶囊如何改善药物的溶解性和生物利用度?
1、油核增溶:油核可以显著增加药物在乙醇中的溶解度,提高药物的负载能力。
2、控释机制:聚合物壳层可以控制药物的释放,延长药物在体内的循环时间。
3、表面功能化:通过在纳米胶囊表面引入聚乙二醇和叶酸等功能团,可以提高纳米胶囊的稳定性和靶向性,从而提高生物利用度。
4、减少副作用:核壳结构有助于减少药物的副作用,提高药物的疗效。
评估纳米胶囊抗肿瘤性能使用的方法:
1、体外细胞实验:通过细胞培养和细胞活性测试,评估纳米胶囊对肿瘤细胞的抑制效果。
2、体内动物模型:使用肿瘤动物模型,通过静脉注射纳米胶囊,观察其在体内的肿瘤靶向能力和抗肿瘤效果。
3、荧光成像:利用荧光标记的纳米胶囊进行体内成像,以评估其在肿瘤部位的积累情况。
4、免疫组化分析:通过流式细胞术和多重免疫组化染色,评估纳米胶囊对肿瘤微环境中免疫细胞的影响,如CD8+ T细胞、树突细胞等的变化。
5、组织病理学评估:通过组织切片和染色,观察纳米胶囊治疗后肿瘤组织的病理变化,评估治疗效果。
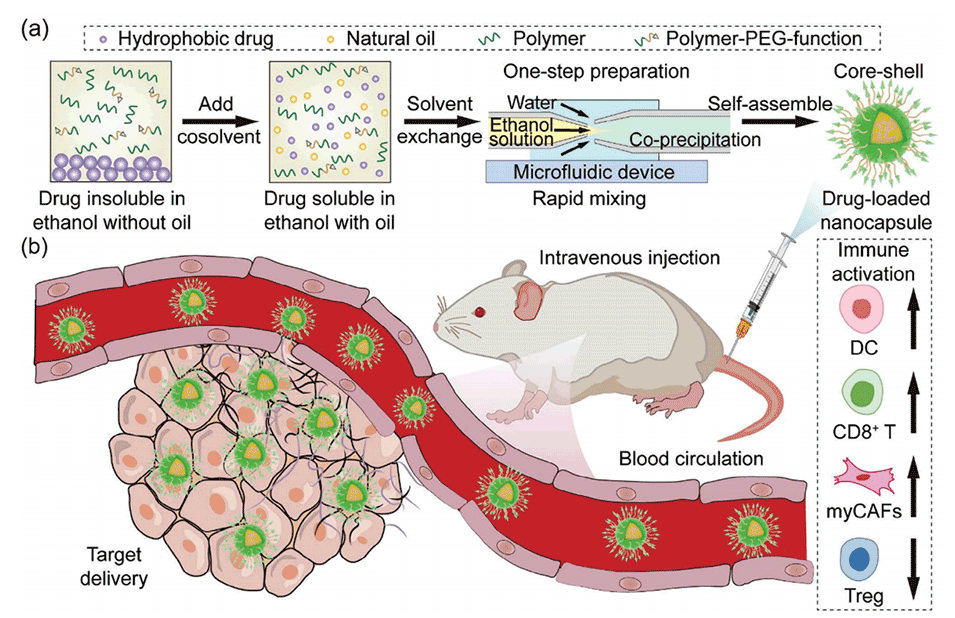
图1.微流控一步制备具有可调表面功能的生物相容性核壳纳米胶囊,以增强药物递送。
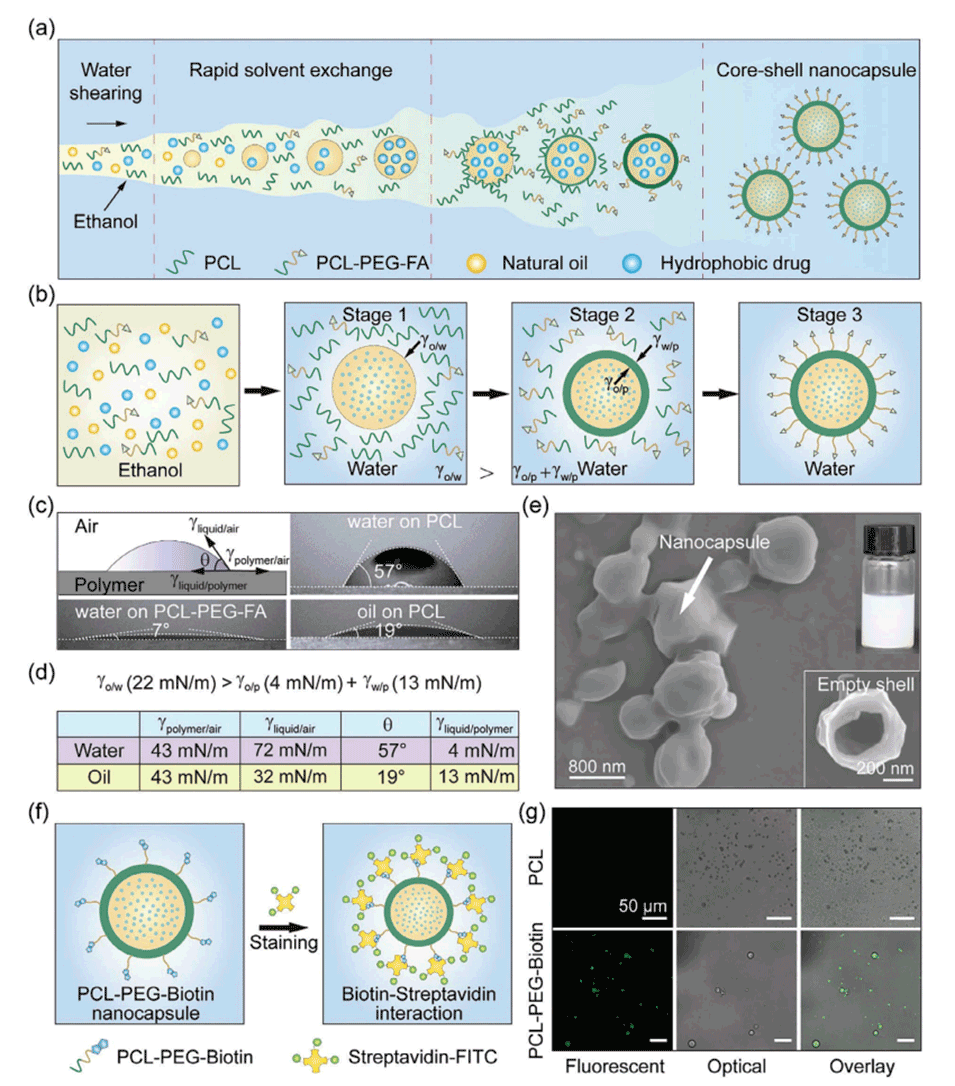
图2.在微流体通道中快速混合后,自组装形成具有可调表面功能的生物相容性核壳纳米胶囊。
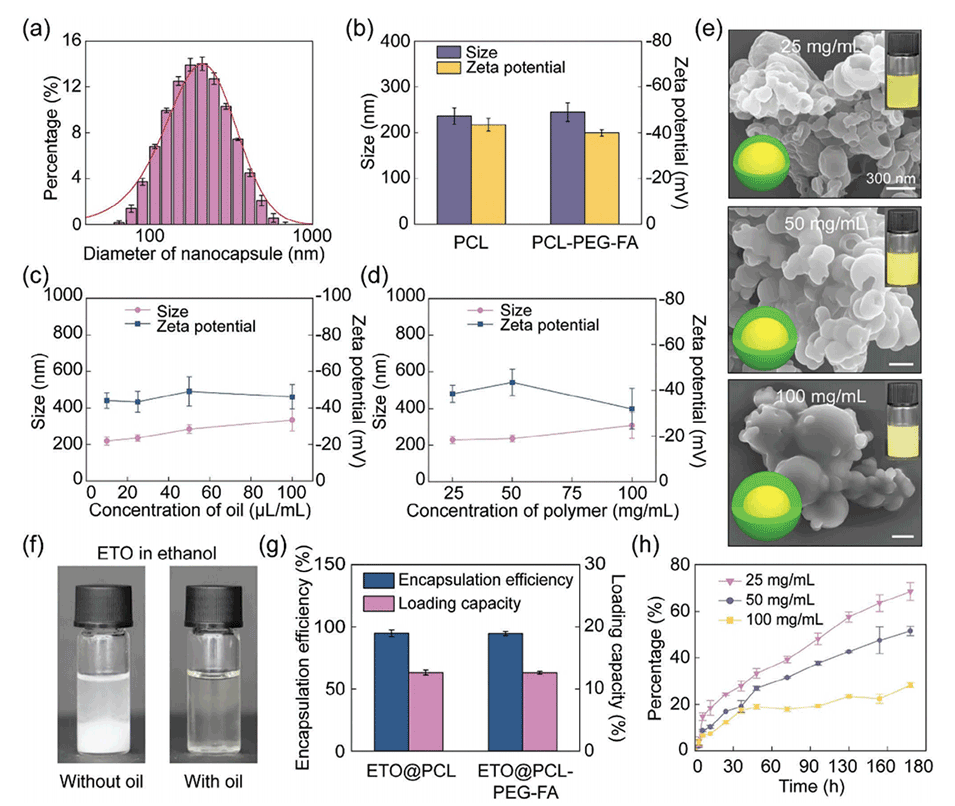
图3.具有可调壳厚和可控释放特性的核壳纳米胶囊的表征。
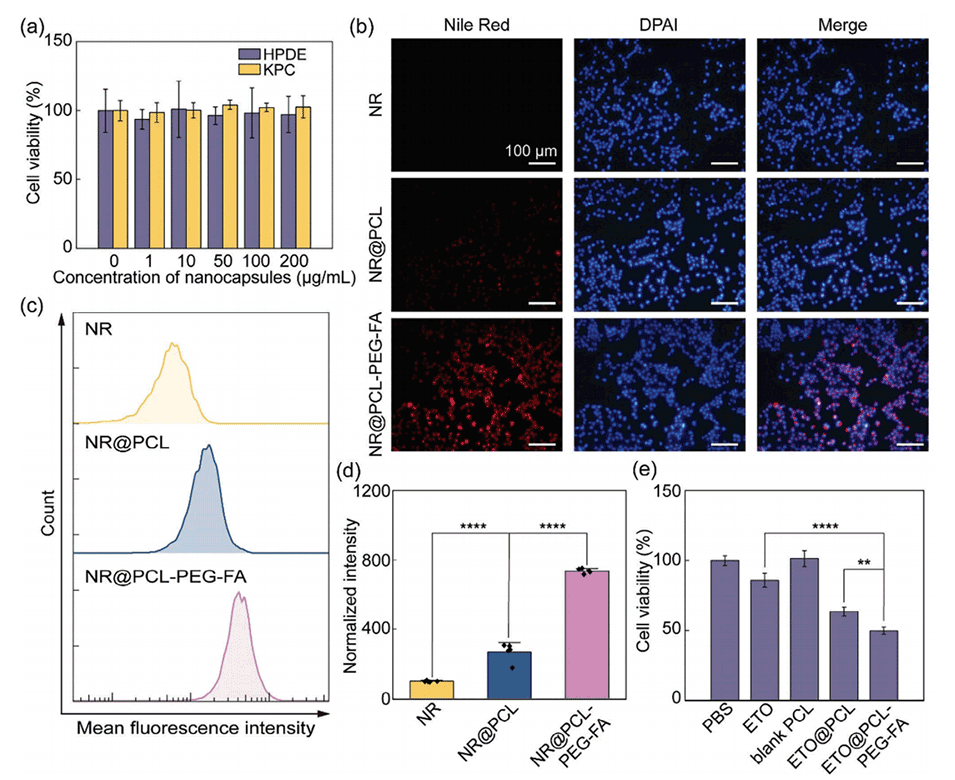
图4.核壳纳米胶囊的体外生物相容性和生物利用度。
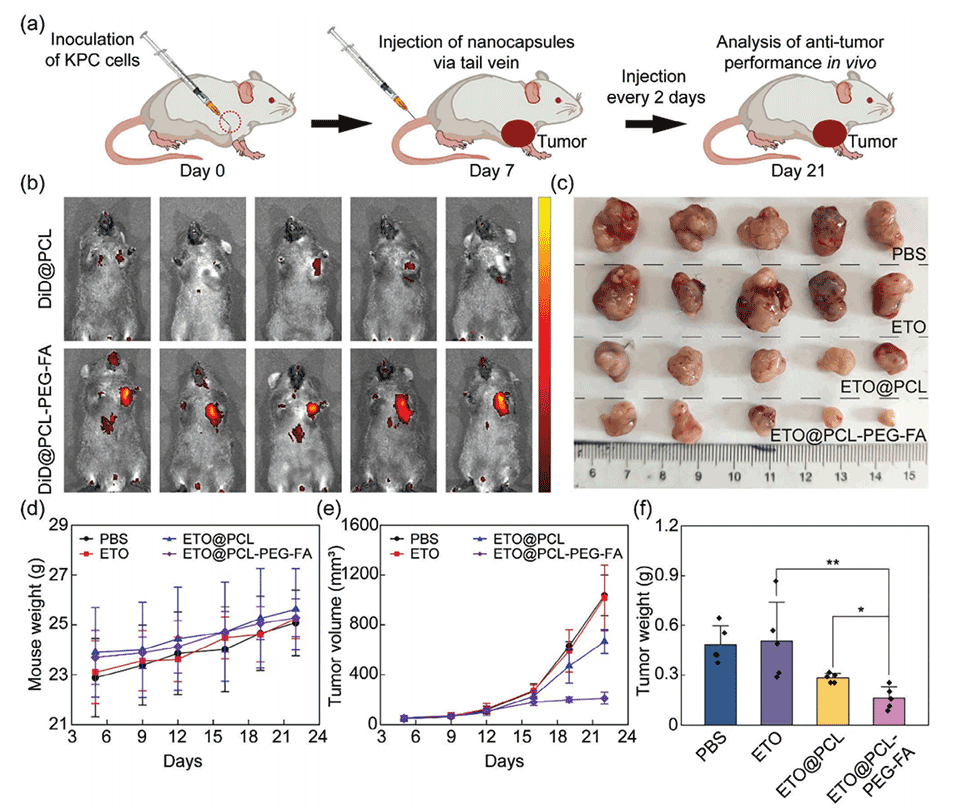
图5.载药纳米胶囊的体内抗肿瘤性能。
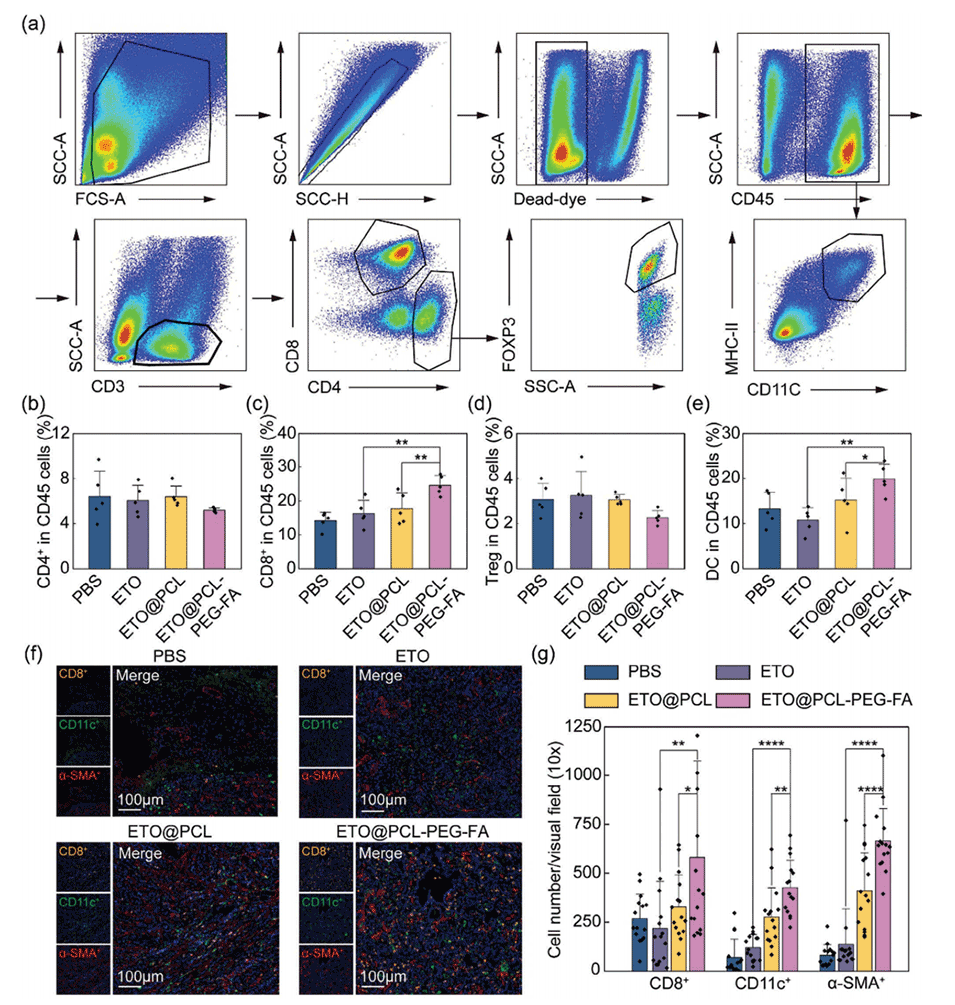
图6.用载药纳米胶囊治疗的小鼠的免疫激活。
原文链接:https://doi.org/10.1002/adfm.202407112














