背景:
随着生物医学材料的发展,微/纳米药物递送系统因其理想的控释能力受到广泛关注。然而,传统制备微球的方法(如乳化法)存在粒径分布宽、纯度低、制备复杂等问题。相比之下,微流控芯片技术具有高可控性、操作简便、试剂用量少、颗粒尺寸均匀等优势,可用于制备具有复杂结构的功能性微球。
海藻酸钠(SA)具有良好的生物相容性和可生物降解性,已被广泛用于药物递送和伤口修复,但由于缺乏抗菌活性,限制了其在感染性创面修复中的应用。银纳米颗粒(AgNPs)具有广谱抗菌活性,但其与SA液体混合易形成不溶性絮状物,难以通过微流控芯片制备微球。

导读:
近期,中国人民解放军总医院温宁教授、徐娟副教授、Jinglong Liu等人与北大口腔医院周维和内蒙古医科大学钱智勇团队合作,通过引入丝素蛋白(SF)包覆AgNPs,开发了一种基于微流控芯片的抗菌复合微球(SA-SF-Ag),用于感染性创面修复。相关研究以“Biocompatible sodium alginate–silk fibroin antibacterial microspheres from a microfluidic platform for infected wound repair”为题目,发表在期刊《Journal of Bioactive and Compatible Polymers》上。
本文要点:
1、本研究利用微流控芯片技术制备了一种具有抗菌性能的生物相容性微球,用于感染性创面修复。
2、采用丝素蛋白(SF)对银纳米颗粒(AgNPs)进行包覆,形成稳定的SF-Ag复合物,再与海藻酸钠(SA)混合,成功制备出具有抗菌特性的SA-SF-Ag微球。
3、该微球克服了AgNPs与SA液体混合物不稳定的问题,可以有效抑制多种细菌和真菌的生长,并缓慢释放AgNPs。
4、体内结果表明,SA-SF-Ag通过杀死小鼠模型感染皮肤伤口表面的铜绿假单胞菌,促进感染伤口愈合和血管生成。
5、总体而言,本研究开发了一种将AgNPs整合到有机聚合物微球中的新方法,为感染性创面修复提供了新的治疗选择。
使用微流控芯片技术制备微球的优势包括:
1、可控性:微流控技术能够在微观尺度上精确控制流体的流动和混合,从而实现对微球尺寸、形态及结构的精确调节。
2、高可靠性:与传统方法相比,微流控芯片提供了更高的可重复性和一致性,减少了制备过程中的变异。
3、低试剂消耗:微流控系统使用的试剂量较少,降低了材料成本和环境影响。
4、操作简便:相比传统的乳化法,微流控技术的操作相对简单,易于实现自动化和标准化。
5、粒径均匀性:通过微流控技术制备的微球通常具有更均匀的粒径分布,这对于药物释放和生物相容性至关重要。
6、复杂结构的形成:微流控技术能够制造具有复杂结构的功能性颗粒,适用于多种生物医学应用。
综上所述,微流控芯片技术在制备微球载体方面具有显著的优势,能够提高药物递送系统的性能和效果。
本研究对现有感染性伤口治疗方法有哪些改进?
1、减少抗生素使用:通过使用具有广谱抗菌活性的AgNPs,减少了对传统抗生素的依赖,有助于减缓耐药性的发展。
2、提高治疗效果:SA-SF-Ag微球的持续释放和促进血管生成的特性,有望增强感染性伤口的治疗效果。
3、减少副作用:通过形成蛋白冠层减少AgNPs的毒性,降低了治疗过程中的副作用。
SA-SF-Ag微球的制备和应用中存在哪些技术挑战?
1、材料稳定性:AgNPs与SA混合时容易生成不溶性絮状物,需通过SF包覆技术解决这一问题,但包覆过程的稳定性和效率仍需优化。
2、释放控制:如何进一步优化AgNPs的释放速率,使其在抗菌效果和生物安全性之间达到平衡,是一个重要挑战。
3、规模化生产:微流控芯片技术虽然具有高精度,但在大规模生产中可能面临效率和成本的限制,需要进一步改进工艺。
4、个体化适配:不同患者的感染类型和伤口特性可能不同,如何根据具体需求调整微球的成分和功能仍需深入研究。
5、长期安全性:AgNPs的长期使用可能存在潜在的毒性风险,需要进一步研究其在体内的代谢和排泄机制。
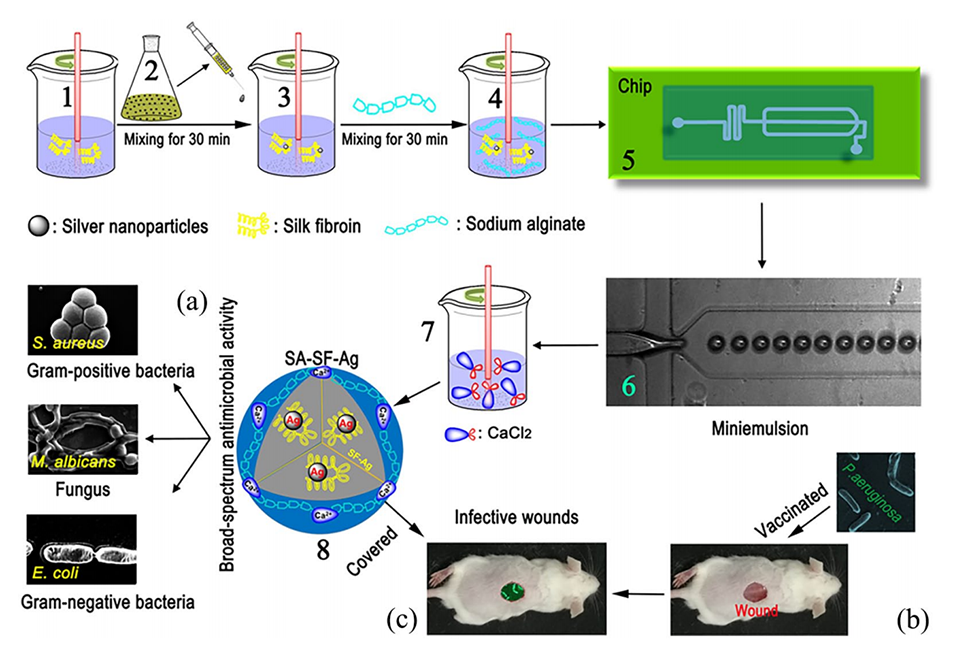
Scheme1.使用微流控芯片技术合成SA-SF-Ag的示意图(1-8)。(a)SA-SF-Ag的广谱抗菌活性。(b)感染小鼠皮肤伤口模型。(c)SA-SF-Ag对感染伤口的治疗效果。
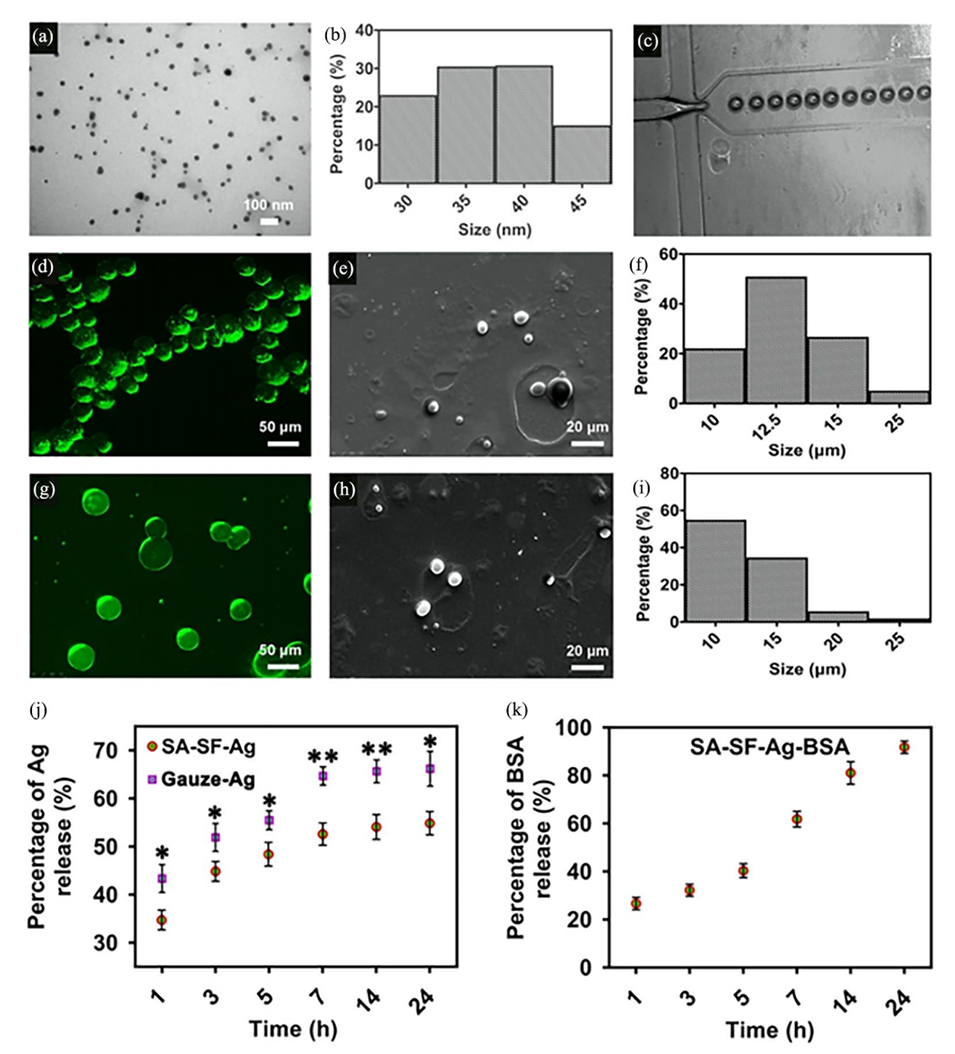
图1.AgNPs、SA-SF微滴和SA-SF-Ag微球的表征。

图2.(a–d)对大肠杆菌(a)、金黄色葡萄球菌(b)、铜绿假单胞菌(c)和白色念珠菌(d)的抗菌活性。(e–h)大肠杆菌(e)、金黄色葡萄球菌(f)、铜绿假单胞菌(g)和白色念珠菌(h)的扫描电镜图像。(e1–h1)用纱布-NS(1)、纱布-Ag(2)、纱布-SA-SF(3)和纱布-SA-SF-Ag(4)处理后的大肠杆菌(e1)、金黄色葡萄球菌(f1)、铜绿假单胞菌(g1)和白色念珠菌(h1)的SEM图像。
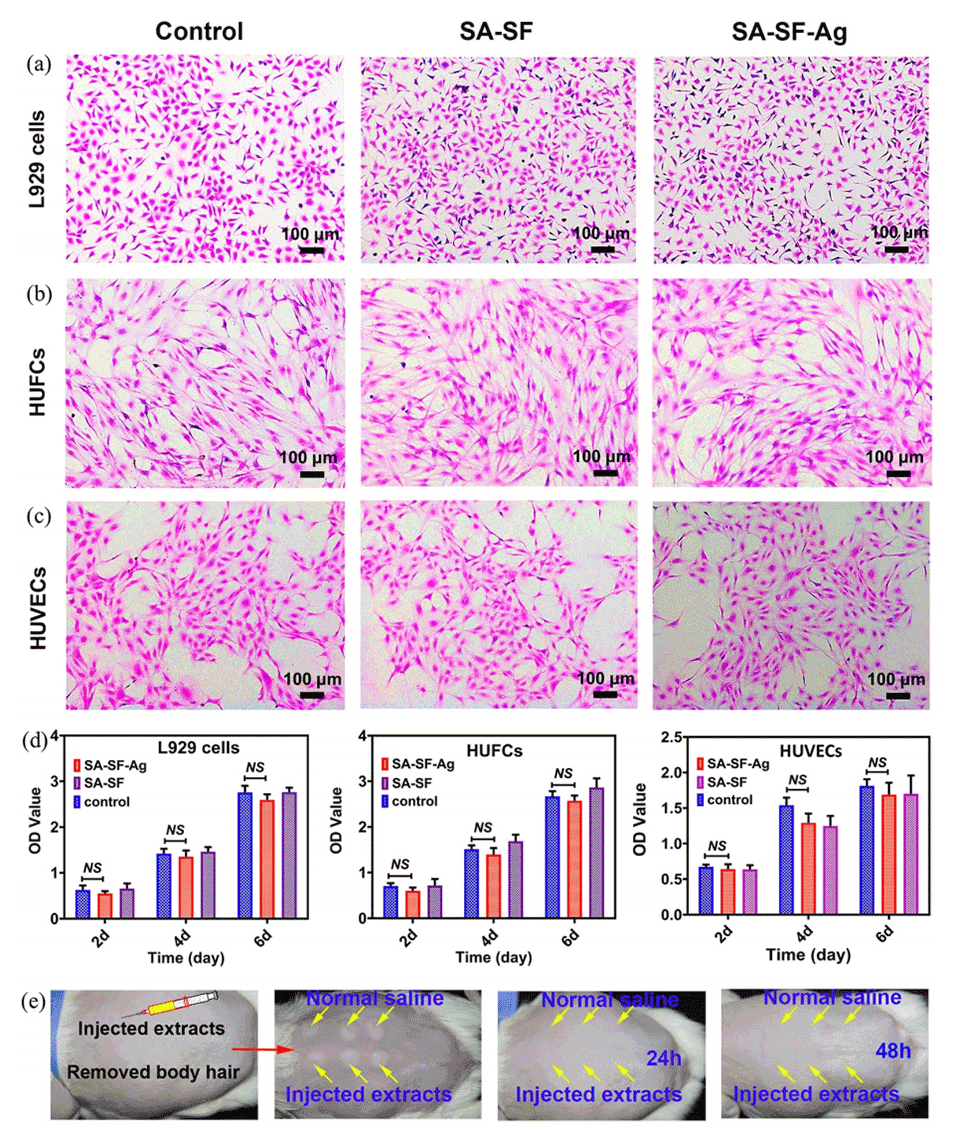
图3.豚鼠细胞相容性和皮下致敏性评估。
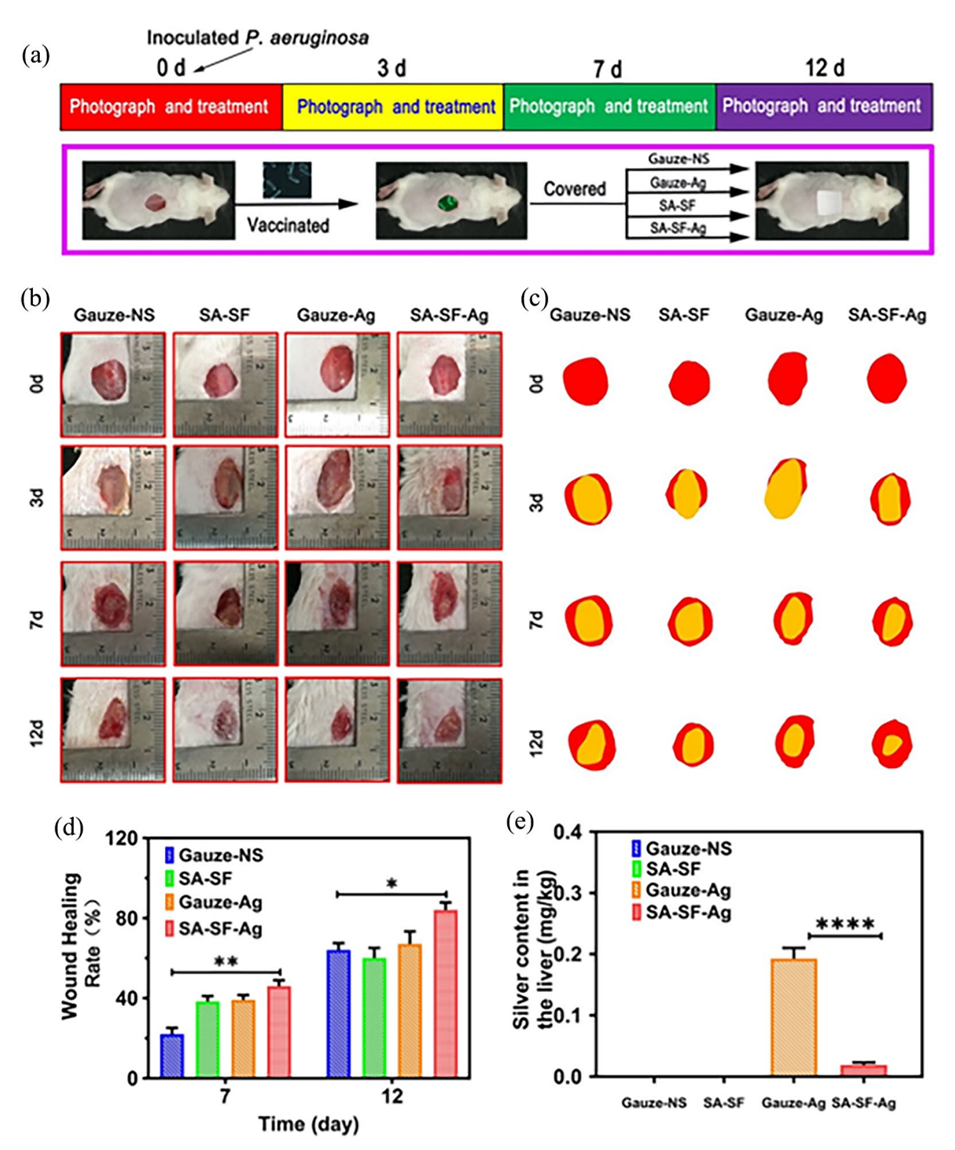
图4.感染性全层皮肤损伤的愈合。
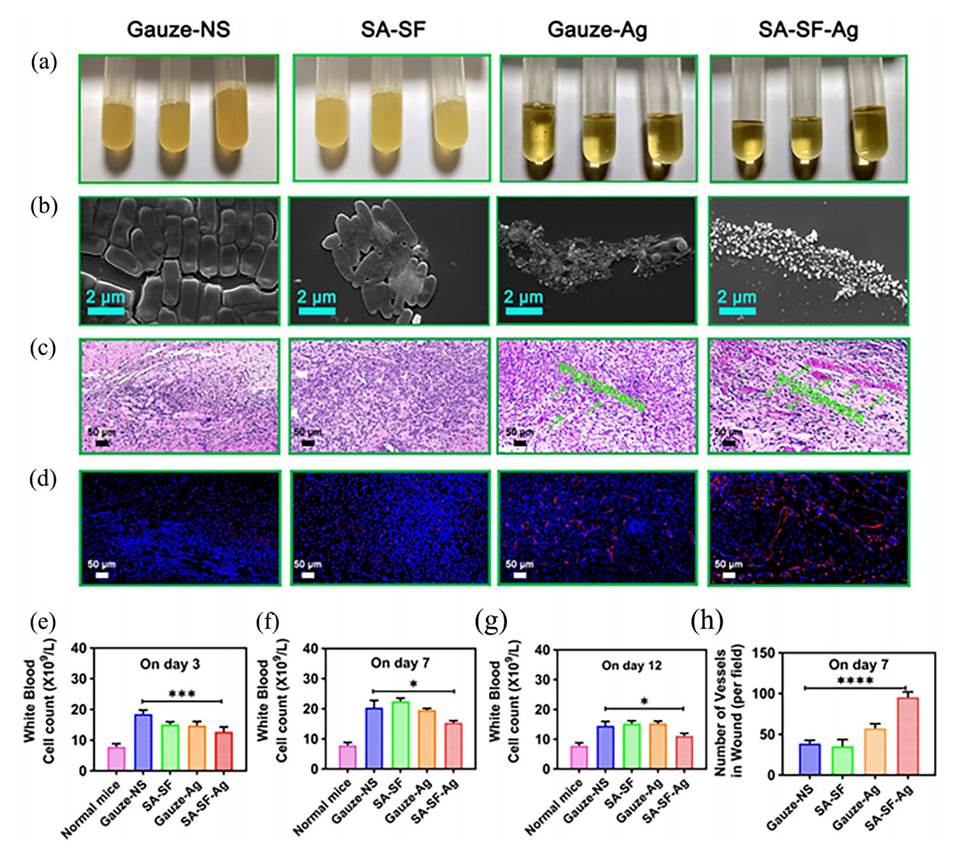
图5.铜绿假单胞菌感染小鼠皮肤创面缺损模型的病理分析。
论文链接:
https://doi.org/10.1177/08839115241241294














