
导读:
与传统的单乳液相比,双乳液(W1/O/W2)的三相双界面结构可同时包载亲水性和疏水性物质,应用潜力显著。近期,中国农业大学食品科学与营养工程学院宋弋副教授、马涛等人通过构建CNC/β-LG复合物与PGPR协同稳定的双乳液体系,系统揭示了界面相互作用机制及其在亲疏水性营养素共递送中的应用潜力。相关研究以“Fabrication of nanocrystal/β-lactoglobulin complexes stabilized W1/O/W2 emulsions: Structure, stabilization mechanism and application for co-encapsulation of curcumin and EGCG”为题目,发表在期刊《Food Hydrocolloids》上。研究不仅阐明了氢键与静电作用对双界面稳定性的关键调控机制,还通过体外消化模拟证实该体系可精准控制姜黄素与EGCG的靶向释放,为功能性食品载体的设计提供了理论依据。
本文要点:
1、本研究以聚甘油聚蓖麻油酸酯(PGPR)为疏水乳化剂,纤维素纳米晶体(CNC)/β-乳球蛋白(β-LG)复合物为亲水乳化剂,通过两步法制备W1/O/W2乳液。
2、结果表明,PGPR浓度(7.0 wt%)和油水比(8:2)可优化初级W1/O乳液的稳定性,而W1/O与W2质量比(3:7)显著提升双乳液稳定性。
3、激光共聚焦显示CNC/β-LG复合物在O/W2界面形成致密吸附层,未吸附颗粒在连续相中形成桥联网络,增强乳液黏度。
4、界面相互作用分析表明,PGPR通过疏水作用稳定W1/O界面,而CNC/β-LG复合物依赖氢键和静电作用稳定O/W2界面。
5、以姜黄素和EGCG为模型物质共包载时,包封率分别达95.7%和86.8%。
6、体外模拟消化表明,营养素在整个口服和胃阶段受到保护,到达肠道时发生受控释放,其生物可及性提升至65.1%和71.6%。该研究为开发不同极性营养素共递送体系提供了新思路。
CNC/β-LG复合物与PGPR如何通过不同界面作用机制协同稳定双乳液体系?
1、PGPR的疏水作用主导初级界面(W1/O界面)的稳定性:
PGPR作为疏水乳化剂,通过疏水相互作用吸附于W1/O界面,形成致密的界面膜,有效防止内水相(W1)液滴的聚结。实验表明,当PGPR浓度达到7.0 wt%时,初级乳液液滴尺寸显著减小(从2.7 μm降至1.2 μm),且存储14天后仍保持稳定。
通过SDS(破坏疏水作用)干预实验发现,PGPR的稳定性高度依赖疏水作用,而尿素(破坏氢键)和pH变化对初级界面影响较小,进一步验证了疏水作用的主导性。
2、CNC/β-LG复合物的氢键与静电作用稳定次级界面(O/W2界面):
CNC与β-LG通过pH调控的静电相互作用形成复合物(pH 3.0时,CNC带负电,β-LG带正电),复合物吸附于O/W2界面形成厚界面层(厚度为单一组分的8-14倍),显著降低界面张力。
尿素干预实验显示,次级界面稳定性依赖氢键;pH 7.0时,两者均带负电引发静电排斥,导致界面层崩解。CLSM观察表明,未吸附的复合物在连续相中形成桥联网络,提升体系黏度,抑制液滴迁移。
该双乳液体系在功能性食品开发中有哪些潜在优势?其控释机制如何实现?
1、潜在优势
共包载能力:三相双界面结构可同时封装亲水性(如EGCG,包封率86.8%)和疏水性(如姜黄素,包封率95.7%)活性成分,突破传统单乳液的极性限制。
低脂健康属性:以水相替代部分油脂,适用于低脂食品开发(如文献中O:W1比例优化为8:2)。
稳定性与生物可及性提升:CNC/β-LG复合物增强界面保护,体外消化中姜黄素和EGCG的生物可及性分别提升至65.1%和71.6%(游离形式仅1-10%)。
2、控释机制
胃部保护:酸性环境(pH 2.0)下,CNC(负电)与β-LG(正电)静电作用维持次级界面完整性,减少胃蛋白酶对活性物质的降解(EGCG胃释放率仅17.5%)。
肠道靶向释放:肠道中性环境(pH 7.0)中,CNC与β-LG均带负电,静电排斥引发次级界面崩解,触发程序性释放。姜黄素因疏水性延迟释放,EGCG因亲水性快速扩散,二者协同增强吸收效率。
黏度调控延缓迁移:连续相中的桥联网络抑制液滴迁移,延长肠道滞留时间,进一步提升生物利用度。
总体而言,该体系为多营养素协同递送(如姜黄素与EGCG的抗炎协同效应)及功能性食品(如益生菌包埋、维生素强化)开发提供了高效载体,兼具稳定性与精准释放特性。
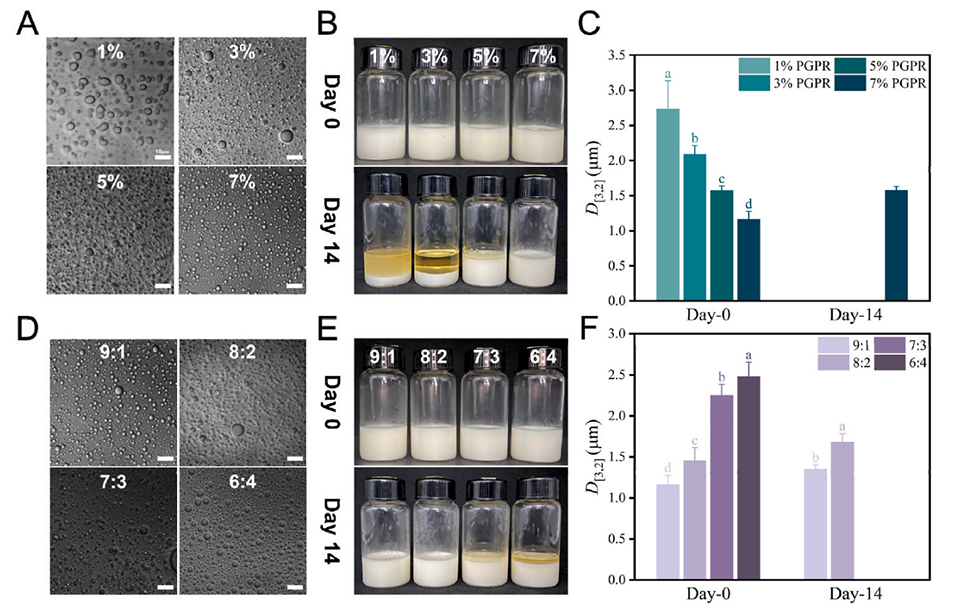
图1.初级W1/O乳液的性质。(A,D)新鲜乳液的微观结构(比例尺:10μm);(B,E)14天前后乳液的视觉照片;(C,F)14天前后乳液的液滴尺寸。
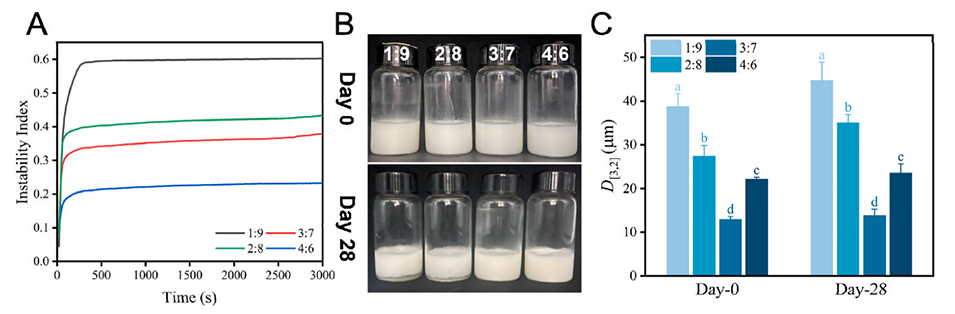
图2.W1/O/W2乳液的性质。(A)新鲜双乳液的物理稳定性;(B)28天前后乳液的视觉照片;(C)28天前后乳液的液滴尺寸。
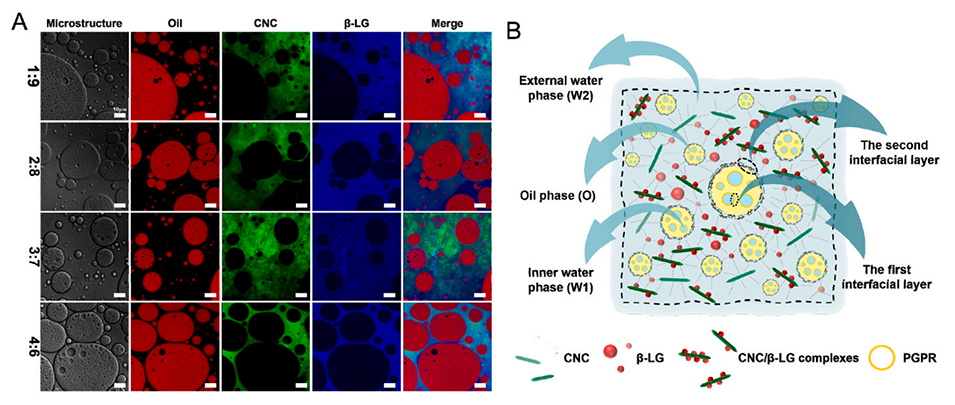
图3.W1/O/W2乳液的CLSM显微照片(β-LG:蓝色通道;CNC:绿色通道;玉米油:红色通道;比例尺:10μm);(B)CNC/β-LG复合物和PGPR稳定W1/O/W2乳液的机制。
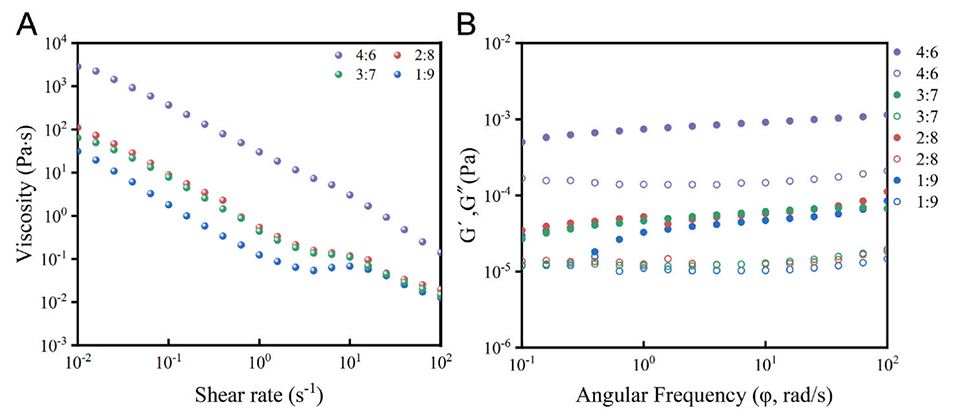
图4.W1/O/W2乳液的流变性能。(A)粘度,(B)模量。G'(填充符号):储能模量,表示弹性(类固体)行为。G''(开放符号):损耗模量,表示粘性(类液体)行为。
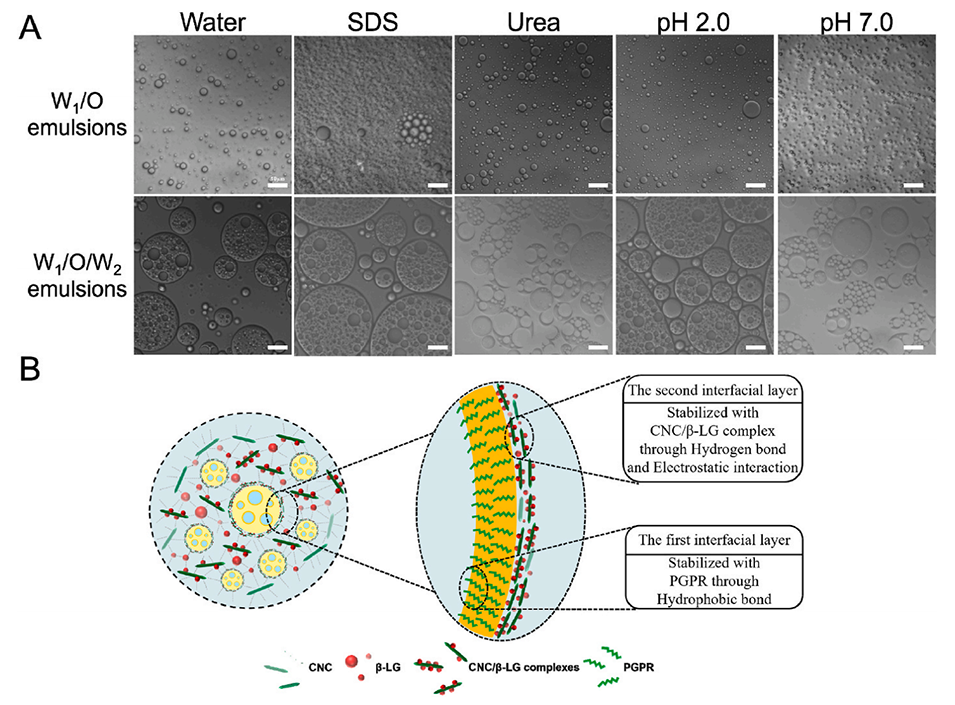
图5.(A)水、尿素、SDS和pH条件对W1/O/W2乳液微观结构的影响;(B)W1/O/W2乳液内界面层相互作用的示意图。
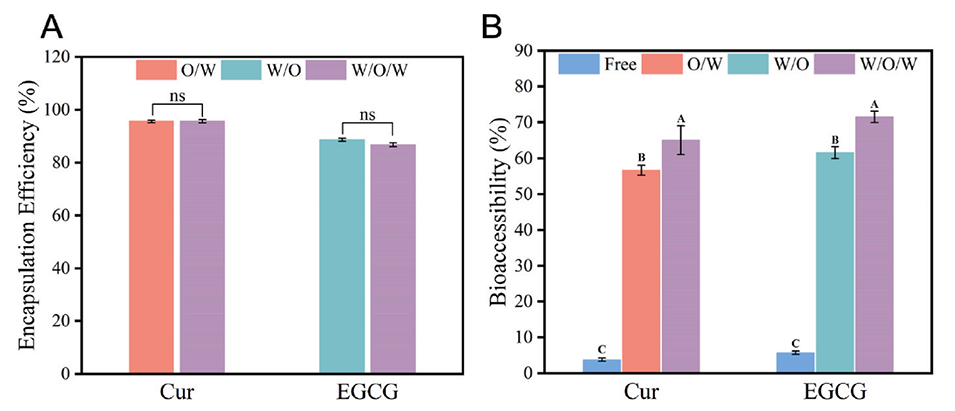
图6.(A)姜黄素和EGCG的包封效率;(B)姜黄素和EGCG的生物可及性。
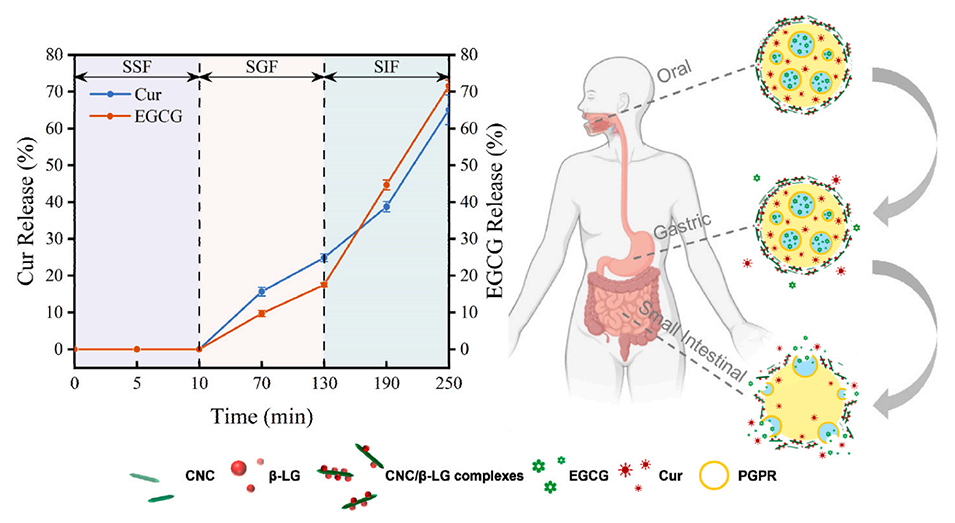
图7.CNC/β-LG复合物和PGPR稳定的W1/O/W2乳液中姜黄素和EGCG的体外释放特性。
论文链接:https://doi.org/10.1016/j.foodhyd.2025.111409














