
导读:
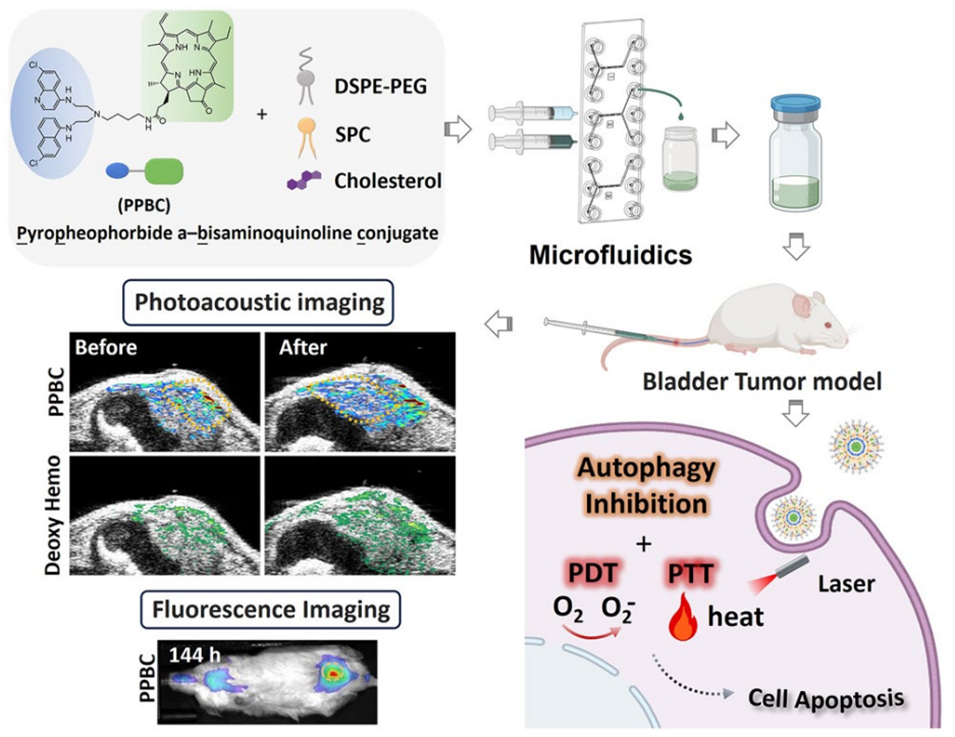
合理设计能够将治疗效果与药物分布和肿瘤状态实时监测相结合的多功能纳米平台正在成为癌症纳米医学中一种有前景的方法。近期,加州大学戴维斯分校生物化学与分子医学系Yuanpei Li教授等人开发了一种多功能纳米平台——焦脱镁叶绿酸a-双氨基喹啉共轭脂质纳米颗粒(PPBC LNPs)。该颗粒通过微流控技术制备,兼具光动力、光热治疗与自噬抑制三重功能,以及光声和荧光双模态成像能力,在膀胱癌模型中实现了高效诊疗并展现出良好临床转化潜力。相关研究以“Multifunctional and Scalable Nanoparticles for Bimodal Image-Guided Phototherapy in Bladder Cancer Treatment”为题目,发表于期刊《Nano-Micro Letters》。
本文要点:
1、本研究开发了一种焦脱镁叶绿酸a-双氨基喹啉共轭脂质纳米颗粒(PPBC LNPs),作为膀胱癌图像引导光疗的双模态系统。
2、该纳米颗粒由脂质赋形剂配制,并使用微流控技术组装而成,具有良好的生物相容性、稳定性和可扩展性。
3、PPBC LNPs在光激活下可同时产生强大的光动力和光热效应,并能有效阻断自噬,诱导膀胱癌细胞死亡。
4、此外,其具备优异的光声(PA)和荧光(FL)成像能力,可实现高分辨率、深组织穿透和高灵敏度的成像,用于追踪药物分布和光疗效果。
5、光声成像证实了纳米颗粒在肿瘤中的高效富集并可预测疗效,而荧光成像显示其在肿瘤部位可滞留长达6天。
6、在膀胱癌模型中,PPBC LNPs联合激光治疗能显著抑制肿瘤生长,部分肿瘤甚至被完全消融,显示出巨大的临床转化潜力。
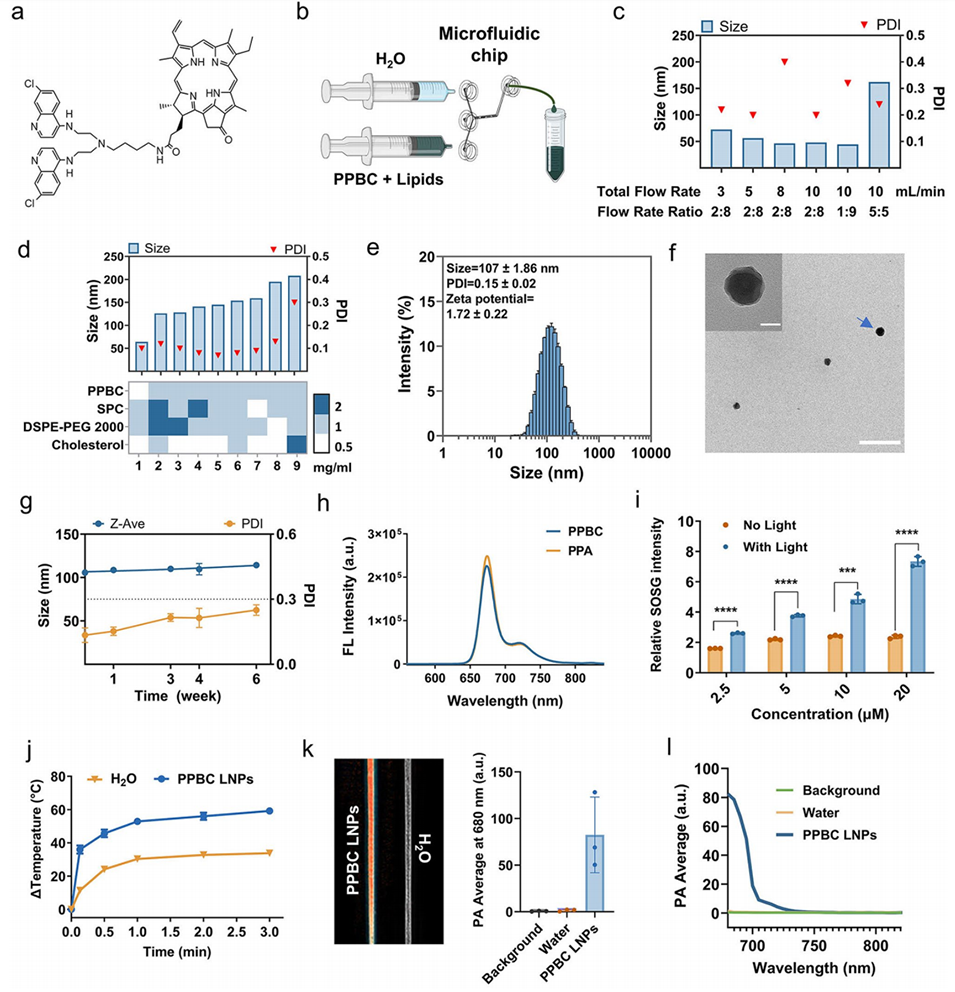
图1: PPBC LNPs的制备与表征。a: PPBC的化学结构式。b: 用于合成PPBC LNPs的微流控系统示意图。c, d: 通过调整总流速、流速比和脂质成分比例来优化纳米颗粒尺寸和PDI。e, f: 复溶后PPBC LNPs的动态光散射粒径分布图和透射电镜图,显示其球形形貌和均匀尺寸。g: 复溶后PPBC LNPs在4°C下的稳定性数据。h: PPBC和PPA的荧光光谱对比。i: 使用SOSG指示剂测量的PPBC LNPs的单线态氧产生能力。j: PPBC LNPs溶液在激光照射下的光热升温曲线。k, l: PPBC LNPs水溶液的光声信号图及其在680-820 nm波长范围内的光谱性PA振幅。
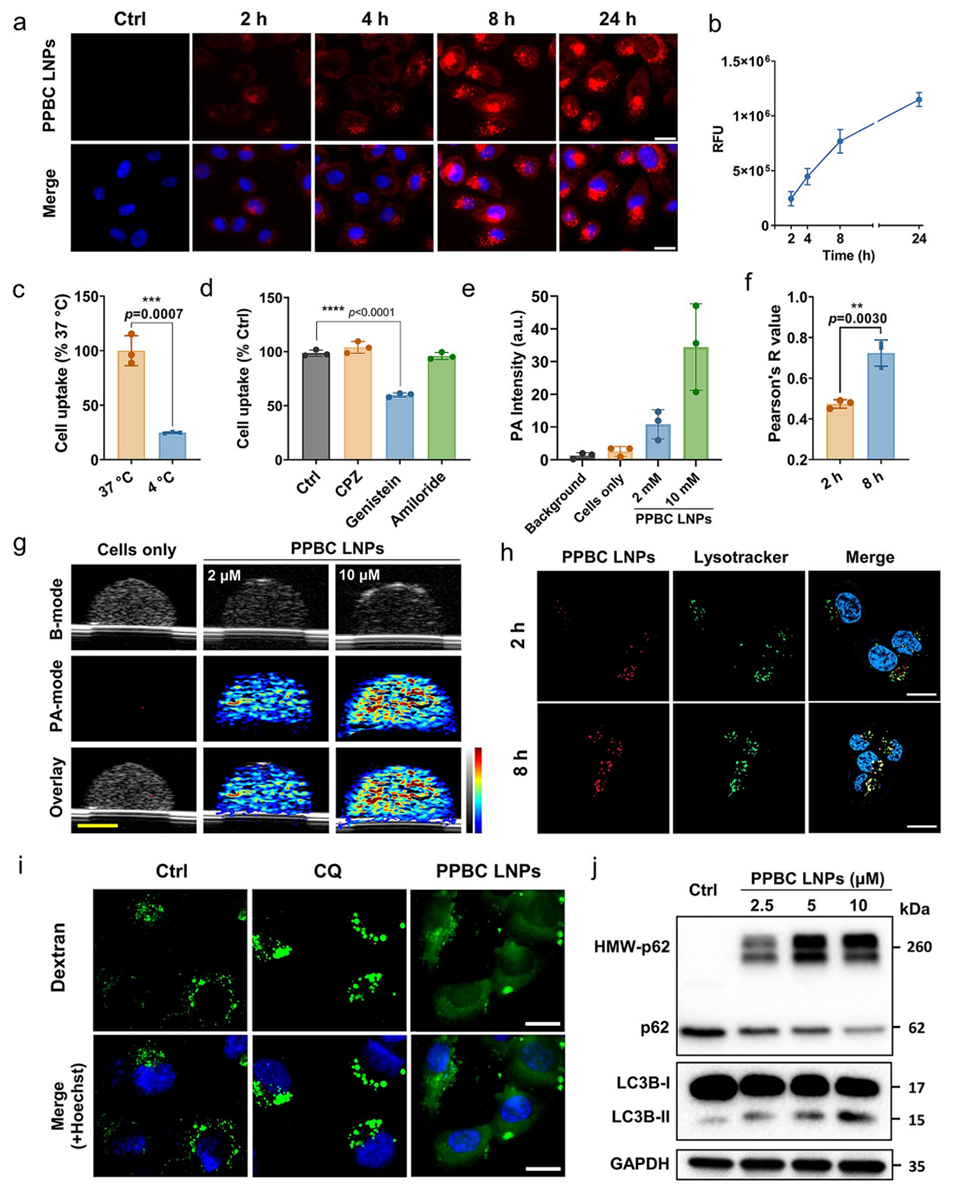
图2: 细胞摄取和抗溶酶体/自噬作用。a, b: T24膀胱癌细胞对PPBC LNPs的时间依赖性摄取荧光图像及定量。c, d: 能量依赖性及不同内吞抑制剂对细胞摄取的影响,证明其主要通过小窝蛋白介导的内吞进入细胞。e, g: 经PPBC LNPs处理的T24细胞在仿体模型中的光声图像及信号定量,显示浓度依赖性PA信号。f, h: PPBC LNPs与溶酶体的共定位分析及皮尔逊相关系数,证明其有效富集于溶酶体。i: 使用Dextran-AF 488评估PPBC LNPs诱导的溶酶体膜透化。j: Western Blot分析显示PPBC LNPs处理后,自噬标志物LC3B-II和高分子量p62的增加,表明自噬被抑制。
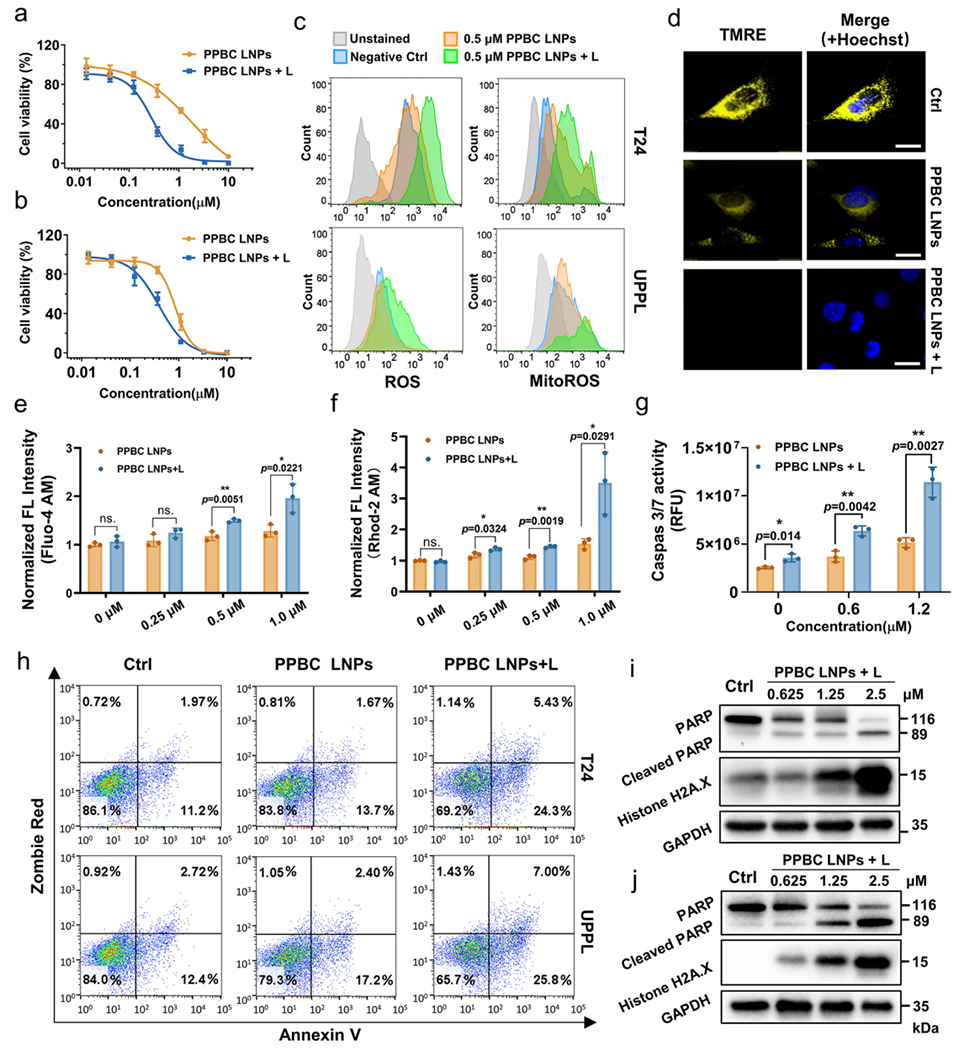
图3: 体外光疗效果评估。a, b: PPBC LNPs在有/无光照下对T24和UPPL膀胱癌细胞的杀伤曲线。c: 流式细胞术分析显示,光照后细胞内活性氧和线粒体活性氧水平显著升高。d: TMRE染色显示,仅PPBC LNPs加光照组线粒体膜电位显著丧失。e, f: 钙离子荧光探针检测显示,光照引发胞内和线粒体内钙离子超载。g: PPBC LNPs介导的光疗显著激活了caspase 3/7。h: Annexin V凋亡检测证实光照诱导了最高水平的细胞凋亡。i, j: Western Blot证实光照后凋亡标志物剪切PARP和DNA损伤标志物H2A.X水平升高。
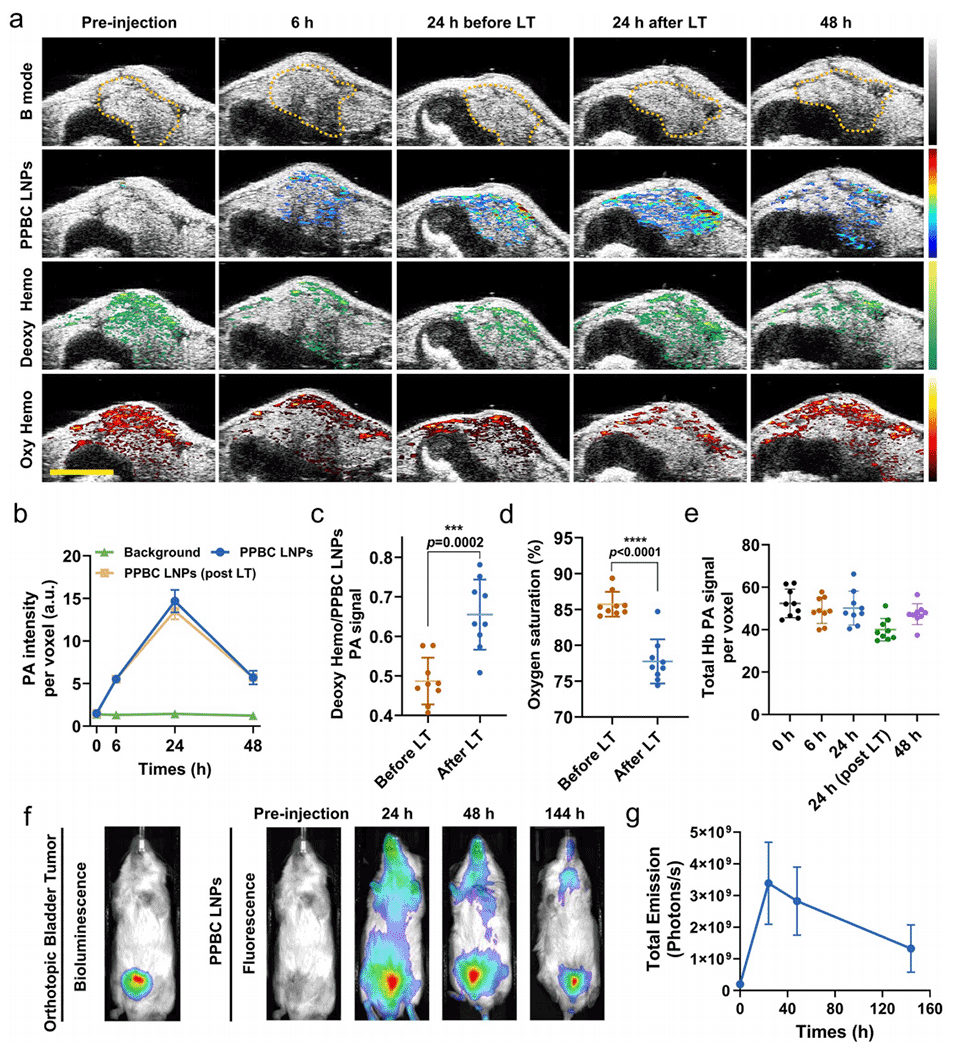
图4: 原位膀胱癌模型中的双模态成像。a: 体内PA成像随时间推移监测PPBC LNPs、脱氧血红蛋白和氧合血红蛋白的信号模式。b: 肿瘤内PPBC LNPs的PA信号定量,显示24小时达到峰值。c, d: 激光治疗前后,肿瘤内脱氧血红蛋白信号和血氧饱和度的定量分析,显示治疗后缺氧加剧。e: 肿瘤内总血红蛋白信号定量,表明其含量基本不变。f, g: 生物发光成像显示肿瘤位置,荧光成像显示PPBC LNPs在体内的分布及在肿瘤部位的长时间滞留。
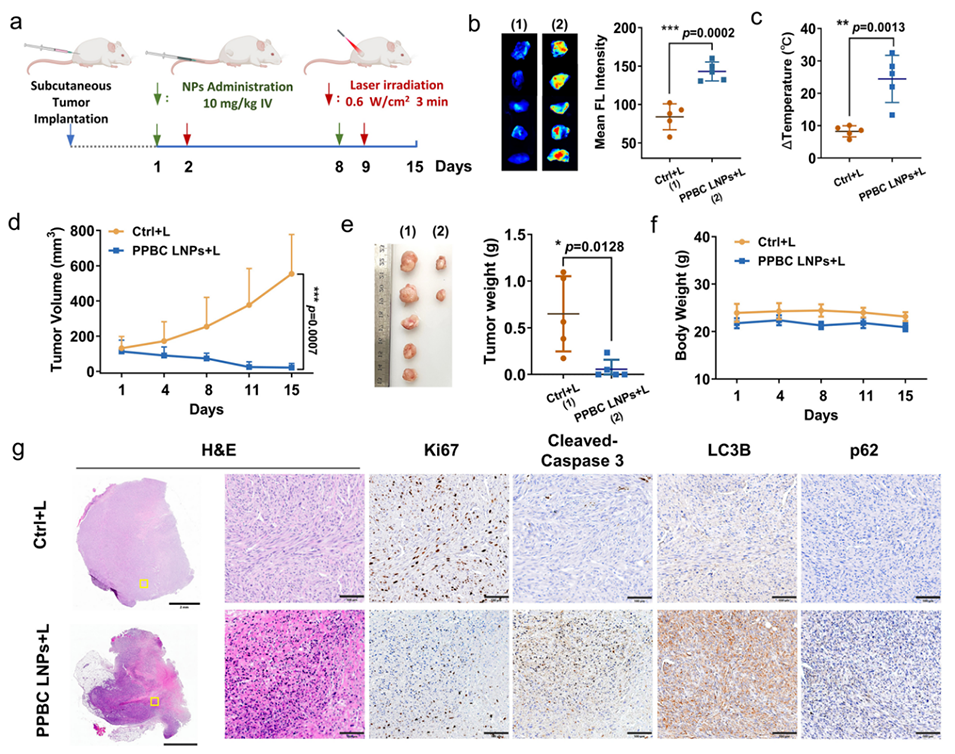
图5: 皮下瘤模型中的光疗效果。a: 皮下膀胱癌模型的治疗时间表。b, c: 离体成像及定量显示,光照后肿瘤内活性氧水平显著升高,并产生显著的光热效应。d, e, f: PPBC LNPs加激光治疗显著抑制了肿瘤生长,部分肿瘤完全消融,且小鼠体重稳定。g: 肿瘤组织的H&E和免疫组化染色显示,治疗组出现组织损伤、细胞增殖减少、凋亡增加和自噬抑制。
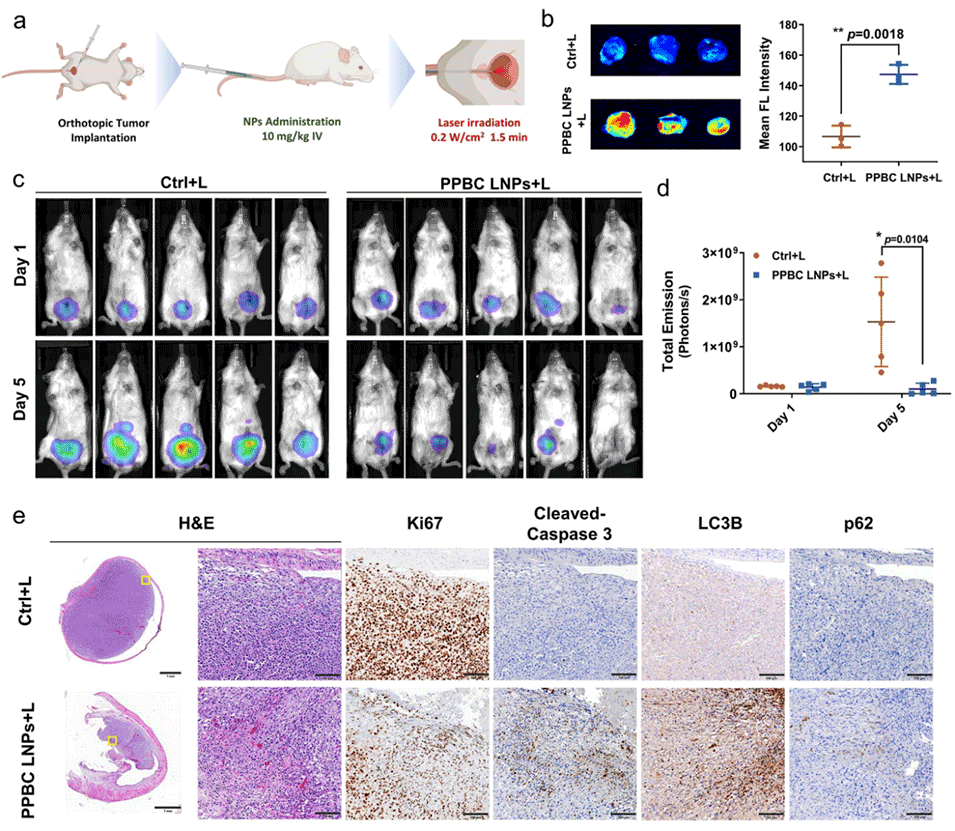
图6: 原位瘤模型中的治疗效果。a: 原位膀胱癌模型的治疗示意图。b: 离体成像及定量显示,光照后原位肿瘤内活性氧水平显著升高。c, d: 生物发光成像及定量显示,PPBC LNPs加激光治疗组肿瘤信号被显著抑制,甚至完全消融。e: 原位肿瘤组织的H&E和免疫组化染色结果与皮下模型一致,证实了治疗的有效性。
论文链接:https://doi.org/10.1007/s40820-025-01717-0
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














