
导读:
传统DNA结晶方法中对宏观晶体形态和数量的控制不足,阻碍了对DNA晶体的详细研究。近期,中国科学院宁波材料技术与工程研究所张建涛研究员、周峰研究员等人开发了双同轴通道微流控装置,借助双乳液液滴实现DNA基序与结晶习性调节剂的精准比例封装,成功制备出长径比可调的高质量DNA单晶,且能引导晶体沿纵向或横向定向生长。相关研究以“Precise Morphological Control of DNA Crystals Through Concentration‐Modulated Microfluidic Droplets”为题目,发表于期刊《Small》。
本文要点:
1、该研究提出一种借助微流控双乳液液滴(DED)微反应器实现DNA晶体宏观形态精准调控的新方法。
2、传统DNA结晶方法在宏观形态和数量控制上存在不足,而该方法通过两个同轴通道调节溶液流速,可精确调控每个微反应器内结晶习性调节剂的浓度,进而实现DNA晶体的定向生长(纵向或横向),并制备出长径比在5.94至1.10之间可控的菱面体晶体。
3、实验中,研究人员先验证了微流控装置能在DED序列中实现浓度梯度封装,其体积分辨率和浓度分辨率均达到预期标准;随后以2T三角形DNA基序为研究对象,通过调控其与结晶习性调节剂ΔH的封装比例,成功实现了DNA晶体长径比的可调,并提高了单晶体液滴的比例。
4、此外,该方法还可应用于13-mer DNA晶体,通过不同的结晶习性调节剂(Δ3'和Δ5')实现了晶体向圆柱状或上边缘加宽等不同形态的精准塑造。
5、该方法为DNA晶体的宏观结构调控提供了可靠平台,有助于深入研究结晶动力学,同时拓展了DNA晶体在微工程等领域的应用前景。
当前研究中,双乳液液滴(DED)的浓度调控依赖于精准调节两水相流速,其核心优势是无需制备多组浓度梯度溶液,可实时生成单分散性良好的晶体,但规模化生产时面临“精度-效率”的核心矛盾:流速调节的精细化要求限制了单通道的液滴生成速率,多通道并行时又可能因流体力学差异导致浓度均匀性下降。
技术优化方向可从三方面突破:
1、多通道并行与标准化:设计阵列式双同轴通道微流控芯片,通过微加工技术保证各通道的尺寸一致性(如毛细管内径、通道夹角),同时采用高精度流量分配系统(如压电式流量控制器),使多通道流速同步调控,在不损失精度的前提下提升液滴产量;
2、智能反馈调控系统:集成在线检测模块(如微流控拉曼光谱、荧光强度传感器),实时监测液滴内DNA基序与调节剂的浓度比例,通过算法自动修正流速偏差,抵消规模化生产中流体阻力变化、温度波动等干扰因素,维持浓度精度;
3、液滴融合与二次调控:先通过单通道快速生成高浓度梯度的“母液滴”,再利用微流控液滴融合技术,将不同浓度的母液滴按预设比例精准融合,实现“粗调+精调”两步调控,既提升生产效率,又保障最终浓度的精准性。
这一问题的核心启示是:精准调控技术的落地需兼顾“实验室精度”与“工程化可行性”,微流控技术的优势不仅在于微观操控,更在于通过集成化、智能化设计,实现“精准性-规模化-稳定性”的协同,这也是纳米材料从实验室走向实际应用的关键路径。
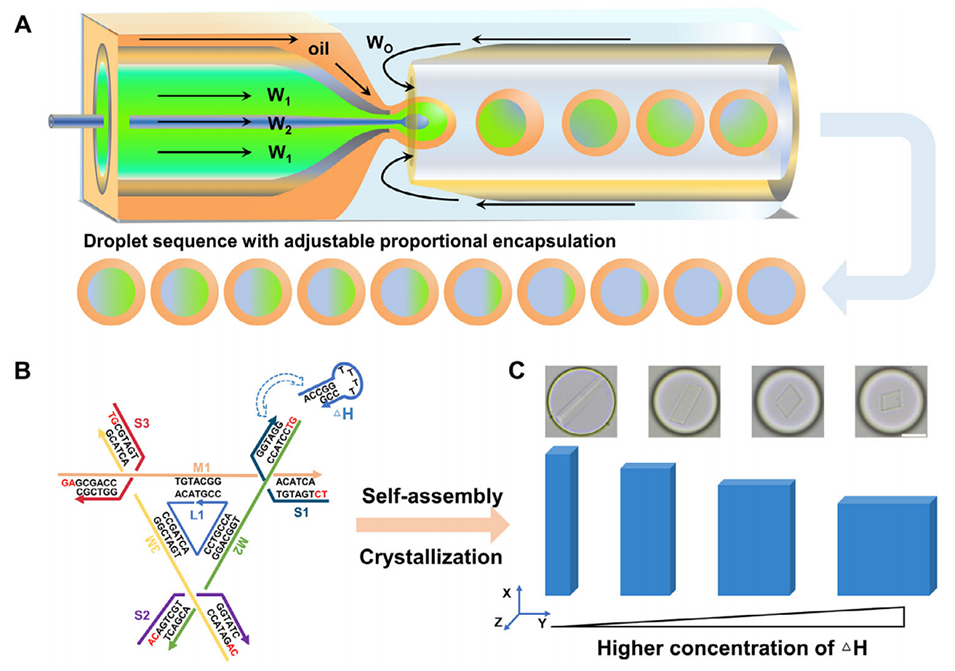
图1:基于浓度调控的微流控液滴实现DNA晶体的精准形貌控制
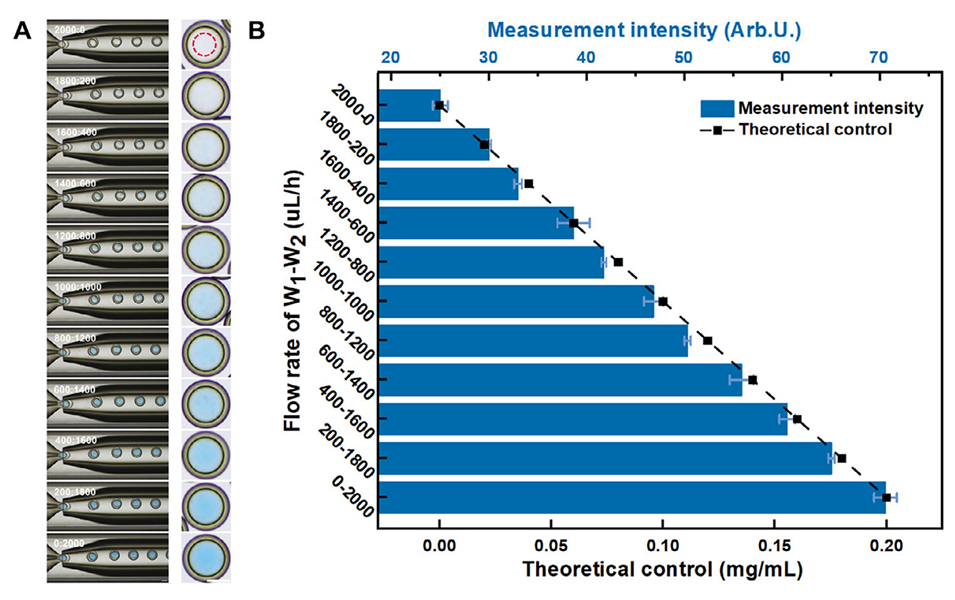
图2:双乳液液滴中的可调浓度包裹特性
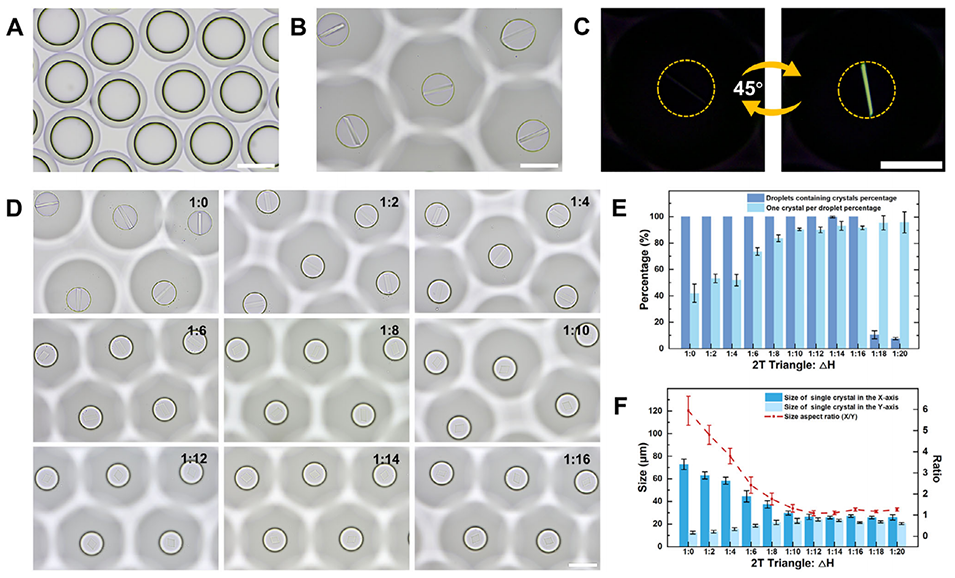
图3:双乳液液滴中 2T DNA 晶体的生长及结晶习性调节剂比例包裹下的形貌精准控制
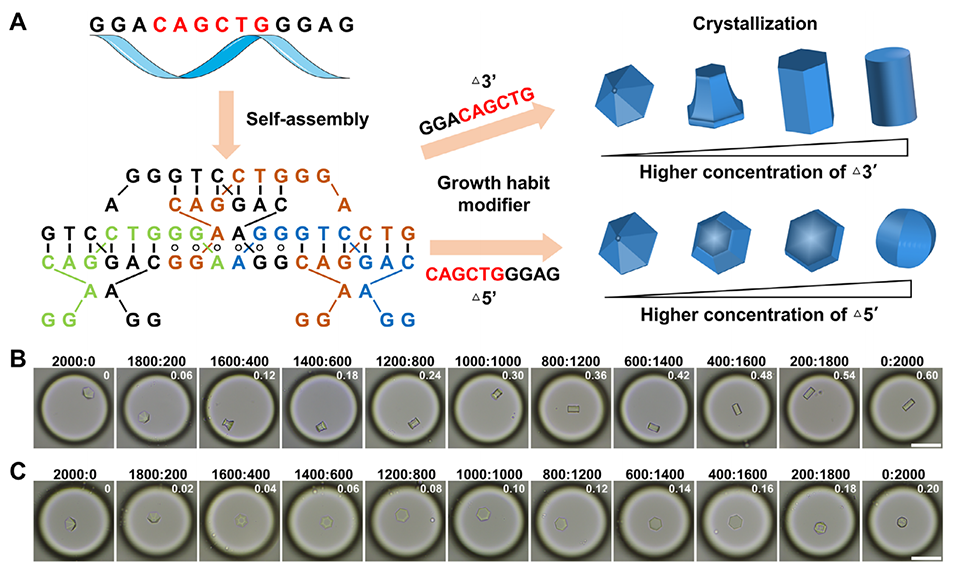
图4:双乳液液滴中 13-mer DNA 晶体的精准塑形
论文链接:https://doi.org/10.1002/smll.202511878
(本文仅供参考学习及传递微流控研究成果,版权归原作者所有,如侵犯权益,请联系删除)














