近日,深圳大学高等研究院闫昇团队在 Analytical Chemistry(IF=6.7,中科院1区TOP)发表题为 “A Pump-Free, Magnetorheological-Elastomer-Driven Oscillatory Microfluidic Device for Cell Manipulation” 的研究论文。该工作提出了一种基于磁流变弹性体驱动的无泵振荡微流控平台,在无需外部泵、阀门或电极的条件下,实现了微纳颗粒聚焦、血细胞/癌细胞分离以及低剪切条件下的血小板激活,为便携式微流控芯片和动态生物力学研究提供了新思路。
深圳大学高等研究院闫昇研究员为文章通讯作者,蒙纳士大学博士生吴佳霖为第一作者,深圳大学高等研究院硕士生刘文举,王慧锦,本科生曾凡坤,东南大学博士生刘勇等参与该工作。深圳大学高等研究院许杉杉研究员团队和北京大学深圳医院检验科为本研究提供生物样品支持。

振荡流微流控:重要但不够“轻便”
振荡流在微流控领域具有独特优势。与传统单向流相比,振荡流能够为颗粒和细胞提供重复作用的弹性力与惯性力,在颗粒聚焦、细胞分离、流体混合以及组织微环境模拟等方面展现出重要价值。然而,现有振荡微流控系统通常依赖外部注射泵、空气压缩装置,或复杂的片上电学、声学驱动结构,这在一定程度上限制了系统的小型化、生物相容性和实际应用。
针对这一问题,闫昇团队设计了一种无泵磁驱振荡微流控器件(PMOM)。该器件由旋转永磁体与集成磁流变弹性体薄膜的微流控芯片组成(图1)。旋转磁场周期性作用于弹性体膜,使其发生形变并压缩微通道,从而在直通道中产生稳定的往复振荡流。器件采用单层芯片结构,制备简单(图2),同时避免了传统外接泵和复杂片上驱动单元带来的体积、成本和集成难题。
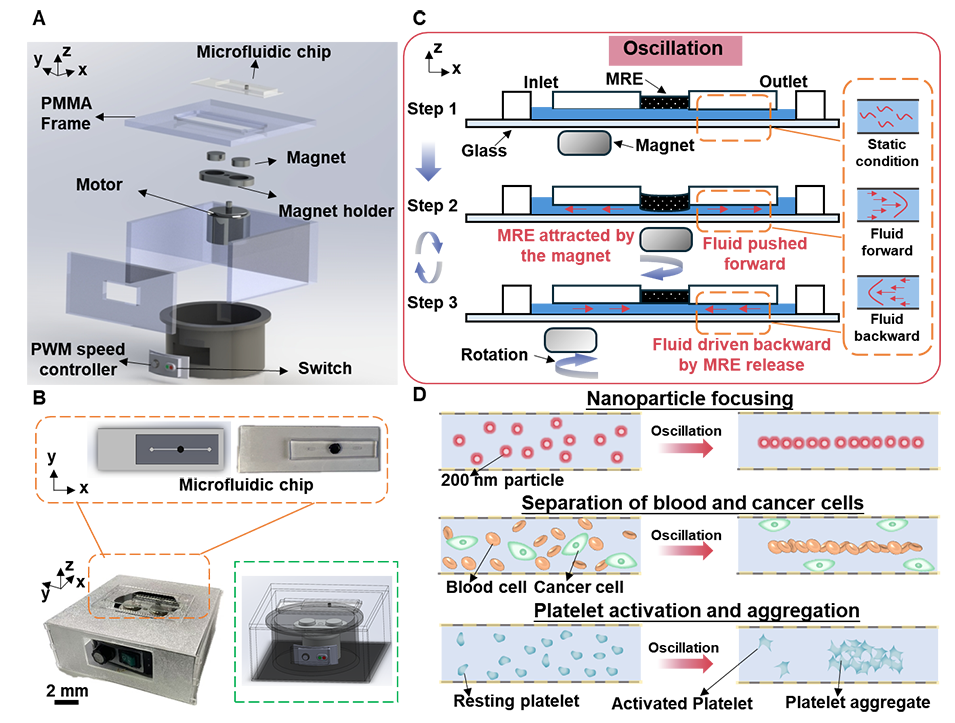
图1. PMOM器件的总体设计与应用示意图。(A) 器件分解示意图;(B) 器件与芯片实物图;(C) 工作原理示意图;(D) 在颗粒聚焦、细胞分离和血小板激活中的应用。
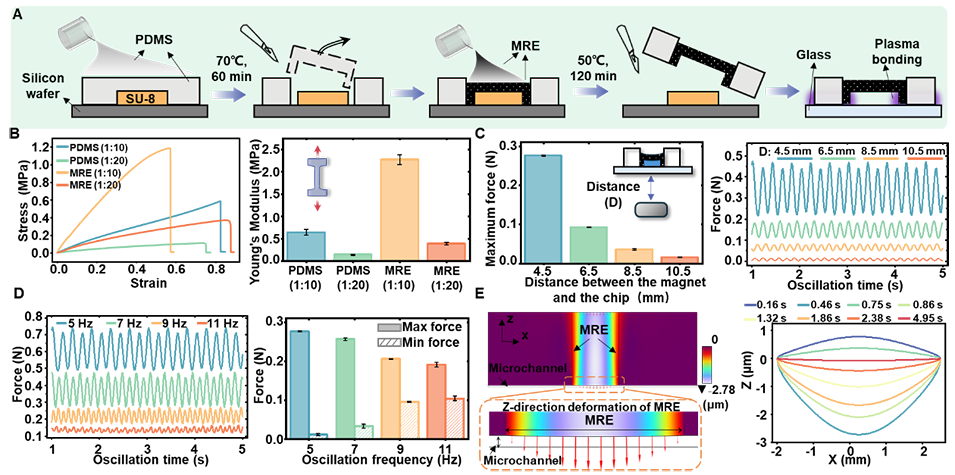
图2. PMOM器件的制备与表征。(A) 器件制备流程;(B) 不同配比下 PDMS 和 MRE 的杨氏模量;(C) 不同芯片-磁体距离下的磁驱动力;(D) 不同频率下的最大与最小磁力;(E) MRE 形变仿真结果。
超低阻塞比下实现亚微米颗粒聚焦
在颗粒操控方面,团队系统研究了聚合物浓度、振荡时间和振荡频率对颗粒迁移行为的影响(图3)。结果表明,在振荡黏弹流中,颗粒能够在有限长度直通道内经历多轮弹性力和惯性力作用,相当于在芯片中构建了一个“虚拟无限长通道”,从而显著增强横向迁移和聚焦效果。
值得关注的是,该平台在阻塞比仅为 0.0047 的条件下,实现了 0.2 μm 亚微米颗粒的清晰单线聚焦。这一数值相比传统稳态惯性微流控中约 0.07 的常规阈值降低了约 93%,显示出该器件在低约束、大通道条件下依然具备高效颗粒操控能力。论文还指出,这一结果已接近近年来高精度外部泵驱动系统所报道的极低阻塞比水平。
此外,团队还在宽度 150 μm、高度 25 μm 的较大直通道中,实现了约 270 nm 细胞外囊泡(EVs) 的聚焦与富集,表明该平台不仅能够操控微米级颗粒,也具备处理纳米尺度生物颗粒的潜力。
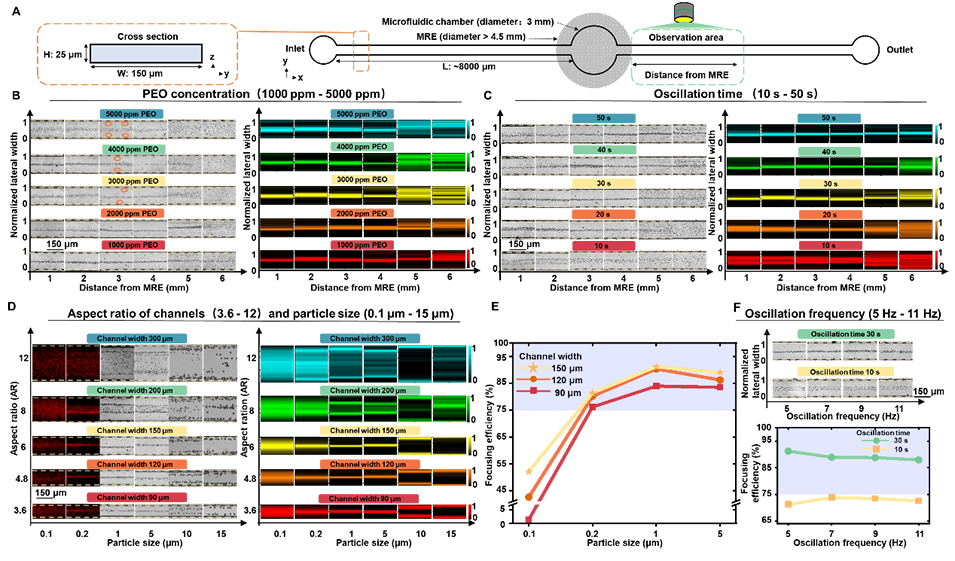
图3 振荡黏弹流中的颗粒聚焦。 (A) 芯片结构与通道尺寸;(B) 不同 PEO 浓度下 1 μm 颗粒聚焦结果;(C) 不同振荡时间下 1 μm 颗粒聚焦结果;(D) 不同粒径颗粒在不同通道中的分布;(E) 不同粒径颗粒的聚焦效率;(F) 不同频率下 1 μm 颗粒的聚焦表现。
尺寸依赖性分离血细胞与癌细胞
在生物样本操控方面,PMOM 平台进一步展示了尺寸依赖性的细胞分离能力。研究发现,在稀释全血样本中,血细胞会在振荡黏弹流作用下迁移并聚焦至通道中心;而尺寸更大的癌细胞则趋向通道两侧,从而实现无标记的空间分离(图4)。
在混合样本实验中,血细胞集中在通道中心区域,而SW620 结直肠癌细胞或者MDA-MB-231 乳腺癌细胞迁移至两侧壁区域。该结果表明,该平台能够在无需高精度外部泵的情况下,实现血细胞与癌细胞的有效分离。
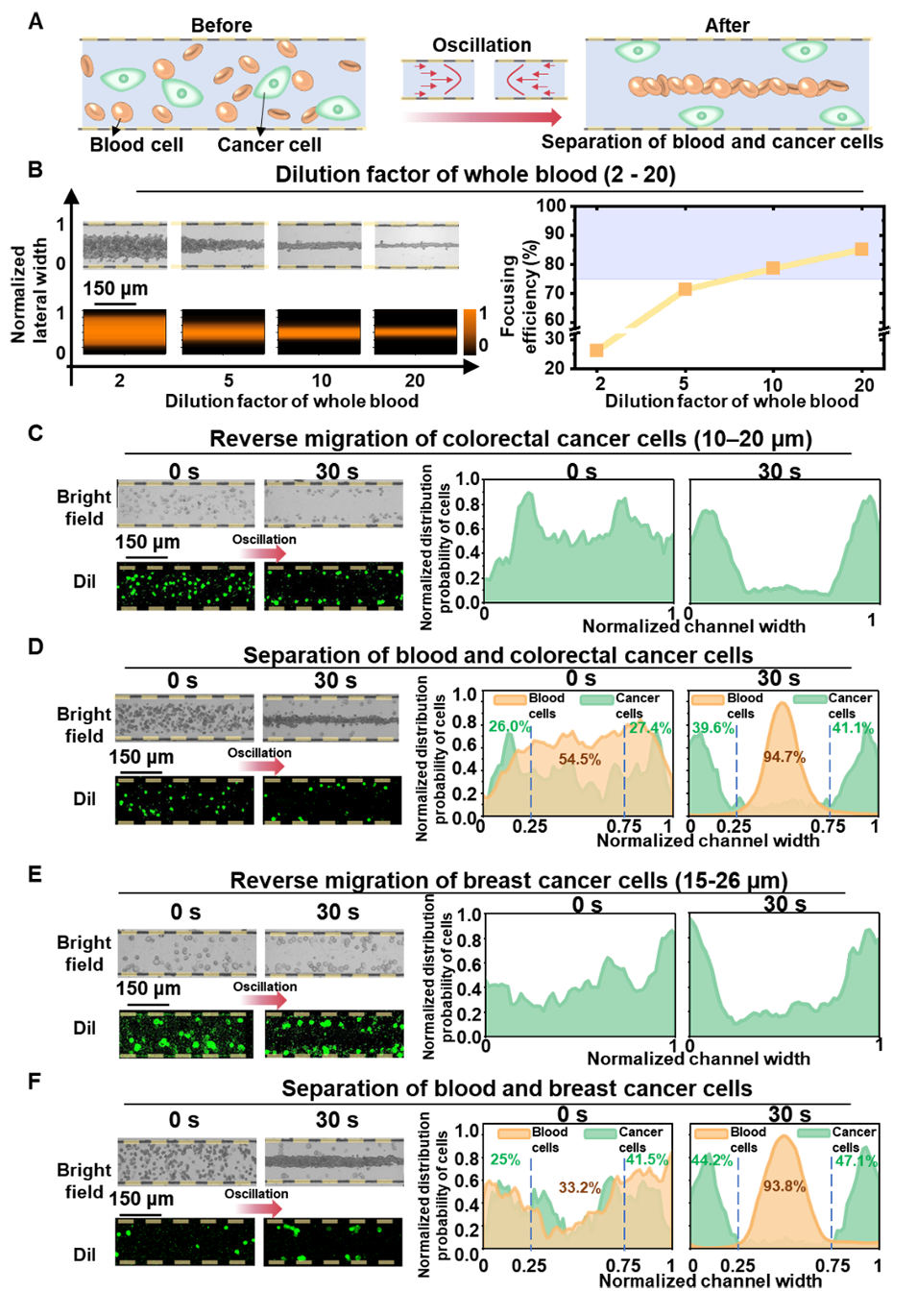
图4. 血细胞与癌细胞分离。(A) 分离原理示意图;(B) 不同稀释倍数血样的聚焦结果;(C) SW620 细胞的侧壁迁移;(D) 血细胞与 SW620 细胞的分离结果;(E) MDA-MB-231 细胞的侧壁迁移;(F) 血细胞与 MDA-MB-231 细胞的分离结果。
无化学激动剂条件下诱导低剪切血小板激活
除颗粒聚焦和细胞分离外,该平台还被用于研究振荡流条件下的血小板力学响应。研究表明,在 2000 ppm PEO 条件下,血小板在静置或单向流中保持静息状态,但在振荡流中会发生明显激活和聚集。
数值模拟显示,振荡流中快速交替变化的剪切方向和剪切幅值,即使在低于传统阈值的条件下,仍然能够通过机械刺激诱导血小板激活。进一步实验还发现,即使加入高浓度替格瑞洛抑制 ADP 受体通路,血小板在振荡黏弹流中仍可发生聚集,说明该过程主要受机械力学刺激而非传统生化激动剂驱动。这使得 PMOM 平台有望成为研究血栓形成、血小板机械敏感性以及复杂流动微环境的重要体外模型。
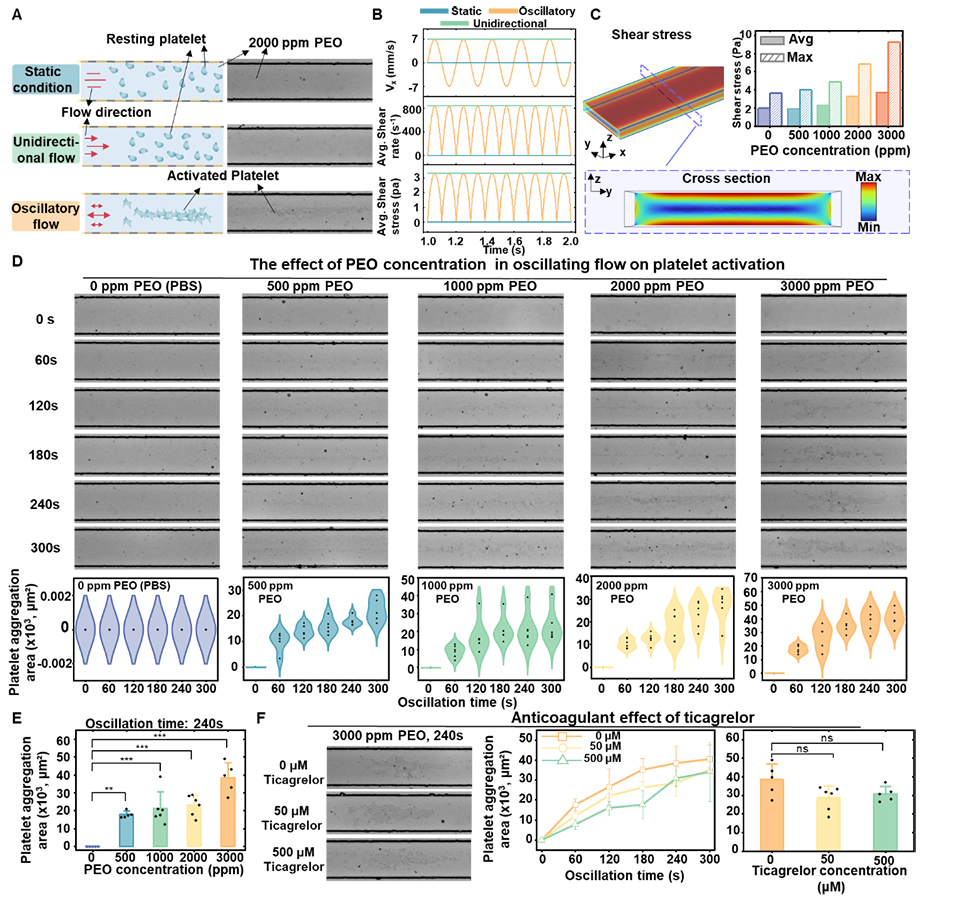
图5. 振荡黏弹流条件下的血小板激活。(A) 不同流动条件下的血小板状态;(B) 不同流动模式下的剪切特征;(C) 剪切应力分布与 PEO 浓度关系;(D, E) PEO 浓度和振荡时间对聚集的影响;(F) 替格瑞洛对血小板聚集的影响。
总结
总体来看,这项工作构建了一种结构简单、制备方便、成本较低、便于携带的无泵振荡微流控平台。该平台不仅在超低阻塞比条件下实现了亚微米颗粒与纳米囊泡聚焦,还实现了血细胞/癌细胞分离和低剪切血小板激活,展示出其在生物颗粒与细胞分离富集、细胞外囊泡分析以及动态力学微环境模拟中的广阔应用前景。未来,该平台还有望进一步拓展到组织发育模拟、药物筛选以及复杂体外循环微环境构建等方向,为微流控与生物医学交叉研究提供新的工具。
原文链接:https://pubs.acs.org/doi/10.1021/acs.analchem.6c01227














