
导读:
近期,葡萄牙米尼奥大学研究人员发表综述,介绍了药物筛选应用中使用的两代脂质仿生模型,重点探讨了微流控技术在脂质仿生模型制备中的应用,并分析了其在药物-膜相互作用中的筛选应用。最后,对这一快速发展领域的潜在未来方向进行了批判性分析。相关研究以“Lipid Microfluidic Biomimetic Models for Drug Screening: A Comprehensive Review”为题目,发表在期刊《Advanced Functional Materials》上。
本文要点:
1、开发新药复杂耗时,因此在早期阶段识别潜在的药代动力学问题至关重要。
2、许多药物靶点和代谢酶位于细胞内,需穿过细胞膜屏障。受细胞膜脂质双层结构启发,脂质基仿生平台被开发用于研究细胞膜水平的生化和生物物理过程。
3、微流控技术可将传统脂质模型微型化,开发出新一代双层模型。
4、本文概述了两代脂质模型在药物筛选中的应用,详细介绍了微流控法制备模型的复杂性,并探讨了其在药物-膜相互作用筛选中的应用,最后对未来研究方向进行了批判性分析。
一张图读懂全文:
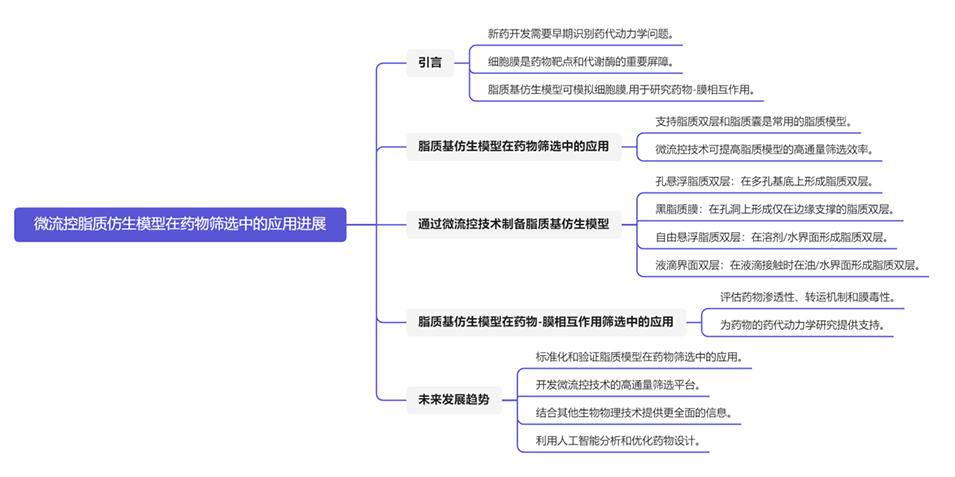
微流控技术如何促进脂质仿生模型在药物筛选中的发展?
1、小型化:微流体技术允许分析的小型化,减少反应体积和相关成本,同时提高吞吐量和分析性能。
2、高通量筛选:微流体平台实现了测试的大规模并行化,有助于将实验室程序集成到平面芯片中,并缩短处理时间。
3、受控特性:微流体可以精确控制脂质模型的性质,如大小、薄片度和管腔含量,这对研究药物与膜的相互作用至关重要。
4、快速溶液交换:微流体设备有助于快速溶液交换,使药物筛选实验中的动力学研究和体积减少成为可能。
5、表面敏感技术:微流体平台能够将脂质囊泡固定在固体支持物上,从而实现高通量实验和利用表面敏感技术进行检测。
总体而言,微流体技术为药物筛选脂质仿生模型的开发和应用提供了一个具有成本效益、可重复性和高通量的平台。
该综述得出了多项重要发现和见解:
1、药物发现的复杂性、耗时性和费用,突出了在早期阶段识别潜在药代动力学问题的重要性,以避免投资于不具潜力的候选药物。
2、脂质仿生模型在研究药物-膜相互作用方面的意义,为在受控和可调节的条件下进行生物物理研究提供了一个平台。
3、微流体技术的出现,为解决脂质仿生模型在筛选应用中的难题提供了一种前景广阔的解决方案,实现了脂质模型的微型化、高通量筛选和可控生产。
4、需要对微流体平台内不同方法产生的脂质模型进行标准化、验证和系统表征,以取代膜相互作用研究中的传统脂质模型。
总的来说,这篇综述概述了用于药物筛选的脂质仿生模型的现状、微流体技术在其发展中的作用以及这一快速发展领域的潜在未来方向。
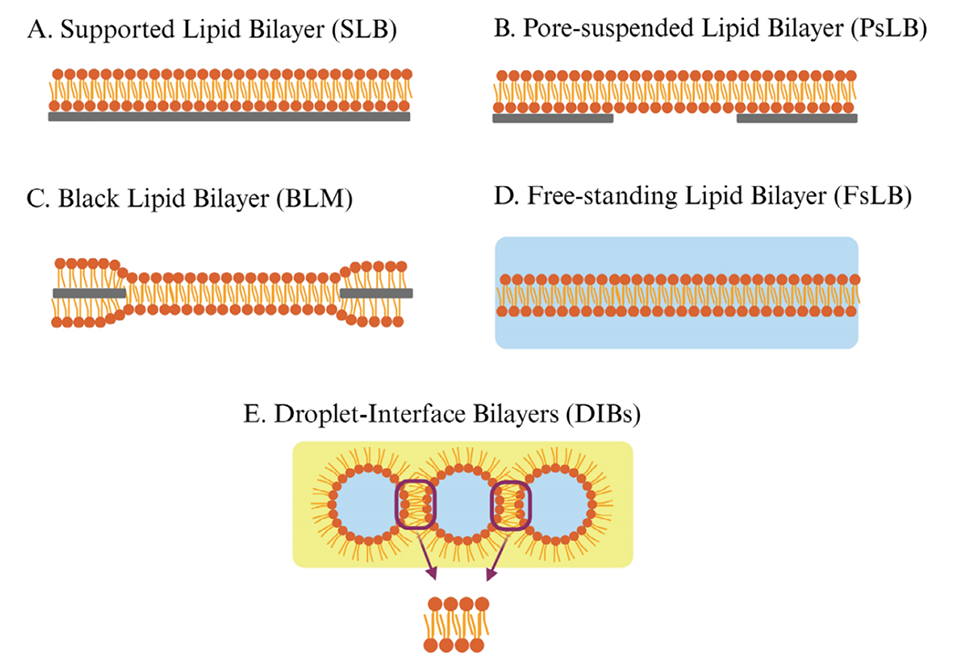
图1.支持脂质双层及其基于修饰的脂质仿生模型的示意图(未按比例)。
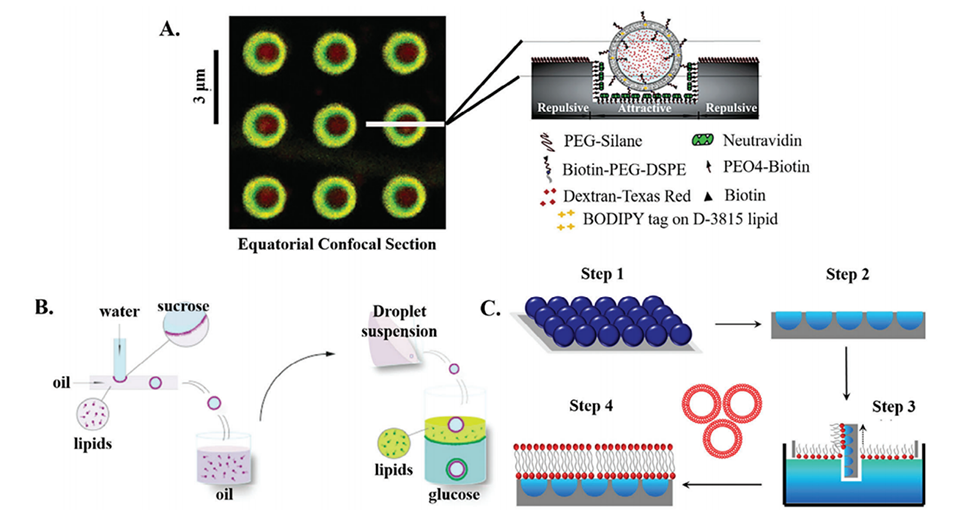
图2.使用非微流控技术形成脂质仿生模型的示例。
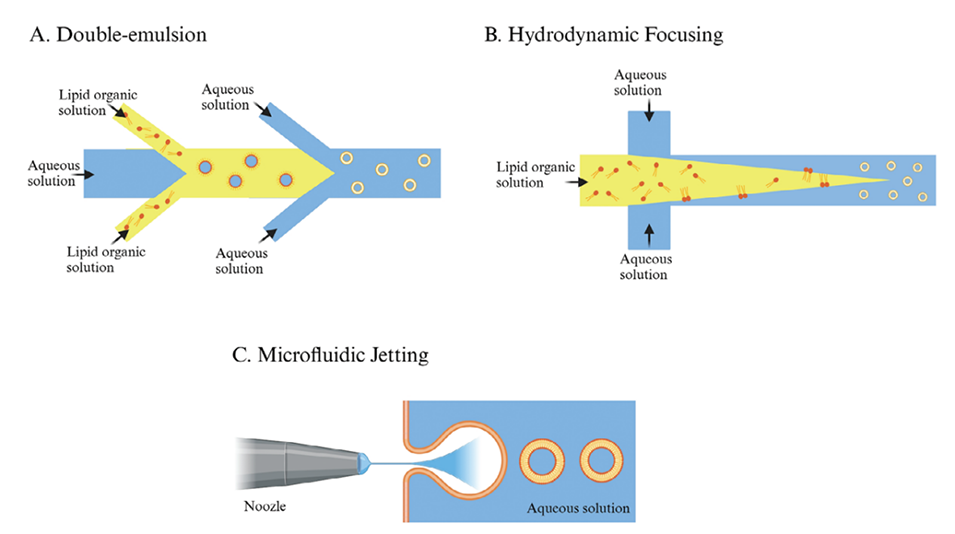
图3.在微流体中形成脂质囊泡的不同技术的示意图:A)基于双乳液;B)流体动力学聚焦和C)微流控喷射。
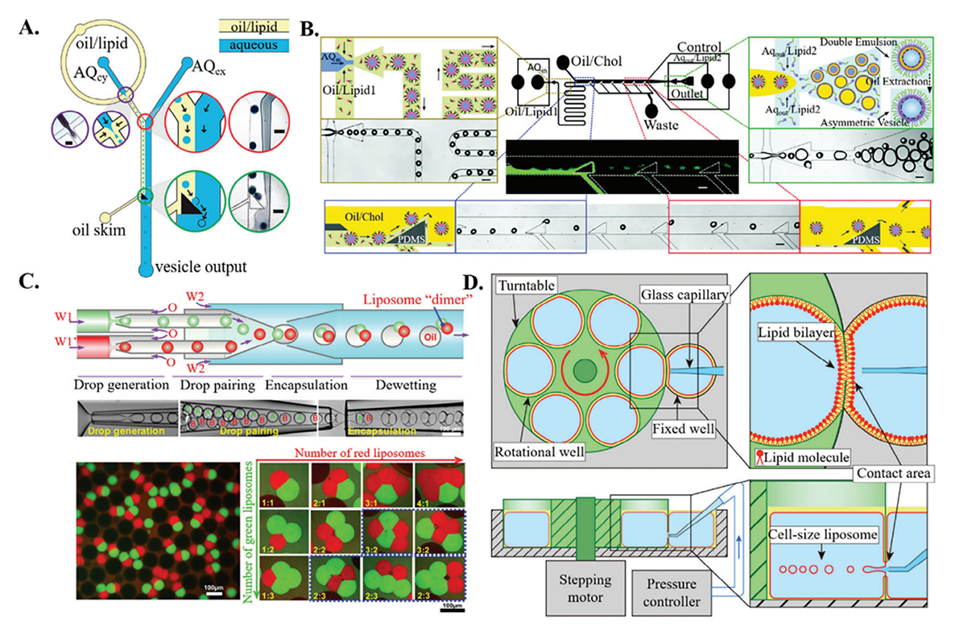
图4.在微流体中形成脂质囊泡。
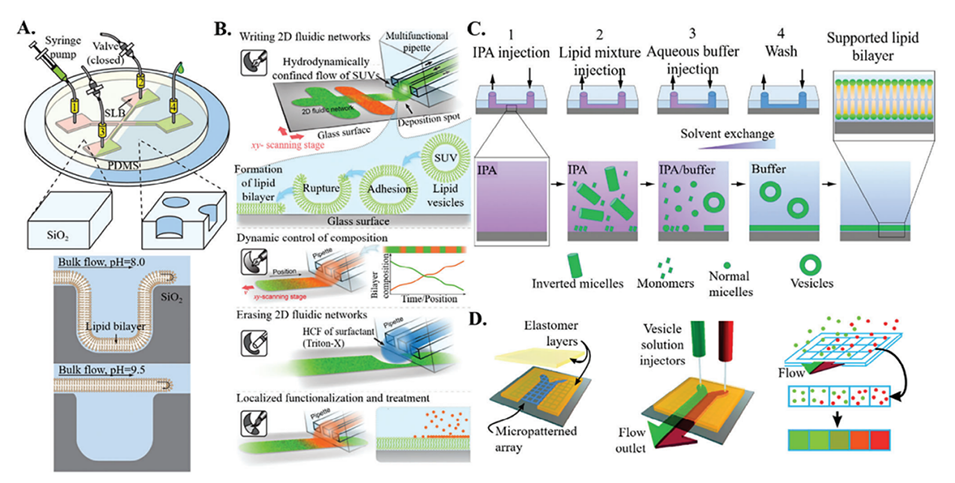
图5.使用基于囊泡融合的方法在微流体中形成SLBs。

图6.使用不同方法在微流体中形成BLMs。
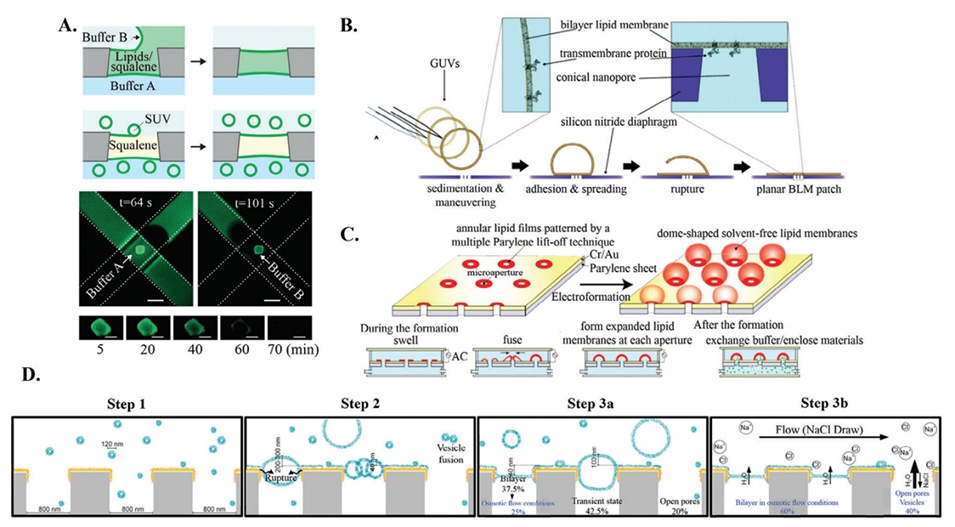
图7.在微流体中形成FsLB(A)和PsLB(B–C)的方法。
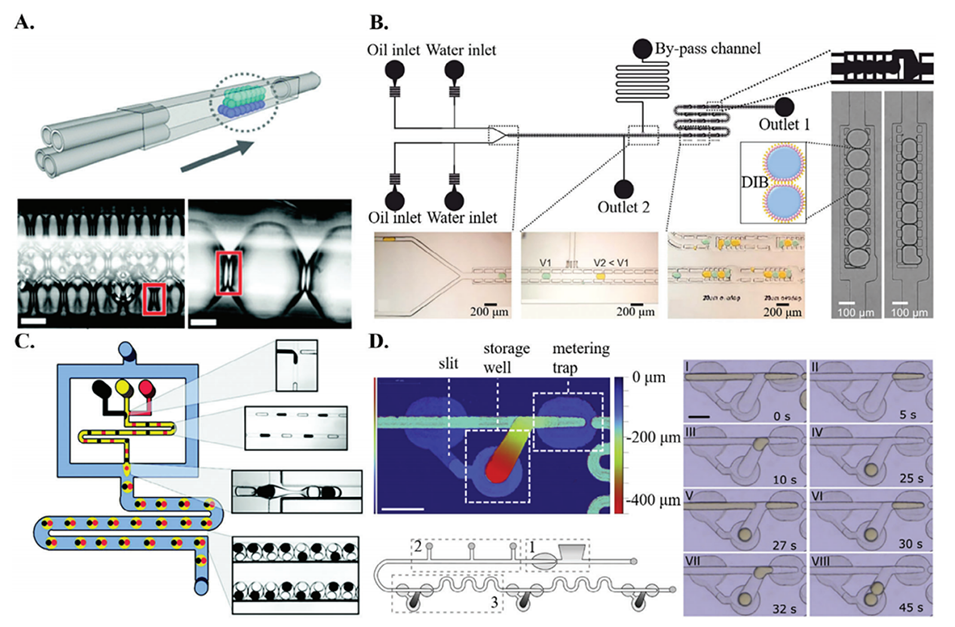
图8.在微流体中形成液滴界面双层(DIBs)。
论文链接:https://doi.org/10.1002/adfm.202315166














