
导读:
近期,复旦大学杨武利教授团队开发了一种微流控流动聚焦装置,用于制备和优化载有艾塞那肽(Exenatide)的聚乳酸-羟基乙酸共聚物(PLGA)微球。通过添加表面活性剂和优化工艺参数,显著提高了药物的负载能力和缓释性能,同时实现了生产效率的提升,达到每小时2克的生产速率。这项研究为肽类药物的缓释提供了新的方法,相关成果以“Microfluidic-based preparation of PLGA microspheres facilitating peptide sustained-release”为题,发表在期刊《Materials Letters》上。
本文要点:
1、本研究开发了一种微流控流动聚焦装置,用于制备和优化负载艾塞那肽的聚乳酸-羟基乙酸共聚物(PLGA)微球。
2、通过添加表面活性剂,显著提高了乳液的稳定性,从而增加了药物的负载能力。
3、将药物载体的粒径增大至30μm,显著减少了突发释放现象。
4、此外,采用多通道液滴微流控装置,生产能力提高了100倍,达到每小时2克的生产速率。
5、通过对载肽微球的释放行为进行综合评估,确认了最佳制备工艺,所得产物具有良好的单分散性和持续释放能力,为肽类药物载体的制备提供了指导。
使用微流控设备制备载有肽类药物的微球具有以下几个优势:
1、提高均匀性:微流控设备能够生产出粒径均一、药物分布均匀的微球。
2、增加药物负载能力:通过添加表面活性剂,微流控过程显著提高了药物的负载能力。
3、减少突发释放:通过控制微球的粒径和配方参数,可以显著降低药物的突发释放现象,实现更持续的释放特性。
4、提高生产效率:多通道微流控设备能够实现生产速率的显著提升,达到每小时2克的生产能力,适合工业化应用。
5、简化工艺:微流控方法可以简化制备过程,减少传统方法中常见的复杂步骤和设备需求。
6、可扩展性:微流控设备的设计便于从实验室规模扩展到商业规模,能够满足更大生产量的需求。
微流控技术在制备负载艾塞那肽的PLGA微球时,主要通过以下方式解决突发释放的问题:
1、添加表面活性剂Span 80提高乳液稳定性:
添加Span 80可以大幅提高乳液的稳定性,减少内水相向连续相的泄漏,从而提高药物的负载量和包封效率。
2、增加微球尺寸以减少突发释放:
制备较大尺寸(30μm)的微球相比小微球,可以显著降低初始突发释放,并在5周内保持稳定的缓释特性。这是因为较大微球的剪切力较小,内水相与连续相的融合也较少,从而减少了药物溶液的泄漏。
3、在内水相中添加PVA改善缓释性能:
添加PVA可以增加内水相的粘度,从而降低药物从内水相到外水相的扩散速率,减少药物在释放初期的快速泄漏。同时,PVA的亲水性也有助于后期的持续缓释。
4、优化药物与PLGA的质量比:
当艾塞那肽与PLGA的质量比降低到2:20时,可以有效消除突发释放现象。这是因为较低的药物含量使其更多地分散在微球内部,而不是集中在表面。
综上所述,通过添加表面活性剂、合理调控微球尺寸、内水相成分以及药物与PLGA的质量比等参数,可以有效解决艾塞那肽负载PLGA微球的突发释放问题,为制备具有优良缓释性能的肽类药物微球提供了重要指导。
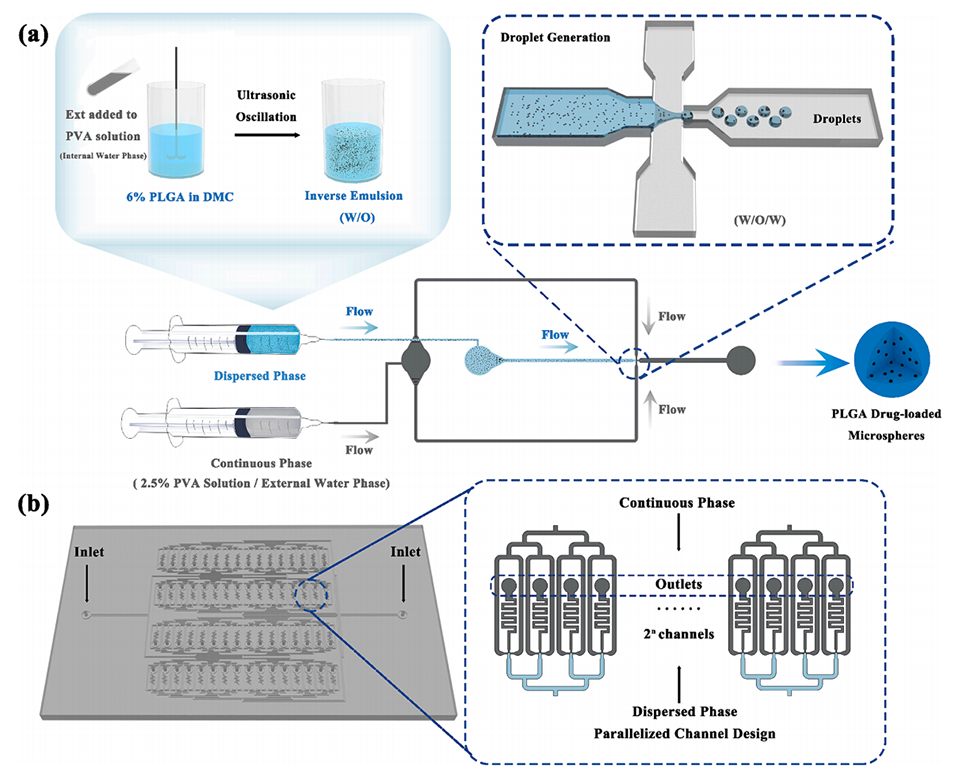
图1.(a)肽负载PLGA微球的制备;(b)多通道液滴微流体装置的设计。
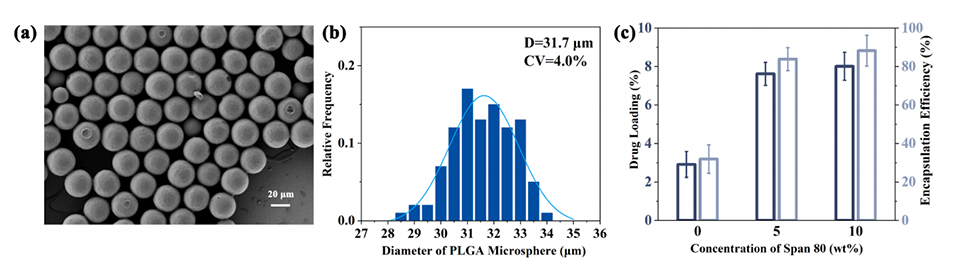
图2.(a)Ext负载PLGA微球的SEM图像,(b)粒径分布,(c)不同Span 80浓度制备的肽负载微球的DL和EE。
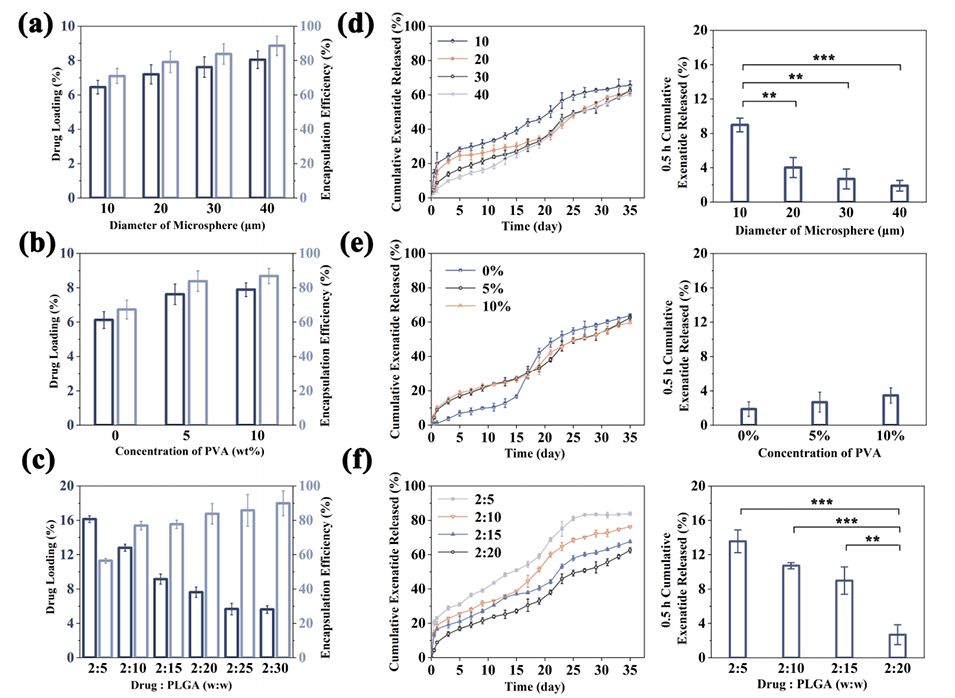
图3.(a)不同微球尺寸、(b)不同PVA浓度和(c)不同Ext与PLGA质量比制备的肽负载微球的DL和EE。(d)不同尺寸、(e)不同PVA浓度和(f)不同Ext与PLGA质量比制备的肽负载微球的释放曲线和0.5小时初始突释。

图4.由(a)8通道微流体设备和(b)64通道微流体设备生成的PLGA液滴的光学图像和Ext负载PLGA的SEM图像。
论文链接:https://doi.org/10.1016/j.matlet.2024.136675














