急性耐甲氧西林金黄色葡萄球菌(MRSA)肺炎是一种常见的严重肺部感染,伴随较高的发病率和死亡率。由于MRSA的抗生素耐药性、毒性和致病性日益增加,迫切需要探索有效的抗菌策略。

近期,南开大学医学院王志刚副教授、庞代文教授等人开发了一种基于可吸入聚合物微粒的新型治疗策略,用于MRSA肺炎的噬菌体与光热协同治疗。该研究通过将噬菌体与光热剂吲哚菁绿结合并负载于多孔微球中,实现了对肺部深部感染的有效递送和治疗,显著降低了感染小鼠肺部的细菌负荷,同时减轻炎症和损伤,展现出良好的临床应用前景。相关研究以“Inhalable Polymeric Microparticles for Phage and Photothermal Synergistic Therapy of Methicillin-Resistant Staphylococcus aureus Pneumonia”为题目,发表在期刊《Nano Letters》上。
本文要点:
1、本研究开发了一种可吸入干粉制剂,该制剂由聚乳酸-羟基乙酸共聚物(PLGA)制备的多孔微球组成,内部负载有吲哚菁绿(ICG)修饰的耐热噬菌体。
2、这种制剂可以将治疗剂量的ICG修饰活性噬菌体输送到深部肺组织感染部位,避免被肺泡巨噬细胞快速清除。
3、结合噬菌体疗法和光热疗法的协同作用,该制剂在急性MRSA肺炎中显示出强大的杀菌作用。
4、凭借其在室温下的长期稳定性和可吸入特性,该制剂有望成为临床治疗MRSA肺炎的有前景的药物。
如何优化PLGA多孔微球的制备以提高其载药能力和药物释放性能?
1.优化微球的制备工艺
乳化溶剂挥发法:这是制备PLGA微球的常用方法。通过调整乳化剂的种类和用量,可以控制微球的粒径和孔隙率。例如,使用聚乙烯醇(PVA)作为乳化剂时,增加PVA的浓度可以提高微球的孔隙率,从而增加载药量。
喷雾干燥法:这种方法可以制备出粒径均匀、孔隙率高的微球。通过调整喷雾参数(如喷雾速度、进风温度等),可以优化微球的结构,提高载药能力和药物释放性能。
冷冻干燥法:适用于热敏感药物。通过控制冷冻和干燥过程中的温度和压力,可以制备出具有高孔隙率和良好药物包封率的微球。
2.调整PLGA的组成和分子量
PLGA组成:PLGA是由乳酸和羟基乙酸共聚而成的聚合物,其组成比例会影响微球的降解速率和孔隙率。增加乳酸的比例可以提高微球的强度和稳定性,但可能会降低孔隙率;增加羟基乙酸的比例则可以提高孔隙率,但可能会降低微球的强度。
分子量:PLGA的分子量越高,微球的机械强度和稳定性越好,但药物释放速率可能会变慢。因此,需要根据药物的性质和治疗需求选择合适的分子量。
3.优化微球的孔隙结构
添加孔隙形成剂:在制备过程中加入一些孔隙形成剂(如碳酸氢钠、氯化钠等),可以在微球内部形成孔隙,增加微球的比表面积,从而提高载药量和药物释放速率。
控制孔隙率和孔径大小:通过调整制备工艺参数(如搅拌速度、溶剂挥发速度等),可以控制微球的孔隙率和孔径大小。较大的孔径有助于药物的快速释放,但可能会降低微球的机械强度。
4.表面修饰
增加表面电荷:通过在微球表面引入电荷(如通过添加带电的聚合物或表面活性剂),可以提高微球对药物的吸附能力,从而增加载药量。
靶向修饰:在微球表面修饰特定的靶向分子(如抗体、肽段等),可以提高微球对病变组织的靶向性,减少药物在非靶组织的分布,提高治疗效果。
5.药物包封技术
多层包封:采用多层包封技术,可以将药物包封在微球的内部,减少药物在制备和储存过程中的损失,提高载药量和药物稳定性。
纳米包封:将药物先制成纳米颗粒,再包封到微球中,可以提高药物的溶解度和稳定性,同时增加微球的载药量。
6.优化药物释放条件
pH敏感性:通过在微球中引入pH敏感的聚合物或交联剂,可以使微球在特定的pH环境中(如炎症部位的酸性环境)快速释放药物,提高药物的局部浓度。
温度敏感性:引入温度敏感的材料,可以使微球在体温下快速释放药物,提高药物的释放速率。
7.实验验证与优化
体外实验:通过体外药物释放实验,评估微球在不同条件下的药物释放性能,优化制备工艺。
体内实验:在动物模型中验证微球的生物相容性、药物分布和治疗效果,进一步优化微球的制备工艺。
综合应用上述方法,可以有效提高PLGA多孔微球的载药能力和药物释放性能,从而为临床应用提供更有效的药物递送系统。
这种基于噬菌体与光热协同治疗的策略相比传统抗生素具有以下优势:
1、针对性强:噬菌体具有高度的宿主特异性,能够精准靶向MRSA,减少对正常菌群的干扰,降低抗生素治疗中常见的菌群失调风险。
2、协同作用:结合噬菌体的裂解作用和光热治疗的局部高温效应,能够产生协同的杀菌效果,更有效地消灭耐药菌,提高治疗成功率。
3、减少耐药性:噬菌体不易诱导细菌产生耐药性,与传统抗生素相比,这种策略有助于延缓耐药菌的产生和发展。
4、降低副作用:光热治疗的局部高温效应能够在短时间内杀死细菌,减少药物在体内的停留时间,从而降低药物的全身副作用。
5、可吸入性:通过可吸入的聚合物微粒递送系统,能够有效将药物递送至肺部深部感染部位,提高药物在感染部位的浓度,增强治疗效果。
6、长期稳定性:该制剂在室温下具有长期稳定性,便于储存和运输,更适合临床应用和大规模推广。
综上所述,这种治疗策略在治疗MRSA肺炎方面具有显著的优势,能够为临床治疗提供一种更安全、有效且可持续的替代方案。
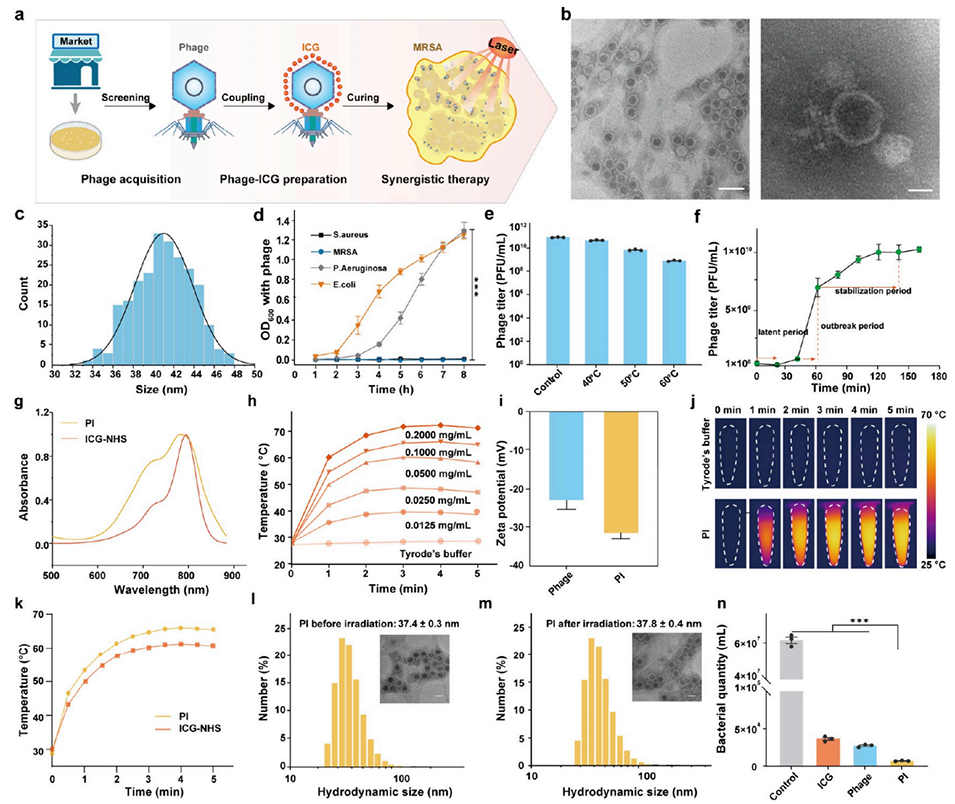
图1.噬菌体的筛选和鉴定及其与ICG偶联后(Phage-ICG,PI)的性质表征。
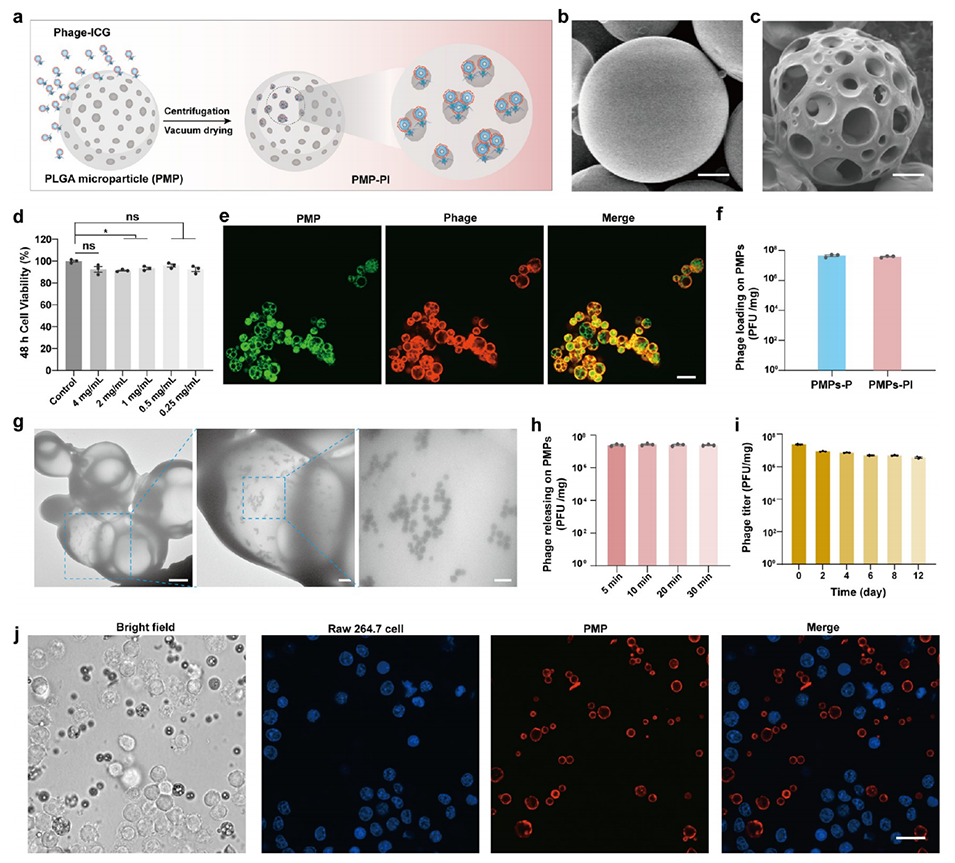
图2.多孔PLGA微球(PMP)的制备和噬菌体-ICG的负载。
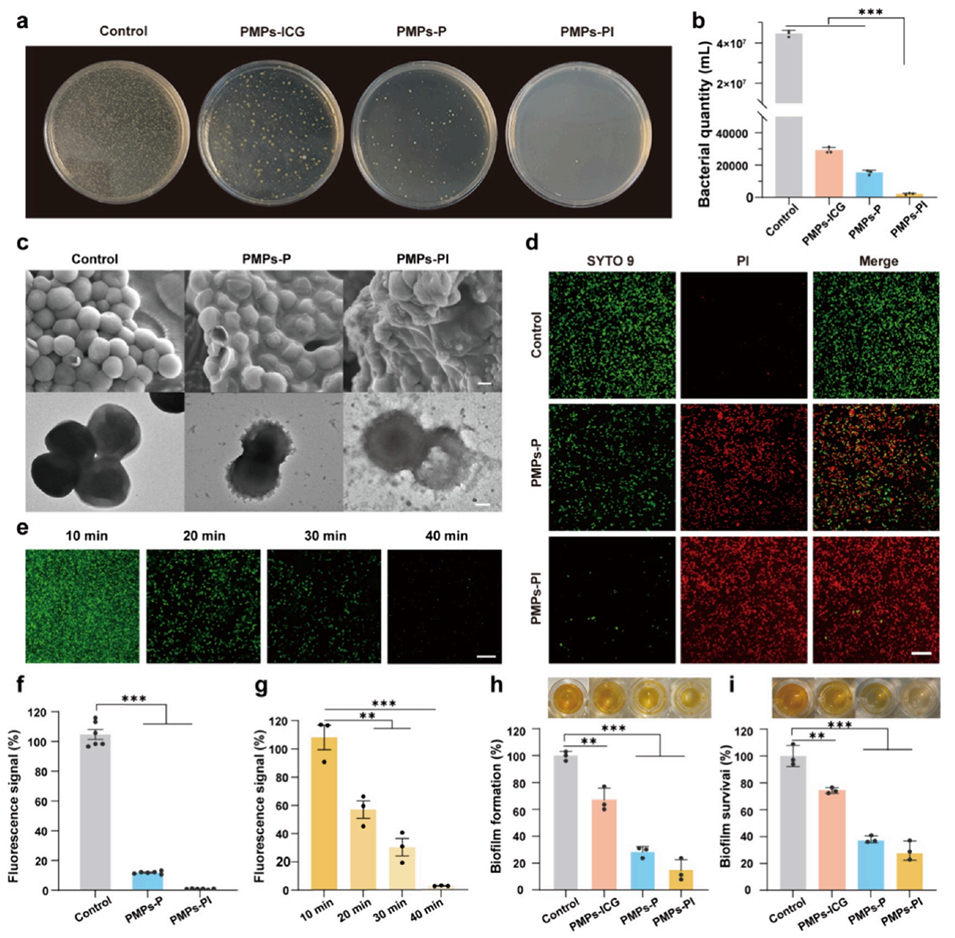
图3.PMPs-PI对MRSA体外杀菌效果的验证。
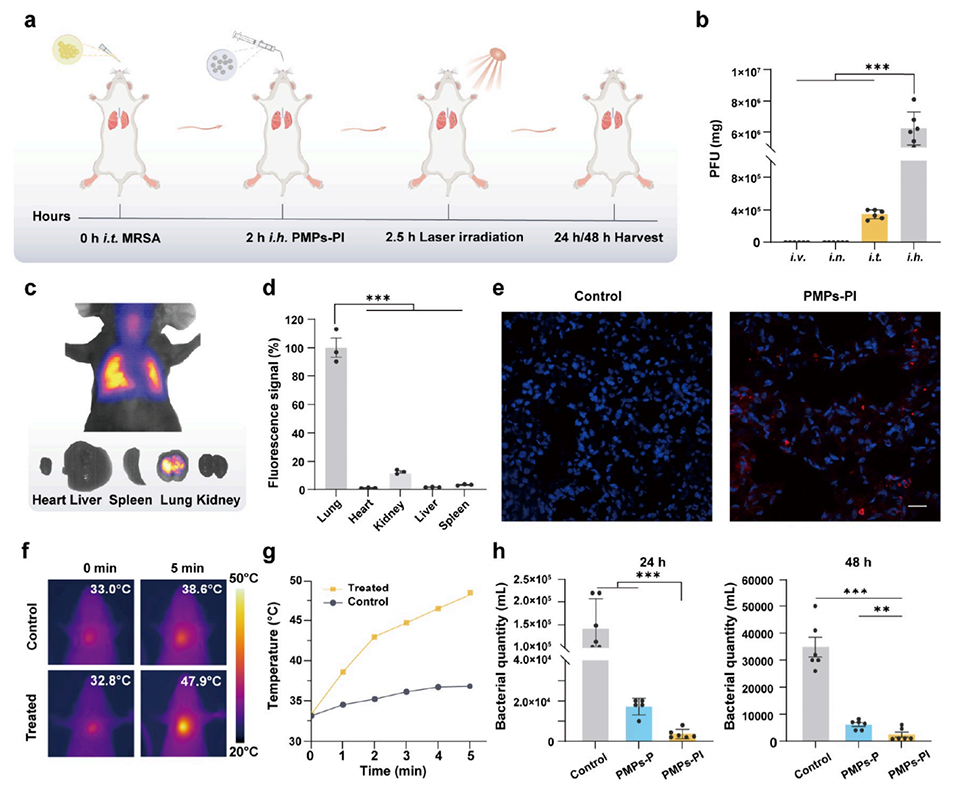
图4.干粉制剂PMPs-PI吸入治疗小鼠MRSA肺炎。
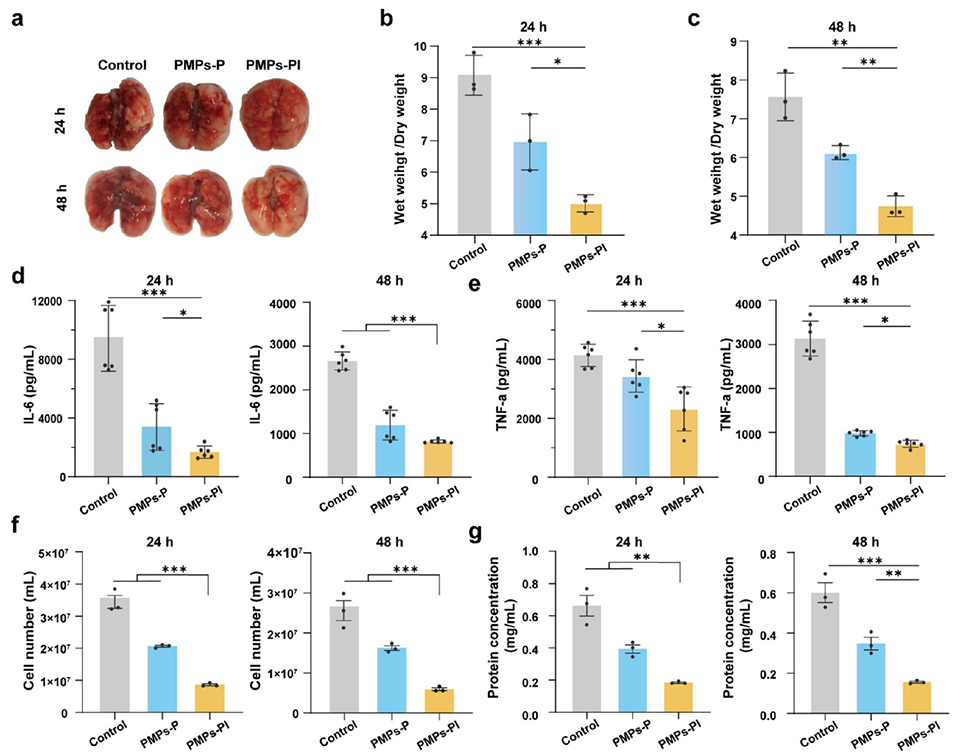
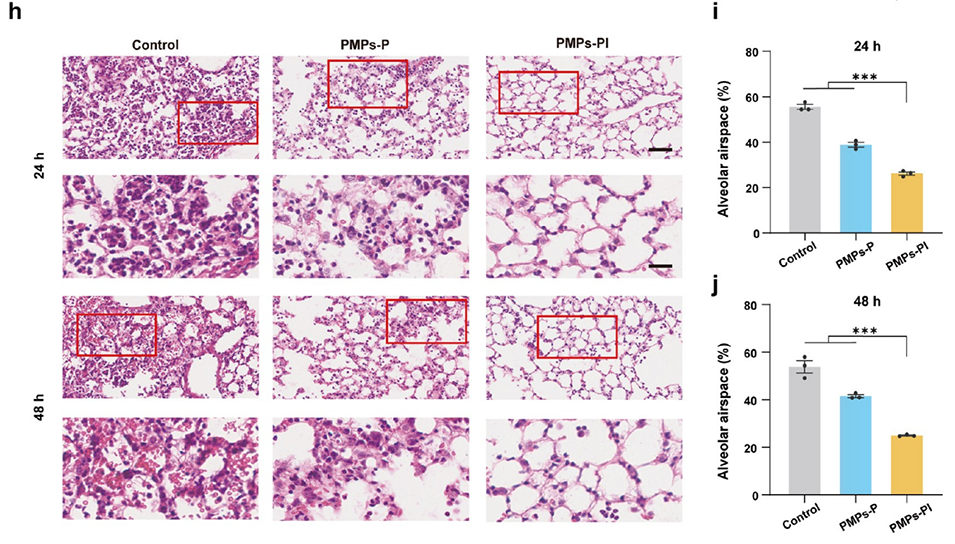
图5.PMPs-PI减轻了MRSA感染引起的小鼠肺部炎症损伤。
论文链接:https://doi.org/10.1021/acs.nanolett.4c02318














