
导读:
水凝胶微粒(HMPs)在组织工程和药物递送中应用广泛,但传统共价交联法存在毒性且难以降解。近期,有研究人员提出基于立体复合作用的物理交联策略,通过4臂聚乙二醇(PEG)引发L-乳酸(PLLA)和D-乳酸(PDLA)寡聚物自组装,结合微流控技术制备出尺寸可控、生物相容且可降解的立体复合水凝胶微粒(SC-HMPs)。该材料兼具高机械强度与功能化潜力,为再生医学和药物递送提供了新的解决方案。相关研究以“Microfluidic Assembly of Degradable, Stereocomplexed Hydrogel Microparticles”为题目,发表在期刊《Journal of the American Chemical Society》上。
本文要点:
1、本研究通过立体复合作用替代传统共价交联方法,利用4臂聚乙二醇(PEG)引发L-乳酸(PLLA)和D-乳酸(PDLA)寡聚物的自组装,制备出生物相容且可降解的立体复合水凝胶微粒(SC-HMPs)。
2、采用微流控技术调控分散相流速(0.9–2.0 μL/min),成功制备了尺寸精确可控的微粒,直径分别为33.7±0.5、62.4±0.6和105.7±0.8 μm,满足不同生物医学应用的需求。
3、通过广角X射线散射(WAXS)和差示扫描量热法(DSC)验证了立体复合结构的形成,显示特征衍射峰(2θ=12.2°、21.2°、24.2°)及高熔点(Tm=159°C),表明材料具有优异的热稳定性和机械性能。
4、交联剂中的炔基支持硫醇-炔点击反应,可实现微粒的预组装或后组装功能化(如荧光标记),拓展了其在药物递送和组织工程中的功能性应用。
5、不同尺寸的SC-HMPs在溶胀实验中表现出显著差异,小尺寸微粒(33.7 μm)溶胀率可达77.0%,且所有微粒在溶胀后均能恢复到接近其原始尺寸和形状,显示出良好的可逆性和稳定性。
微流控技术制备水凝胶微粒的具体步骤如下:
1、芯片制备:通过光刻技术制作硅模具,浇注PDMS并固化,形成含微流通道的芯片,等离子处理后与玻璃片键合。
2、溶液配制:
分散相:10 wt% PEG-PLLA/Pr-PDLA(2:1摩尔比)溶于乙酸乙酯。
连续相1:3 vol% Span80(表面活性剂)溶于矿物油。
连续相2:9 wt% PVA溶于去离子水。
3、液滴形成:
使用三通道微流控装置分别输送有机相、油相和水相,有机相(含高分子材料)在装置中依次被油层(含表面活性剂)和水层(含稳定剂)包裹,形成“水包油包有机相(Org/O/W)”双乳液体系。
调节分散相流速(9–2.0 μL/min)和连续相流速(油相23.0 μL/min,水相32.0 μL/min),通过“jetting”模式生成稳定液滴。
4、立体复合驱动凝胶化:液滴进入水相后,水作为反溶剂触发PLA立体复合结晶,PVA辅助稳定液滴,防止聚集。
5、纯化与收集:离心去除油相和杂质,多次水洗后通过细胞筛过滤,按粒径分选(40–150 μm筛网),最终获得尺寸均一的SC-HMPs。
立体复合方法相比传统共价交联有何优势?
1、生物相容性更高:无需使用光引发剂或紫外光,避免了传统共价交联(如丙烯酸酯、硫醇-烯反应)中可能产生的毒性物质,更适合直接接触细胞的生物应用。
2、可降解性:立体复合作用通过物理交联(PLA立体复合晶体)实现,可在体内逐步水解降解,而共价交联的化学键难以分解,阻碍组织再生。
3、机械性能优化:立体复合结构形成密集的晶体域,赋予材料更高的熔点(T<sub>m</sub>=159°C)和热稳定性,优于均质晶体(HC)或非晶态结构。
4、功能化灵活性:交联剂中的炔基可通过硫醇-炔点击反应实现预组装或后组装功能化(如荧光标记),扩展了材料的应用范围。
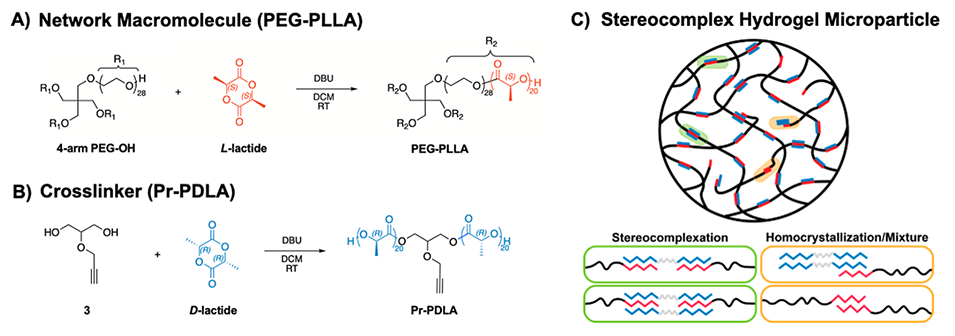
图1.(a)通过L-丙交酯开环聚合合成的等规聚L-乳酸(PLLA)功能化4臂聚乙二醇(PEG-PLLA)星形聚合物;(b)通过D-丙交酯开环聚合合成的炔基功能化等规聚D-乳酸(Pr-PDLA)交联剂。(c)聚合物前体在微流控通道中自组装形成立体复合水凝胶微粒(SC-HMP),其中PLLA链与PDLA寡聚物通过立体复合作用形成物理交联网络。通过使用低分子量PLLA/PDLA及“水包油包有机相”条件抑制同构结晶。

图2.微流控制备SC-HMPs的流程:PDMS微流控芯片引导有机相(10 wt%聚合物前体/乙酸乙酯)、油相(3 vol% Span80/矿物油)和水相(9 wt% PVA/去离子水)形成“水包油包有机相(Org/O/W)”双乳液。分散相通过尖端流动形成稳定液滴,水相触发立体复合凝胶化,最终液滴在去离子水中完成固化。
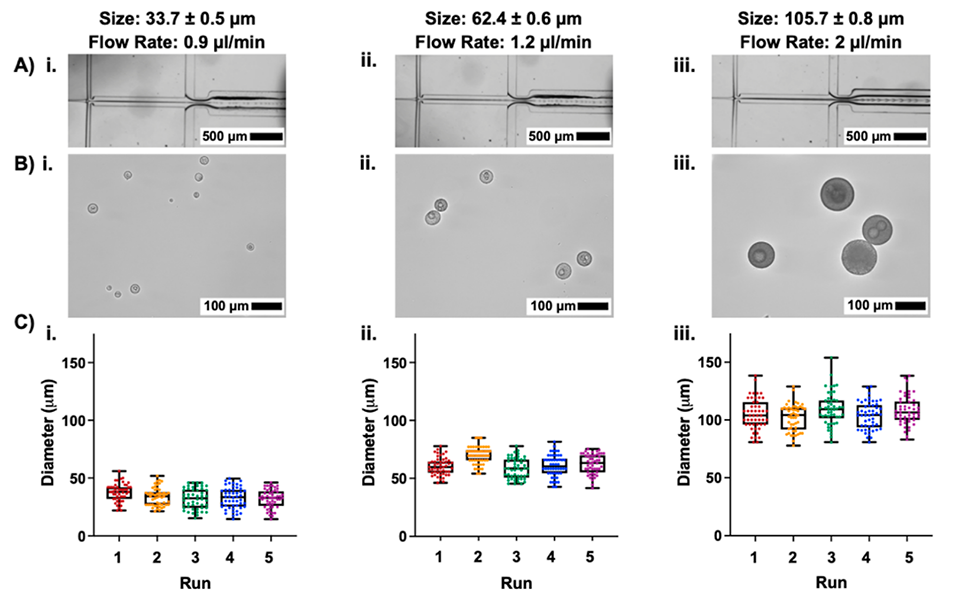
图3.微流控调控SC-HMPs的粒径:(a)分散相流速分别为0.9、1.2、2.0 μL/min时的液滴形成显微图像(2×放大);(b)对应流速下SC-HMPs的显微图像(20×放大);(c)不同流速(0.9、1.2、2.0 μL/min)制备的SC-HMPs粒径分布统计(n=5次实验,每实验测量50个微粒)。
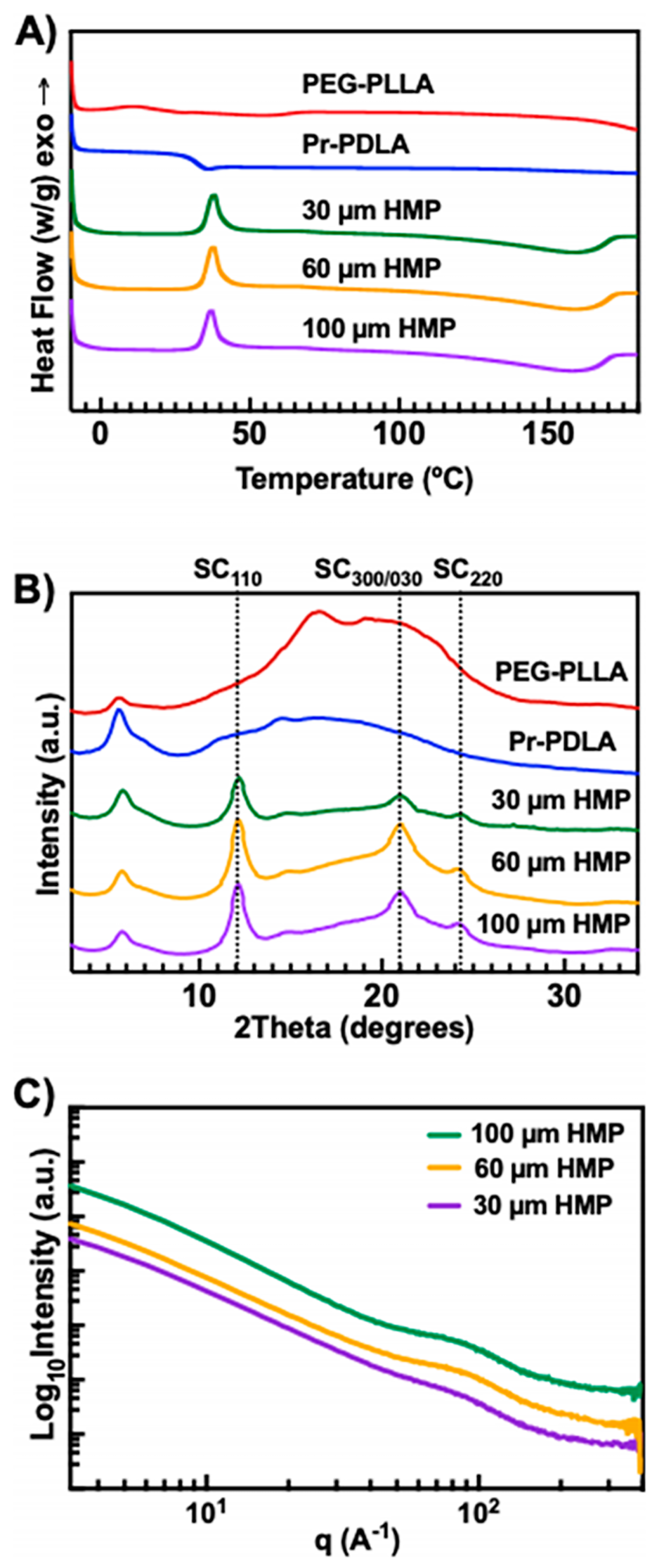
图4.SC-HMPs的热性能与散射分析:(a)DSC热谱显示SC-HMPs在37°C出现结晶放热峰;(b)WAXS谱中SC-HMPs在2θ=12.2°、21.2°、24.2°处显示立体复合PLA的特征衍射峰;(c)SAXS谱表明不同粒径SC-HMPs的网状结构孔径(7.9–9.1 nm)差异较小。
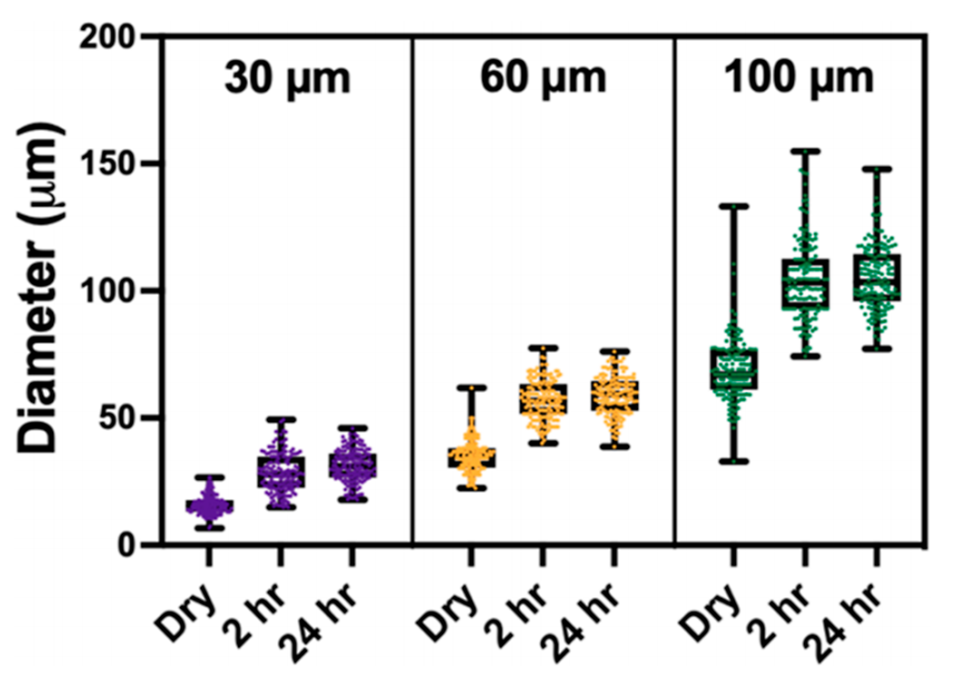
图5.SC-HMPs的溶胀行为:冻干后的微粒在37°C的1× PBS中孵育2小时和24小时后,小粒径微粒(33.7 μm)溶胀率可达77.0%,且所有微粒溶胀后形态恢复率超过90%。
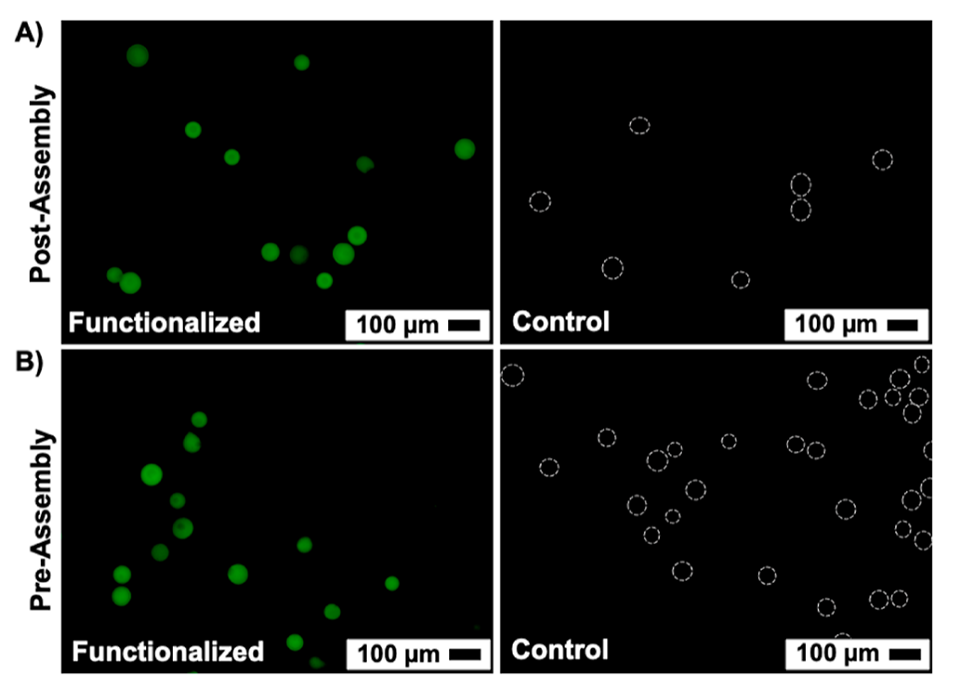
图6.荧光标记SC-HMPs:(a)通过UV/LAP光引发硫醇-炔点击反应实现FITC标记(绿色荧光),对照组无荧光;(b)苯基功能化SC-HMPs(Ph2-PDLA)与未修饰SC-HMPs(Pr-PDLA)的荧光对比。
论文链接:https://doi.org/10.1021/jacs.4c02317














