随着工业污染的加剧,水资源质量严重下降,废水中各种污染物对人类健康和生态环境构成了重大威胁。聚合物微球因其高吸附效率、优良的吸附性能和易于操作的特点,被认为是理想的吸附材料。

近期,浙江树人大学生物与环境工程学院陆胤教授等人发表综述,全面总结了聚合物微球的制备方法、改性技术及其在废水处理中的应用现状。相关研究成果以“Preparation and modification of polymer microspheres, application in wastewater treatment: A review”为题目,发表在期刊《Journal of Environmental Management》上。
本文要点:
1、综述了近年来聚合物微球的制备方法,包括分散聚合、乳液聚合、悬浮聚合等,并比较了各种方法的优缺点。
2、介绍了对聚合物微球进行表面改性的方法,如引入氨基、羧基等官能团,以及使用各种修饰剂对微球的性质进行调控。
3、详细阐述了聚合物微球在废水处理中的应用,包括去除氮、磷、重金属、有机染料等污染物,并分析了其吸附性能和机理。
4、总结了聚合物微球在废水处理中的优势,如易分离回收、高吸附容量等,并指出了未来的研究方向,如进一步提高磁性分离性能、开发低成本复合微球等。
一张图读懂全文:
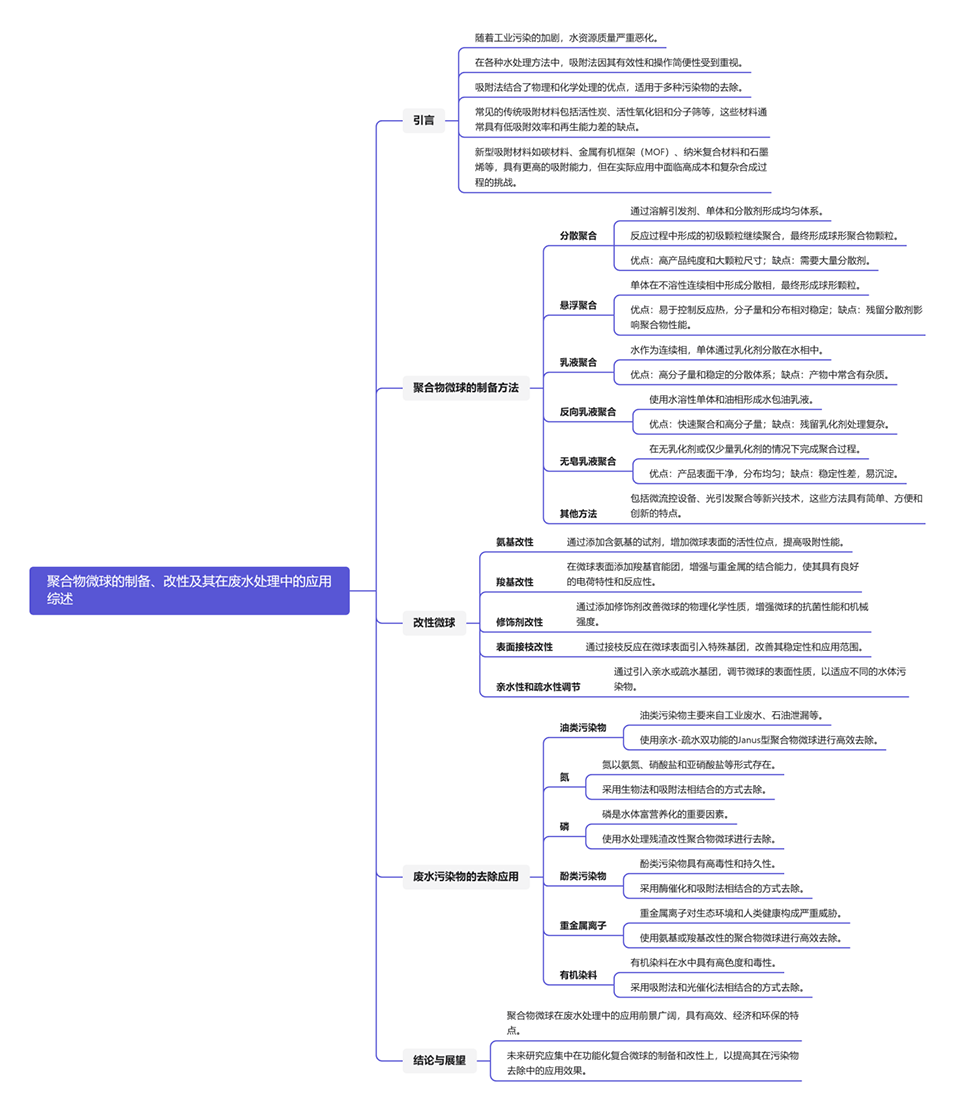
使用聚合物微球作为吸附剂进行废水处理的主要优势如下:
1、高吸附效率:得益于其高比表面积和可调节的表面性质,聚合物微球对有机染料、重金属、磷酸盐、氮化合物等各类污染物均表现出高吸附容量。
2、易于处理和分离:聚合物微球易于操作,可通过磁分离等方式快速从处理水中分离回收,便于后续处理。
3、可循环利用:许多聚合物微球可以进行再生和重复利用,减少了废弃物产生,提高了成本效益。
4、多功能性:聚合物微球可以通过改性和复合等方式针对特定污染物进行优化设计,拓展了其应用范围。
5、环境友好性:聚合物微球通常无毒、可生物降解,不会造成二次污染,是一种环境可持续的吸附材料。
6、稳定性:聚合物微球具有良好的化学、热和机械稳定性,能够承受恶劣的废水环境。
综上所述,聚合物微球作为吸附剂具有高吸附能力、易分离回收、可重复利用、多功能性和环境友好等优势,是一种高效、经济和环保的废水处理技术。
聚合物微球的改性如何提高其在废水处理中的性能?
1、提高吸附效率:通过改性,如引入氨基或羧基官能团,聚合物微球的吸附效率得到显著提升。
2、增强热稳定性:改性后的聚合物微球在高温条件下仍能保持稳定性,适用于更广泛的工业应用。
3、改善物理化学性质:改性后的聚合物微球在物理和化学性质上得到改善,如增强的机械强度和化学稳定性。
4、提高再生能力:改性后的聚合物微球更易于再生,提高了其循环使用的可能性和经济性。
5、增强选择性:通过分子印迹等技术,改性后的聚合物微球对特定污染物的选择性吸附能力得到增强。
6、改善分离性能:特别是磁性改性后的聚合物微球,能够通过磁场辅助快速分离,提高了处理效率。
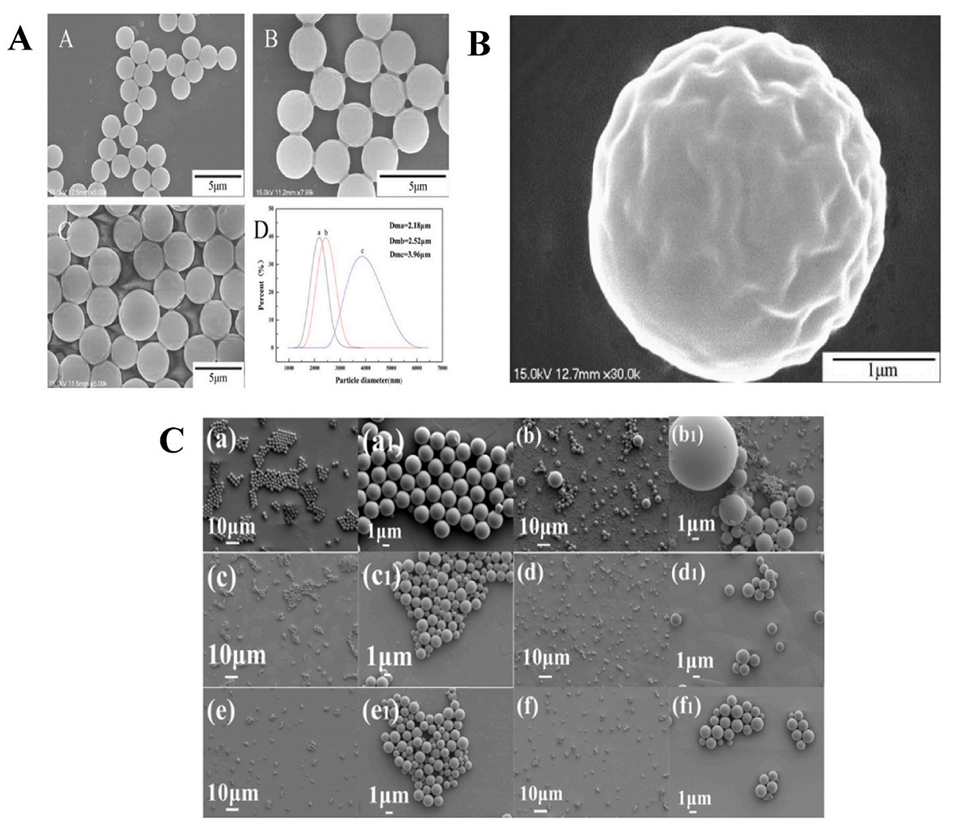
图1.(a)DVB含量为0mL(A)、10mL(B)和20mL(C)制备的PGMA-DVB微球的SEM图像和粒度分布(D)。(b)李子状PGMA-DVB微球的SEM图像。(c)PS/CuO@CLDH微球形成过程示意图。
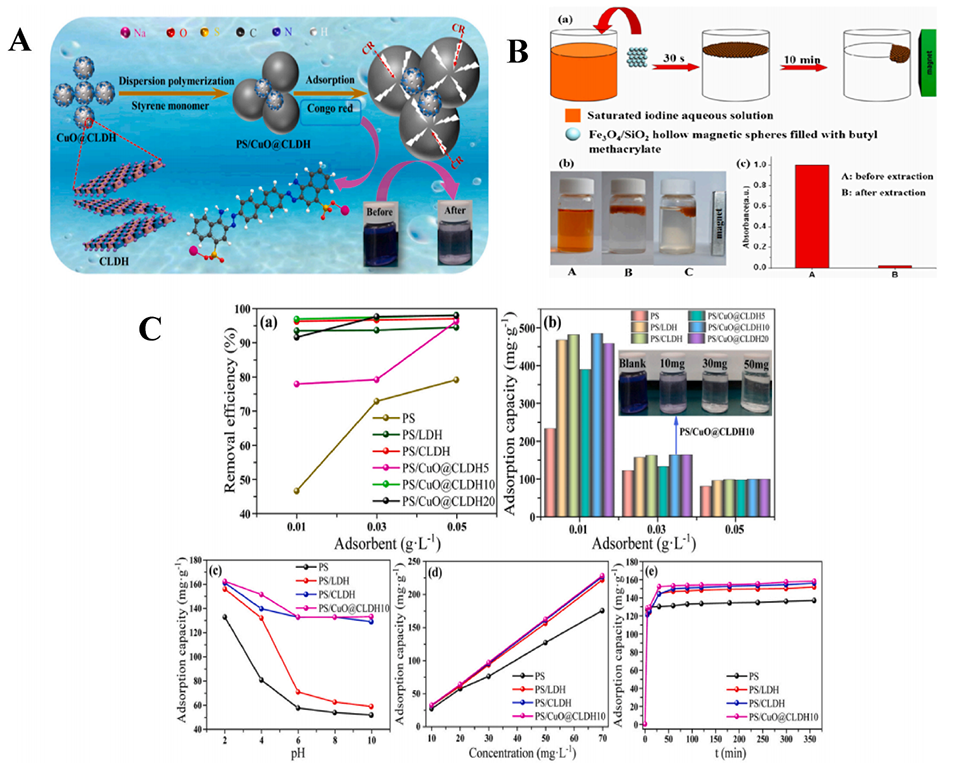
图2.(A)PS/CuO@CLDH微球形成过程示意图。(B)Fe3O4 NPs/SiO2核壳空心微球在解毒提取和快速废物去除中的应用:a提取和去除过程的示意图;b分别为提取前(A)、提取后(B)和外部磁力去除后(C)的碘溶液照片;c添加微球前后在365nm处收集的碘水溶液的紫外吸收。(C)复合材料的吸附性能:吸附剂对(a)去除效率、(b)吸附容量、(C)pH值、(d)初始浓度和(e)接触时间的影响。
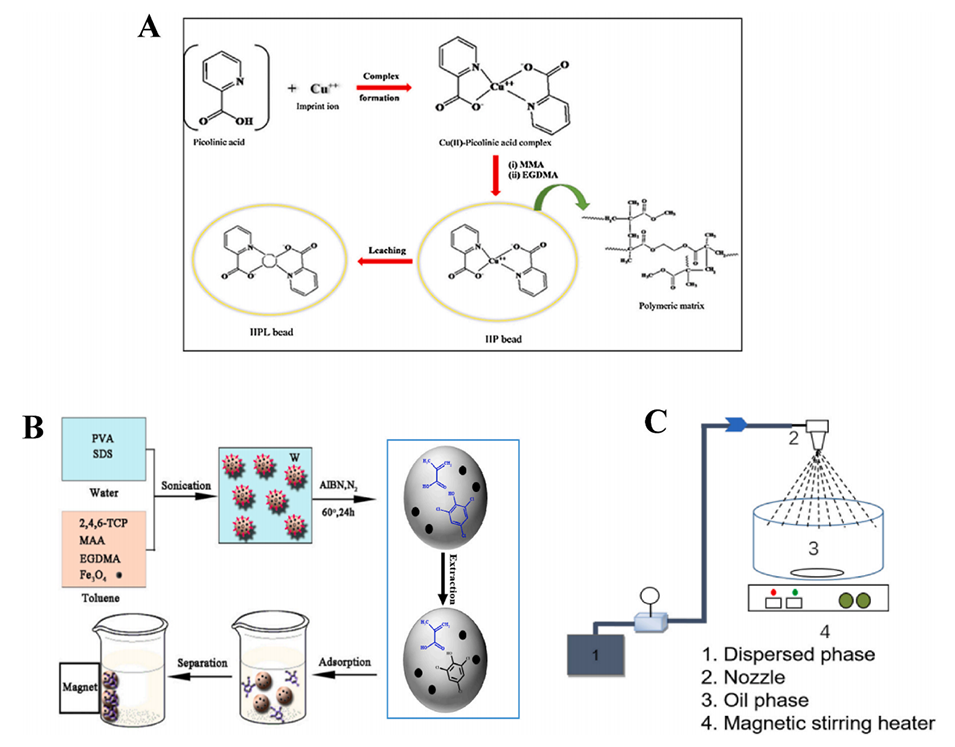
图3.(A)IIP制备示意图。(B)悬浮聚合制备磁性分子印迹聚合物的路线示意图。(C)改性悬浮聚合装置示意图。

图4.(A)(a)IIP珠的SEM图像,(b-c)IIP的低倍和高倍放大。(B)不同SiO2含量下高吸水性聚合物的SEM:a,溶液聚合制备SAP;b-f,SiO2含量为0%、0.5%、1.0%、1.5%、2.0%下的改性悬浮聚合。
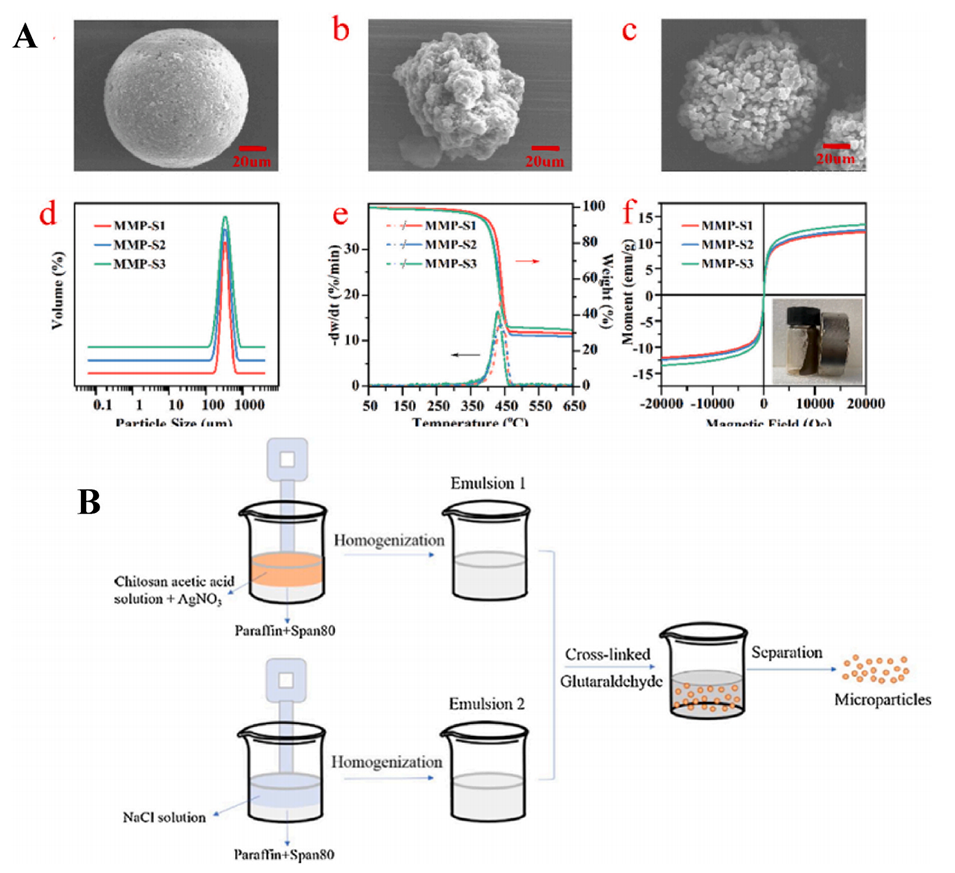
图5.(A)PS@Fe3O4的表征:MMP-S1的SEM(a),MMP-S2的SEM(b),MMP-S3的SEM(c);DLS光谱(d);TGA曲线(e);磁化曲线(f)。(B)AgCl@CM微球制备示意图。
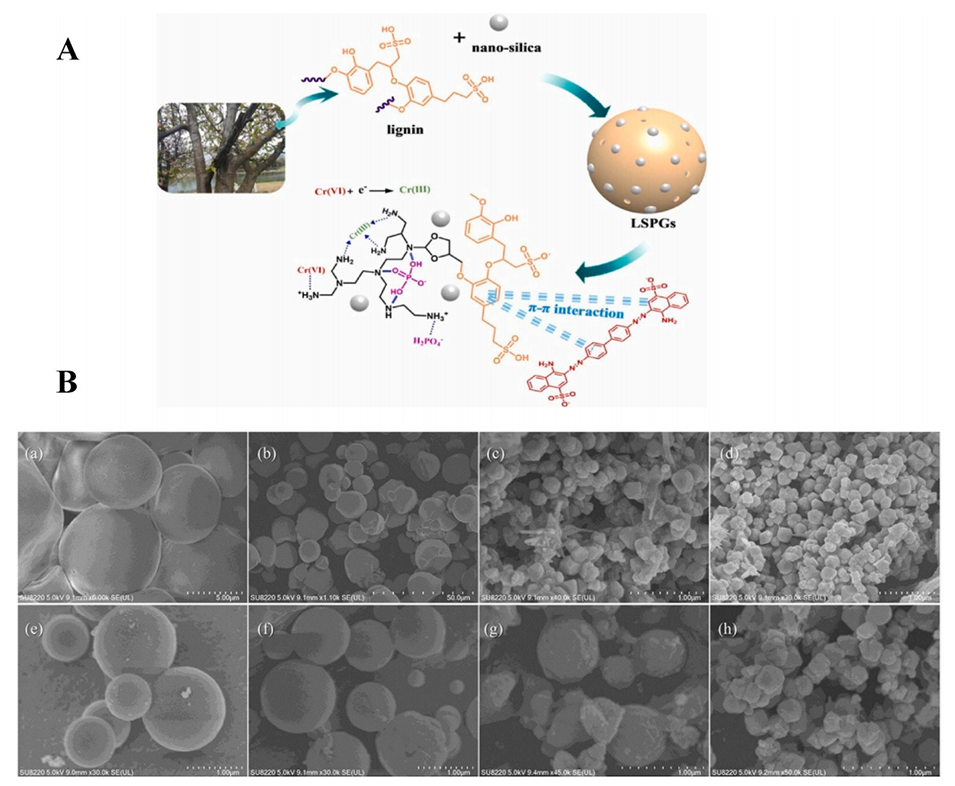
图6.(A)木质素基复合微球LSPGs的制备。(B)木薯淀粉(a)、MS(b)、AAM-MSM(不添加MMA)(c,d)、AAM-MSM(添加MMA)(e,f)、吸附Cd(II)的AAM-MSM(g,h)的SEM图像。
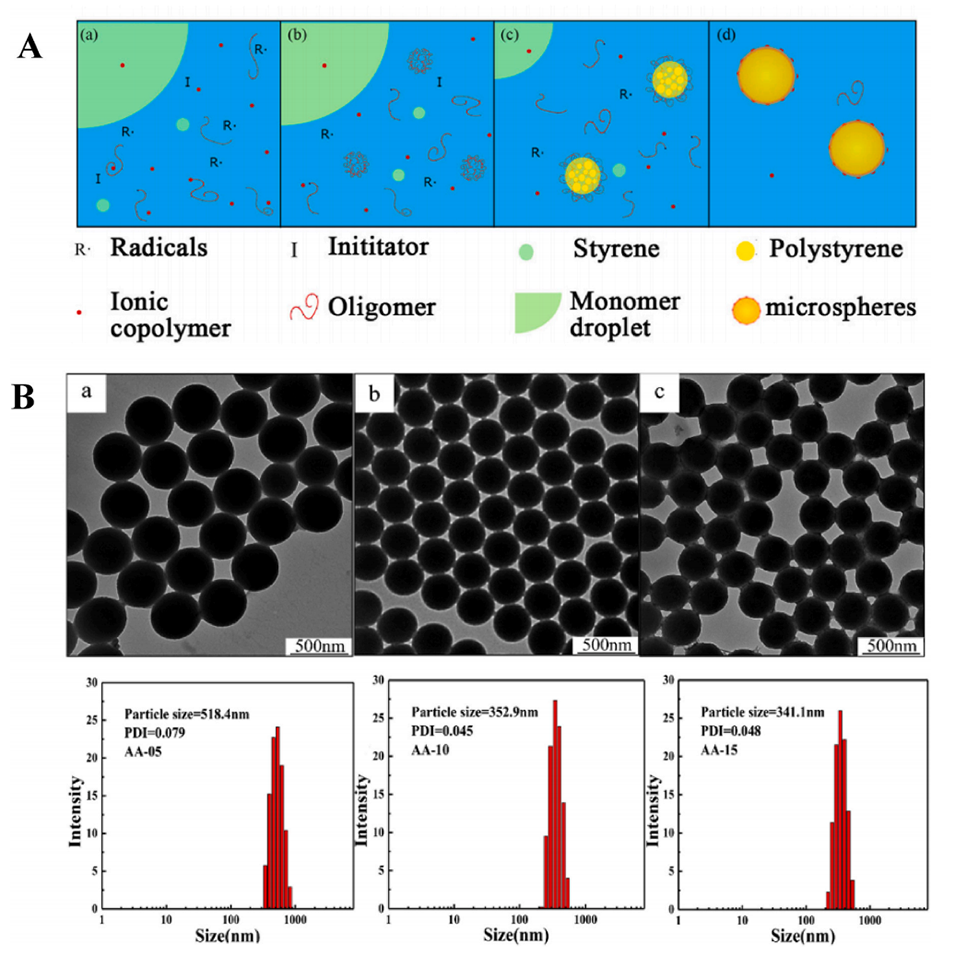
图7.(A)亲水共聚单体存在下超临界流体萃取机理的简化示意图。(B)不同AA含量的P(St-co-AA)共聚物的图像及其相应的直方图。(a)5mol%AA,(b)10mol%AA和(c)15mol%AA。
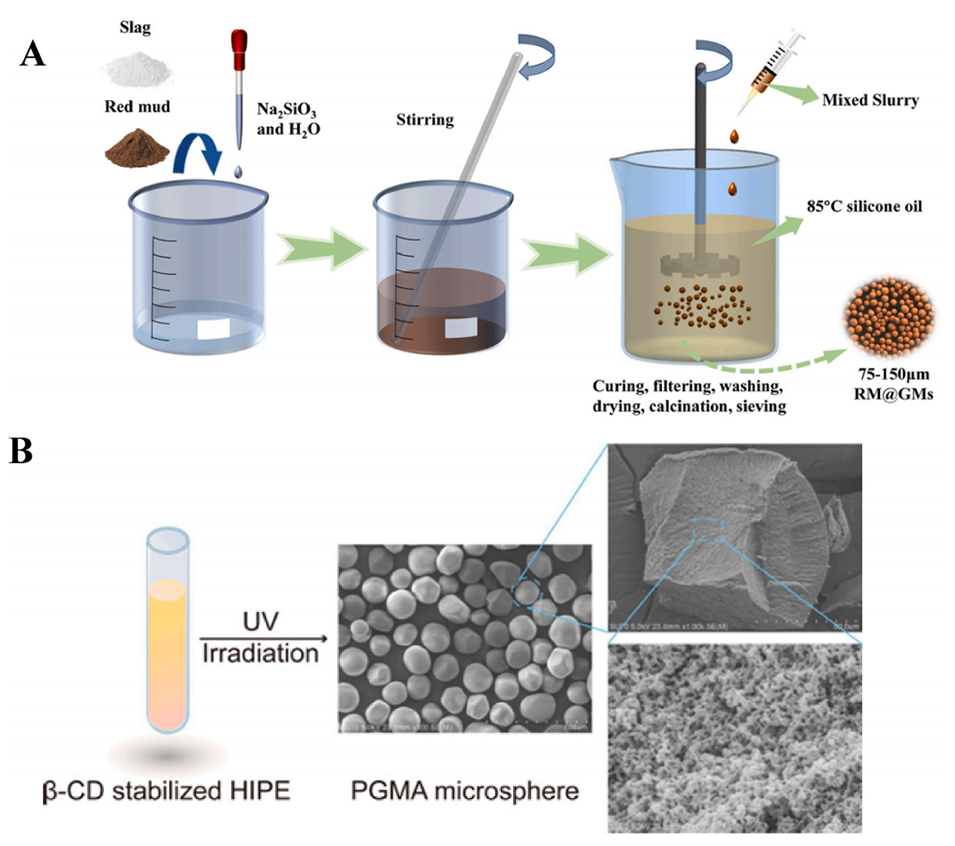
图8.(A)RM@GMs制备流程图。(B)光引发剂引发聚合反应形成PGMA微球的示意图。
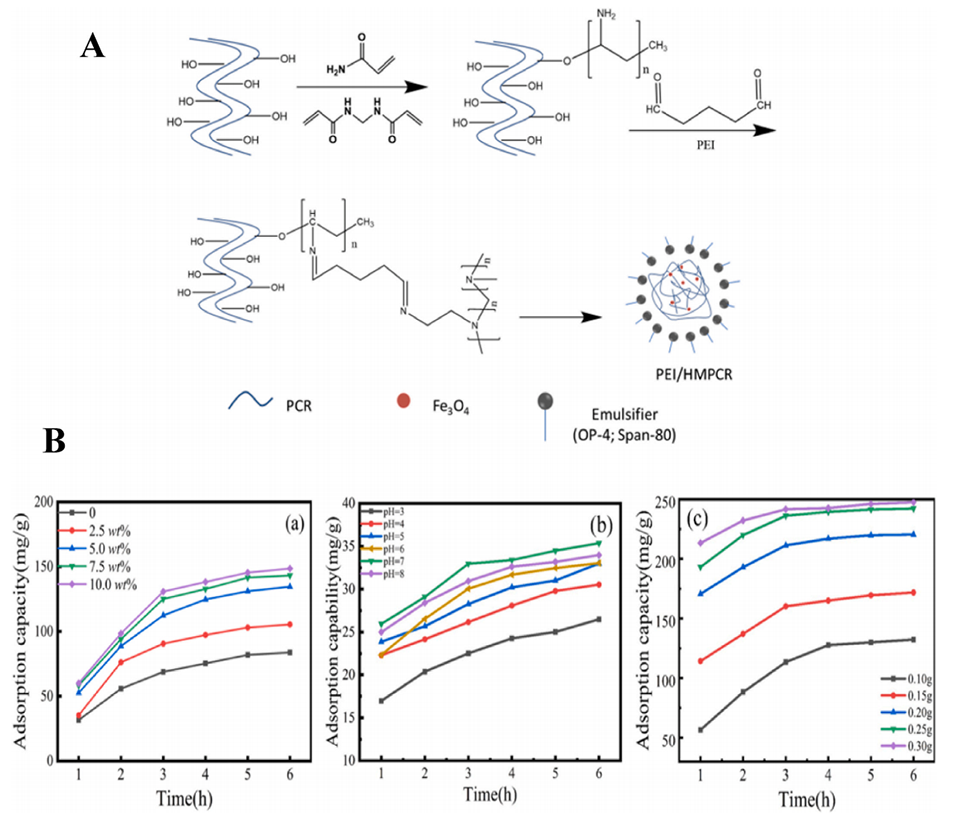
图9.(A)PEI/HMPCR合成示意图。(B)PEI量(a)(25℃,pH=7,初始浓度250mg/L,PEG2000量为20.0wt%)、溶液pH值(b)(25℃,PEI量为5.0wt%,初始浓度为50mg/L,PEG2000量为20.0wt%),以及PEI/HMPCR吸附剂量(c)(25℃,PEI量为5.0wt%,pH=7,初始浓度为250mg/L,PEG2000量为20.0wt%)对Cd(II)吸附容量的影响。
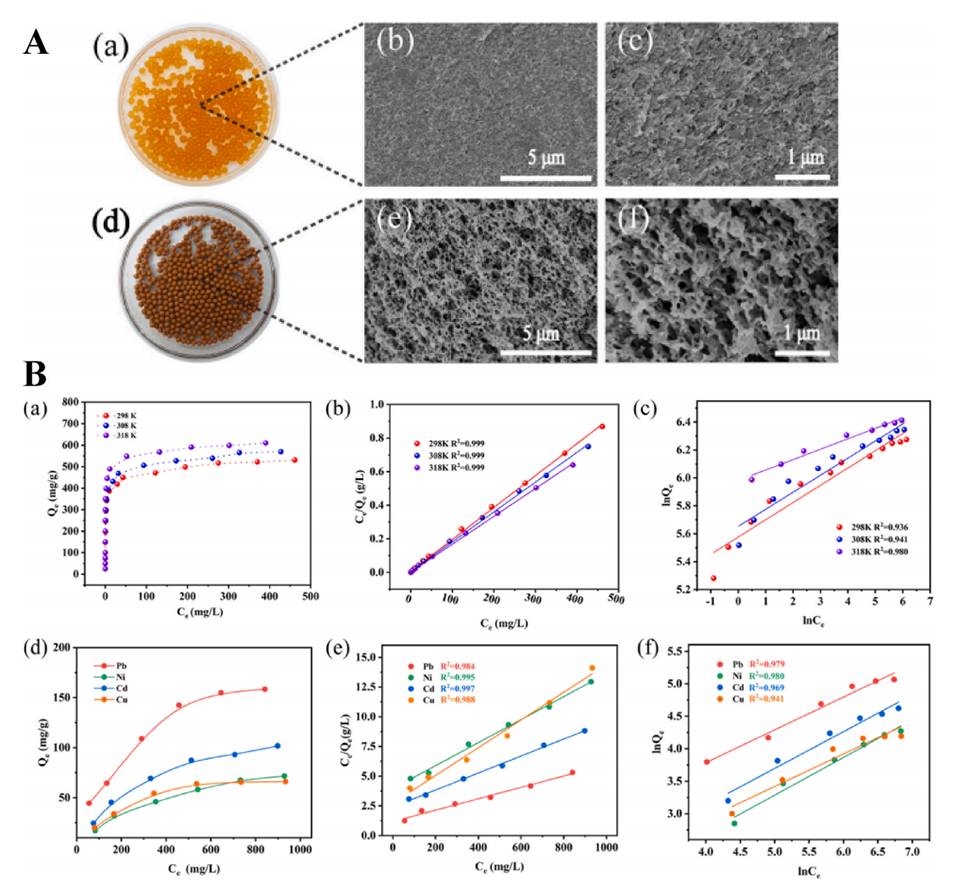
图10.(A)CSFe(a)和CS-Fe@PEI(d)的照片。CS-Fe(b,c)和CS-Fe@PEI(e,f)的SEM图像。(B)CS-Fe@PEI在298、308和318K下对Cr(VI)的吸附等温线(a)、Langmuir等温线(b)和Freundlich等温线(c)。CS-Fe@PEI在298K(d)下对Cu(T)、Cd(II)、Ni(I)和Pb(II)的吸附等温线、Langmuir等温线(e)和Freundlich等温线(f)。
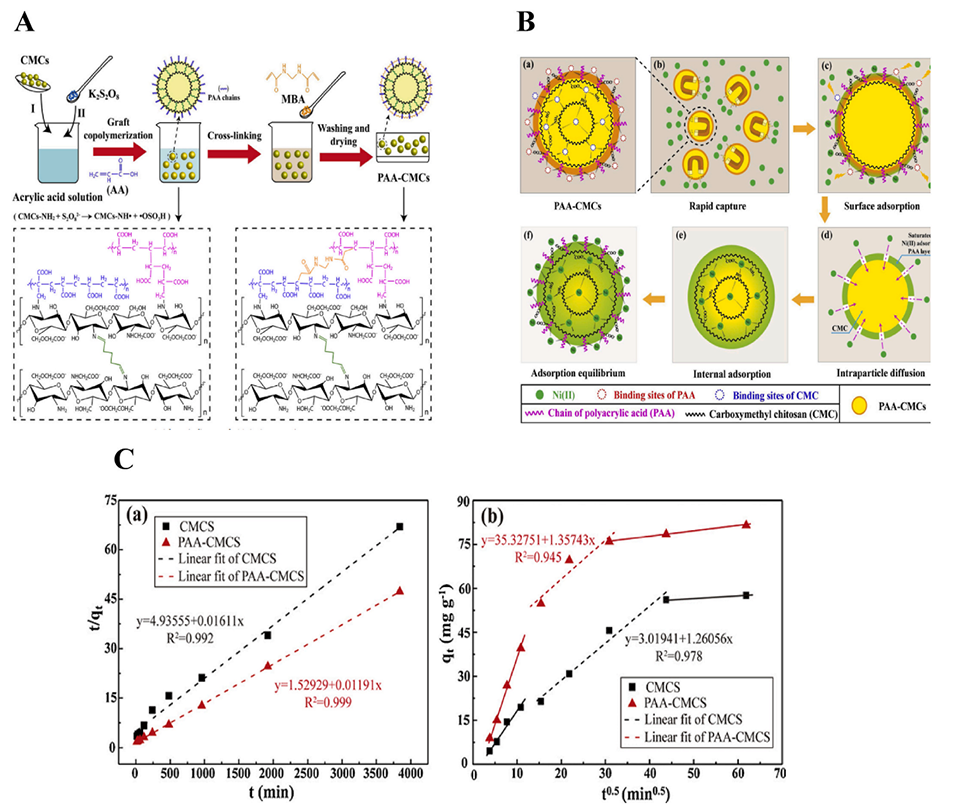
图11.(A)PAA-CMCs制备示意图。(B)吸附机理示意图。(C)(a)伪二阶模型的线性拟合曲线;(b)颗粒内扩散模型(Ni(II)溶液=50mL,Ni(II)浓度=150mg/L,T=298K,吸附剂用量=0.05g)。
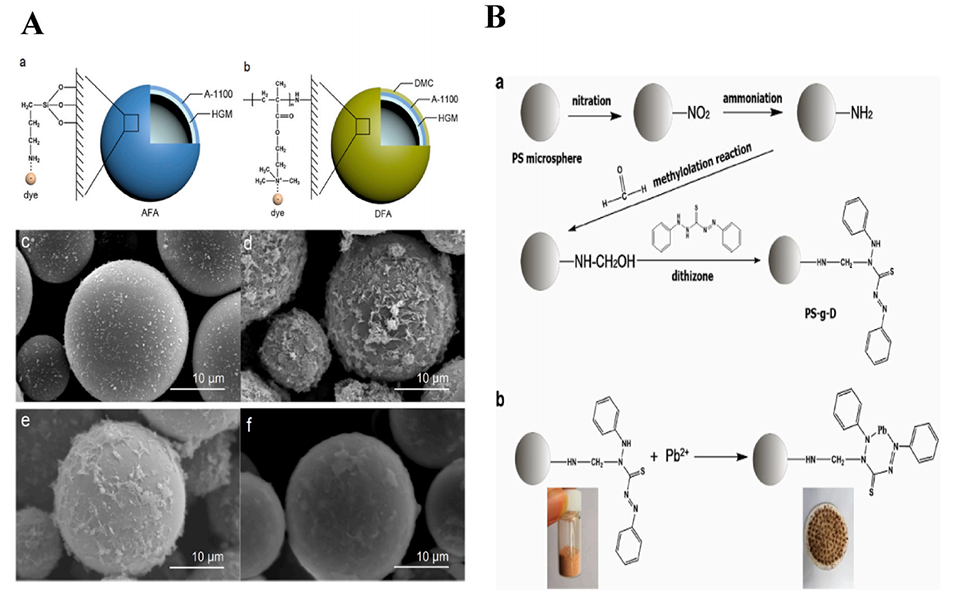
图12.(A)AFA(a)和DFA(b)表面物质的结构图和化学式;HGM(c)、PHGM(d)、AFA(e)和DFA(f)的SEM图像。(B)双硫腙接枝聚苯乙烯微球的制备与吸附,(a)合成路线,(B)Pb2+螯合。
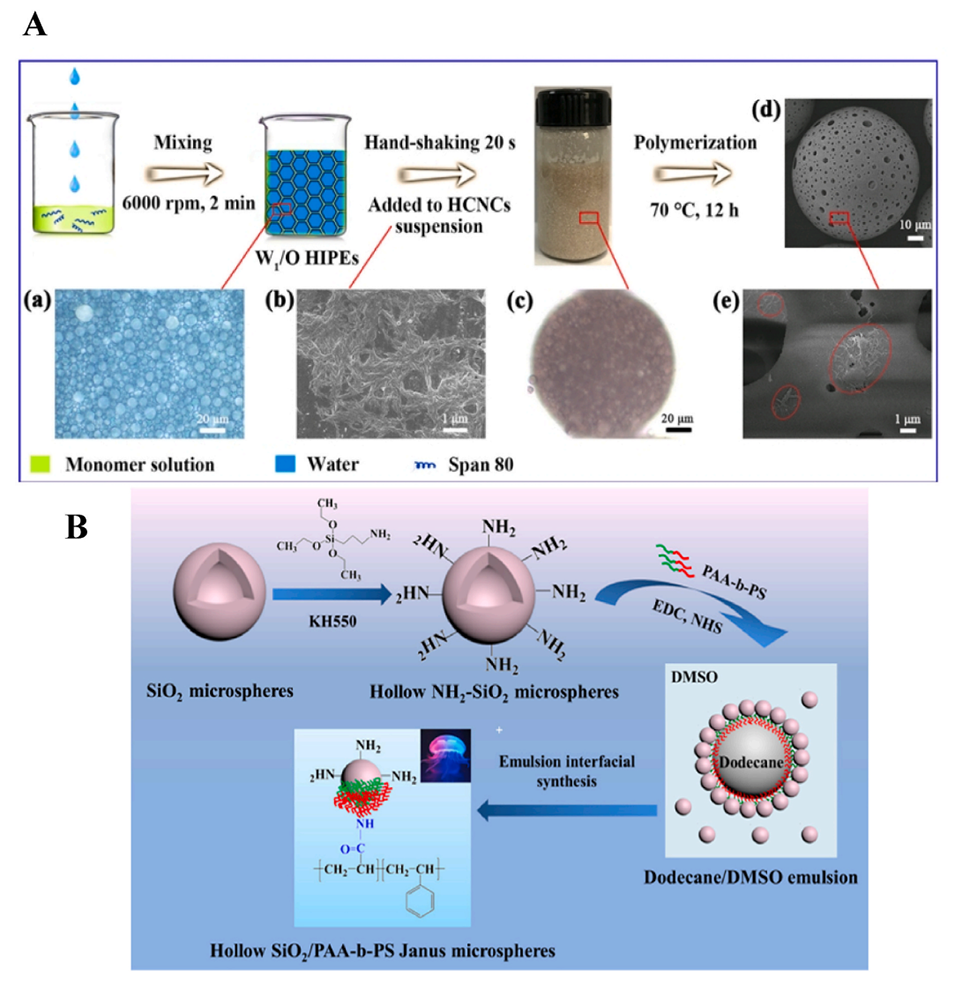
图13.(A)HPHs合成过程示意图。(a)原始W1的光学显微照片,W1/O/W2/O HIPE(水染成蓝色)的光学显微图。(b)HCNCs的SEM图像。(c)双重Pickering乳液(内部水相染成红色)。(d-e)HPHs的SEM图像,(e)中的圆圈显示了嵌入HPHs表面的HCNCs。(B)空心SiO2/PAA-b-PS Janus微球的制备示意图。
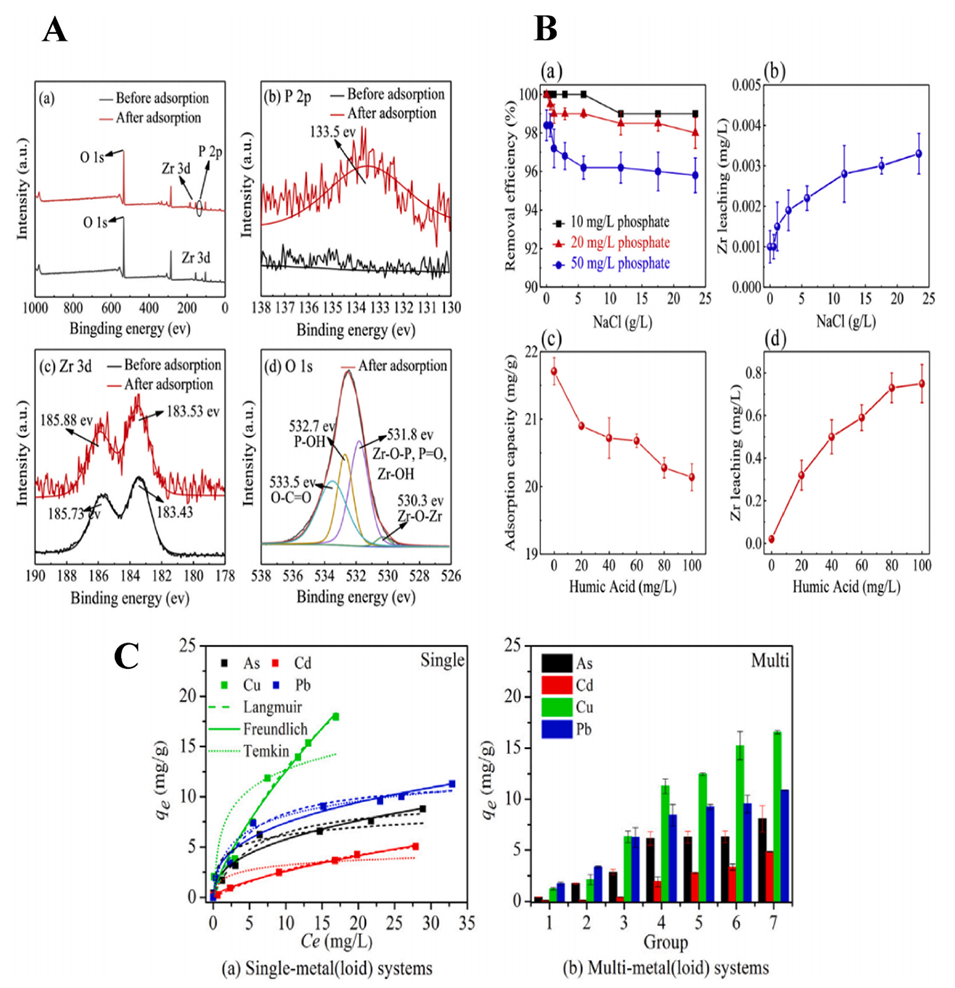
图14.(A)NH-SA-ZrBT在磷酸盐吸附前后的XPS分析:(a)宽扫描光谱;(b)P2p;(c)Zr3d;(d)O1s。(B)NaCl和HA对磷酸盐吸附性能的影响(磷酸盐浓度:40mg/L;溶液体积:40mL;珠粒数:20;接触时间:48h):(a)不同NaCl浓度下的磷酸盐去除效率和(b)Zr离子浸出;(c)吸附容量和(d)不同HA浓度下Zr离子的浸出。(C)在单金属(loid)体系和多金属(loil)体系中,初始浓度对CPM上As(III)和重金属吸附容量的影响。(Ce:初始浓度,mg/L;条件:pH=5.0;接触时间8h;吸附剂剂量2.4g/L;温度25℃)。
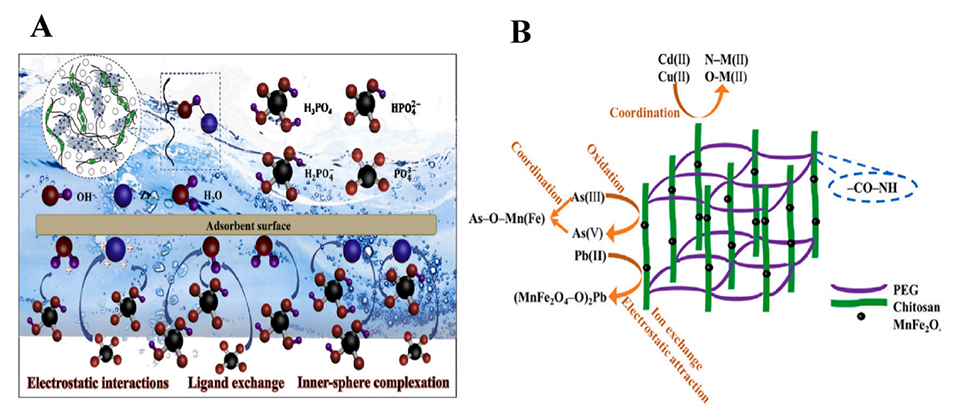
图15.(A)NH-SA-ZrBT吸附磷酸盐的可能机制。(B)CPM对As(III)和重金属的吸附机理。
论文链接:
https://doi.org/10.1016/j.jenvman.2024.121807














