
导读:
近期,湖南工业大学包装与材料工程学院陈一教授团队利用微流控技术制备了多孔海藻酸钠/纤维素纳米纤维(SA/CNF)复合水凝胶微球,通过引入CNF增强机械性能、聚乙二醇(PEG)提高孔隙率,旨在高效去除废水中的重金属离子(如Pb2+、Cu2+和Cd2+),并探讨了影响吸附过程的多种因素。相关研究以“Porous sodium alginate/cellulose nanofiber composite hydrogel microspheres for heavy metal removal in wastewater”为题目,发表在期刊《International Journal of Biological Macromolecules》上。
本文要点:
1、本研究采用微流控技术将海藻酸钠与纤维素纳米纤维复合,并添加聚乙二醇(PEG)作为造孔剂,制备了多孔海藻酸钠/纤维素纳米纤维(SA/CNF)复合水凝胶微球,用于去除废水中的重金属离子。
2、研究表明,吸附过程主要受pH、温度、初始浓度、共存离子和水环境等因素影响,且符合Langmuir等温模型和准二级动力学模型,表明吸附以化学吸附为主。
3、根据Langmuir模型得到的Pb吸附容量在20℃时高达544.66 mg/g。
4、固定床柱吸附实验显示,所制备的SA/CNF微球在流动废水处理中性能优异,表明该水凝胶吸附剂在去除实际废水中的重金属方面具有良好的应用前景。
制备SA/CNF复合水凝胶微球所用的主要材料包括:
海藻酸钠(Sodium Alginate, SA):作为基础材料,分子量为20,000–50,000 g/mol,含有丰富的羟基和羧基官能团,具有良好的重金属亲和力。
纤维素纳米纤维(Cellulose Nanofiber, CNF):增强剂,直径为10–20 nm,长度为10–20 μm,羧酸基含量为1.24 mmol/g,用于提高机械强度和增加吸附位点。
聚乙二醇(Polyethylene Glycol, PEG-400):造孔剂,用于提高孔隙率和比表面积,进一步暴露更多的吸附位点。
液体石蜡(Liquid Paraffin):作为油相物质,生成水油乳液以形成微球结构。
氯化钙(CaCl2):用于交联水凝胶微球,形成稳定的三维网络结构。
辅助化学试剂:如异丙醇、无水乙醇和去离子水,用于清洗及制备过程中。
这些材料协同作用,赋予微球高吸附性和结构稳定性。
影响吸附过程的关键因素包括以下几方面:
1、pH值
溶液的pH值直接影响吸附剂的表面电荷及金属离子的存在形式。
在低pH值时,由于H+与Pb2+竞争吸附位点,吸附能力较低,而随着pH值升高至5,吸附能力显著增强;但在pH值超过6时,Pb(OH)2的沉淀会导致吸附效果下降。
2、温度
温度升高有利于提高吸附容量,表明该吸附过程放热反应。
3、初始金属离子浓度
在初始浓度100–300 mg/L范围内,吸附位点充足,吸附容量快速增加;当超过300 mg/L时,表面吸附位点逐渐饱和,内部结构的位点开始起作用,随后曲线趋于平缓。
4、共存离子影响
同时存在的其他重金属离子可能与目标离子竞争吸附位点。例如,Pb2+优先于Cu2+和Cd2+被吸附,这与金属离子的电负性和水合半径差异有关。
5、盐浓度
在2 mol/L NaCl环境下,吸附作用对Pb2+的去除率仍高达93.34%,表明微球具有优异的抗盐性能,不易受无机盐干扰。
这些因素共同决定了吸附效果及其在实际废水处理中的效率。

图1.(a)通过微流控技术制备的SC0.3-P4微球在湿润状态和干燥状态(插图)下的光学显微镜图像。(b)通过传统滴加法制备的SC0.3-P4微球在湿润状态下的光学显微镜图像(插图是干燥的SC0.3-P4微球照片)。(c)通过微流控技术制备的SA微球在干燥状态下的扫描电子显微镜(SEM)图像和光学显微镜图像(插图)。(d-i)不同CNF和PEG-400用量制备的SA/CNF微球的SEM图像,分别为SC0.1-P0、SC0.2-P0、SC0.3-P0、SC0.3-P1、SC0.3-P2和SC0.3-P4。
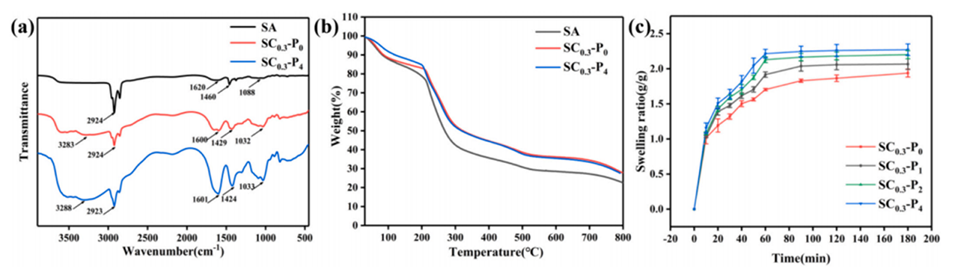
图2.(a)SA、SC0.3-P0和SC0.3-P4的FT-IR光谱及其(b)在N2中的TGA曲线。(c)用不同PEG-400剂量制备的SA/CNF微球的膨胀率随时间的变化。
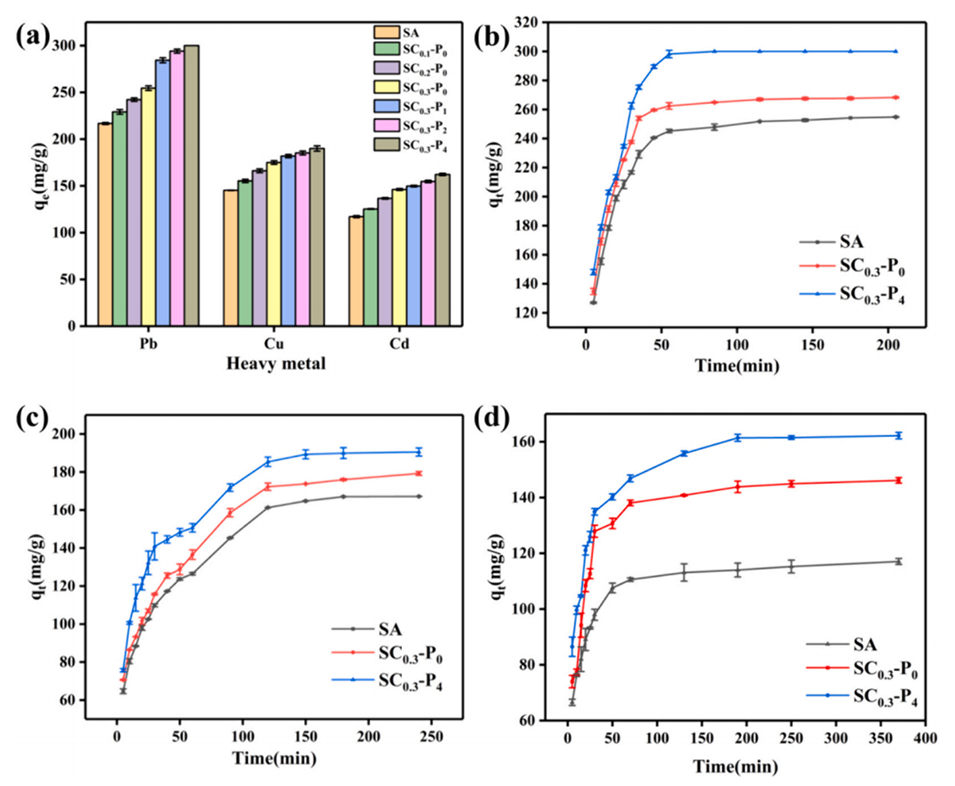
图3.(a)用不同CNF和PEG-400剂量制备的SCx-Py微球对Pb2+、Cu2+和Cd2+的吸附容量(pH=5,C0=300mg/L,25℃)。(b-d)SCx-Py微球从水溶液中吸附不同金属离子的动力学(pH=5,25℃):(b)Pb2+,(C)Cu2+和(d)Cd2+。
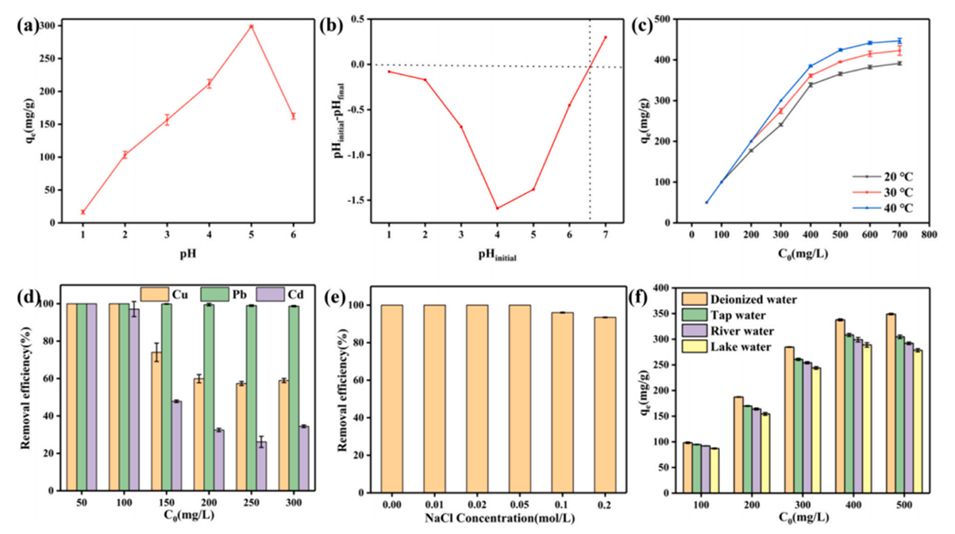
图4.(a-f)不同环境条件对SC0.3-P4微球吸附Pb2+的影响:(a)pH值(C0=300mg/L,25℃),(b)SC0.3-P4微球的pHPZC,(C)温度和初始浓度(pH=5),(d)共存离子(pH=5,25℃),(e)NaCl浓度(pH=5,C0=300mg/L,25℃)和(f)水生环境(pH=5.25℃)。
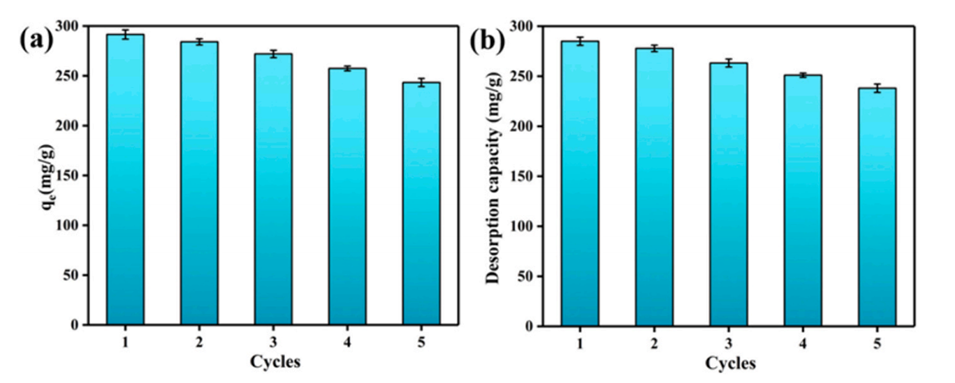
图5.(a)SC0.3-P4微球在五个连续的吸附/解吸循环中对Pb2+的吸附和(b)解吸。
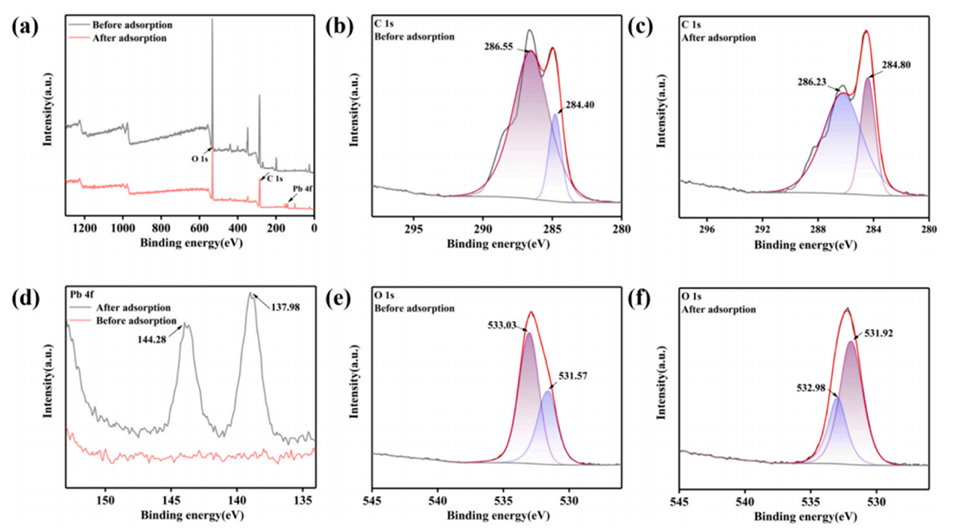
图6.(a)SC0.3-P4微球吸附前后的XPS光谱;SC0.3-P4微球(b)吸附前和(c)吸附后的C1s峰光谱;(d)SC0.3-P4微球吸附前后Pb4f峰光谱;SC0.3-P4微球(e)吸附前和(f)吸附后的O1s峰光谱。
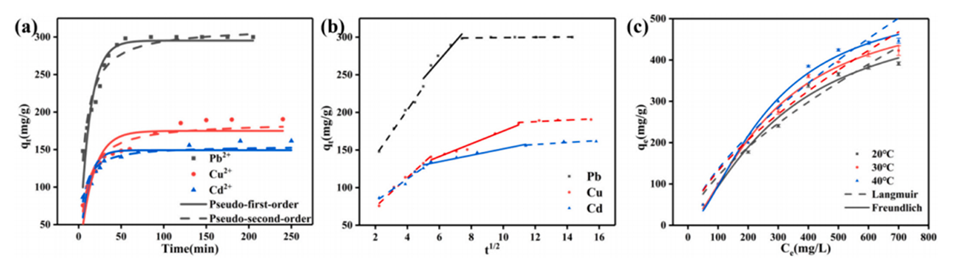
图7.(a)SC0.3-P4微球从水溶液中吸附Pb2+、Cu2+和Cd2+的吸附动力学曲线及拟合曲线和(b)颗粒内扩散曲线(pH=5,25℃)。(c)SC0.3-P4微球从水溶液中吸附Pb2+的等温线和拟合曲线(pH=5)。
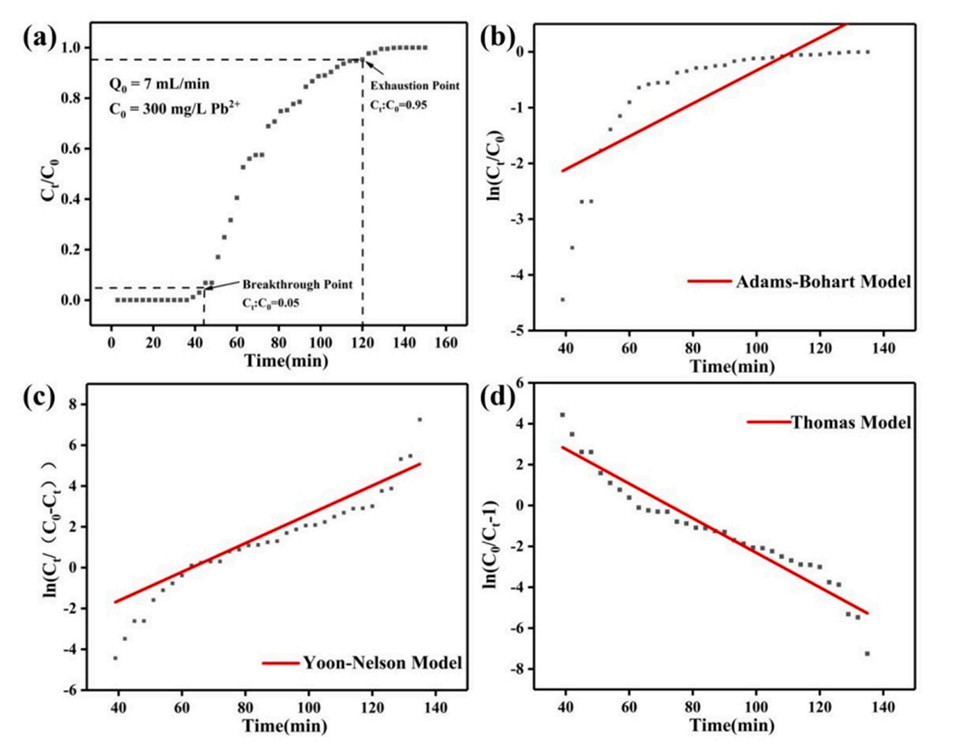
图8.(a)Pb2+通过填充有SC0.3-P4微球的吸附柱的穿透曲线。(b)Adams-Bohart模型拟合曲线。(c)Yoon-Nelson模型拟合曲线。(d)托马斯模型拟合曲线。C0和Ct分别是进水和出水浓度。
论文链接:https://doi.org/10.1016/j.ijbiomac.2024.135000














