由单甘油酯组成的抗菌脂质纳米颗粒为抑制膜包裹的病毒和细菌病原体提供了一种很有前途的策略。传统研究多采用长链单甘油酯(如甘油单油酸酯GMO),虽能形成稳定纳米颗粒但缺乏抗菌活性;而短链单甘油酯(如甘油单月桂酸酯GML)虽有强效抗菌性,却无法自组装成稳定结构且易因稀释失活。

为了克服这些限制并将抗菌单甘油酯掺入稳定的纳米颗粒构型中,本研究报道了一种无溶剂微流控制造策略,设计出具有膜破坏特性的单甘油酯基抗菌脂质纳米颗粒。该策略不需要使用挥发性有机溶剂(如乙醇),从而省略了后续的透析步骤。相关研究以“Solvent-Free Microfluidic Fabrication of Antimicrobial Lipid Nanoparticles”为题发表于期刊《ACS Applied Bio Materials》。
本文要点:
1、本研究开发了一种无溶剂微流控策略,通过混合不同单甘油酯制备兼具稳定性和抗菌活性的纳米颗粒。
2、与依赖于挥发性有机溶剂的传统微流体混合方法不同,该方法采用药用级材料,无需去除有机溶剂,从而省略了后续的透析步骤。
3、动态光散射(DLS)和ζ电位测量证实,所制备的纳米颗粒直径约为250-350 nm,具有较高的胶体稳定性,而纳米颗粒对金黄色葡萄球菌的抗菌活性在很大程度上取决于纳米颗粒的组成。
4、抗菌实验显示,纯甘油单油酸酯(GMO)纳米颗粒无活性,加入甘油单月桂酸酯(GML)后活性略有提升,而进一步引入少量甘油单山萮酸酯(GMB)或甘油二山萮酸酯(GDB)(<5 mol%)可使抗金黄色葡萄球菌活性增强270倍。
5、生物物理实验(耗散型石英晶体微天平QCM-D、电化学阻抗谱EIS)证实,高活性纳米颗粒能显著破坏膜结构,且破坏程度与抗菌效力呈正相关。
6、这一成果不仅展示了通过调整单甘油酯组合来优化抗菌脂质纳米颗粒性能的潜力,还为在生理相关pH条件下调节膜破坏特性提供了新思路。
纳米颗粒的制备过程详解:
1、材料准备
脂质相:将药用级单甘油酯(GMO、GML)及长链结构脂质(GMB或GDB)按特定摩尔比例混合(如GMO:GML:GMB为24.51:70.94:4.55),溶解于由中链单酸、双酸甘油酯(MCM)、丙二醇单辛酸酯(PG8)和丙二醇单月桂酸酯(PG12)组成的混合溶剂中,形成100 mg/mL的均质溶液。
水相:配制含1 mM脱氧胆酸钠(胆汁盐)的PBS缓冲液(pH 7.4),作为纳米颗粒的稳定剂。
2、微流控混合
使用Neonano微流控系统,通过精密泵控制两相流速:
脂质相与水相以1:9的体积比混合,总流速为10 mL/min。
两相在微米级通道中通过混沌混合(chaotic mixing)实现高效乳化,形成纳米级脂质乳滴。
3、温度控制
脂质相和水相在混合前均预热至40°C,确保脂质流动性并防止结晶,促进均匀分散。
4、纳米颗粒形成
混合后,脂质分子在水相中自组装成胶体稳定的纳米颗粒,分散于PBS中,最终浓度为10.4 mg/mL。
无需有机溶剂,因此省去传统方法中的透析或干燥步骤。
5、关键优化点
长链脂质比例:GMB或GDB的摩尔分数控制在<5%,以平衡纳米颗粒稳定性与抗菌活性。
稳定剂选择:脱氧胆酸钠通过静电排斥作用防止颗粒聚集,确保长期储存稳定性。
与传统方法的对比优势:
均一性:微流控技术实现精准流体控制,颗粒尺寸分布更窄(250–350 nm)。
稳定性:比均质化或超声法制备的颗粒更耐储存(实验显示尺寸稳定性更优)。
环保性:无挥发性溶剂(如乙醇),减少后续纯化步骤,符合绿色制药趋势。
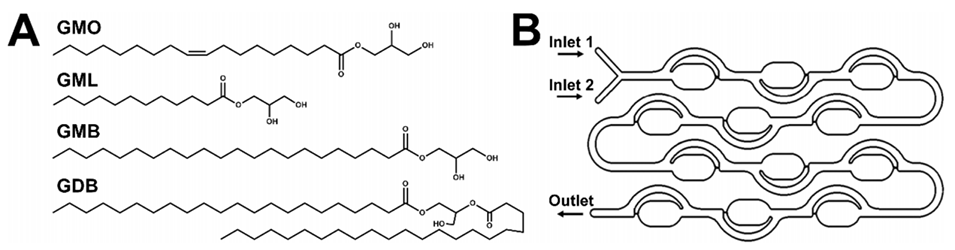
图1.制备抗菌脂质纳米颗粒的微流控制造策略。
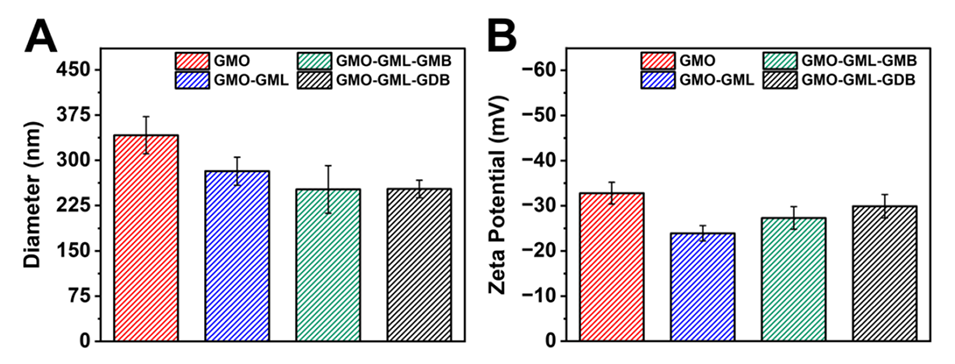
图2.纳米粒子尺寸和ζ电位表征。
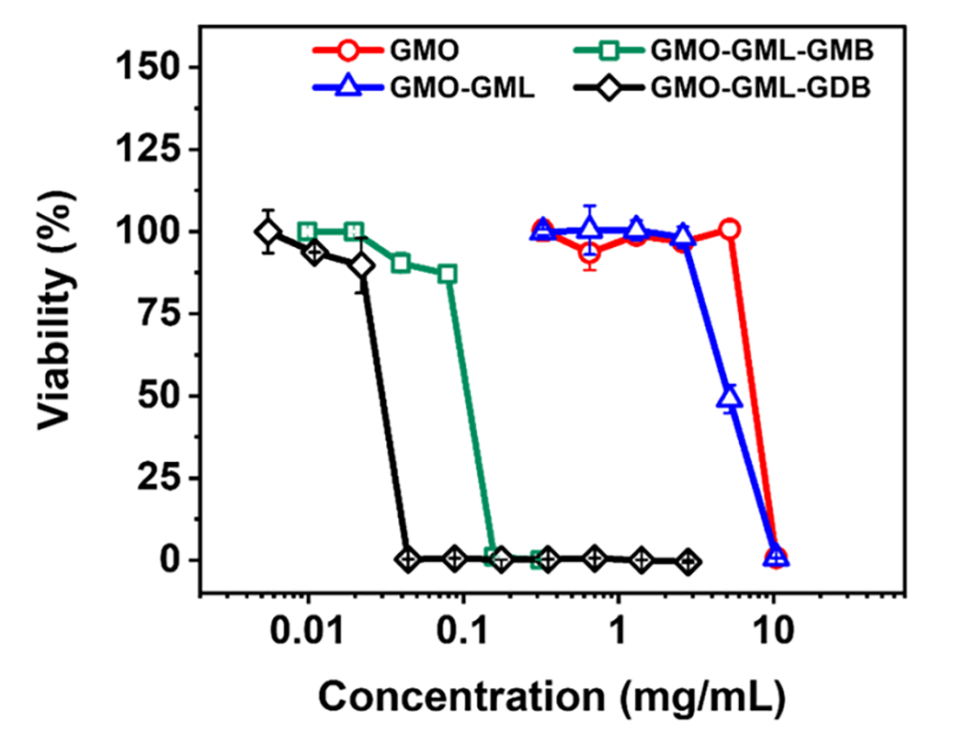
图3.脂质纳米颗粒抑制金黄色葡萄球菌生长的抗菌试验。
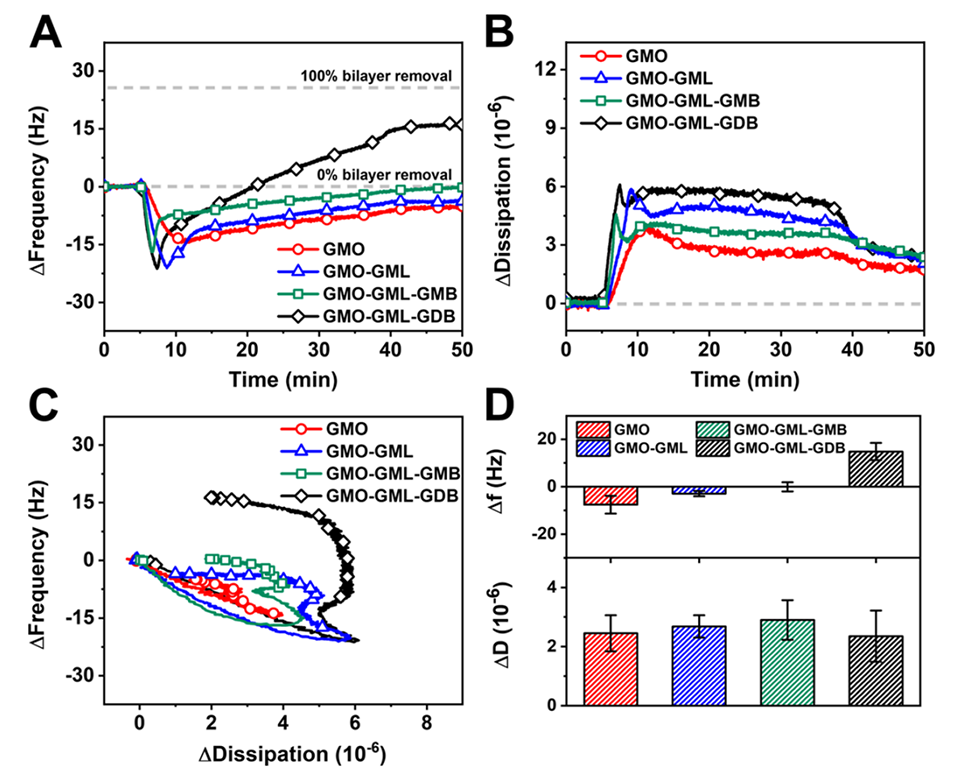
图4.纳米颗粒与负载型脂质双层平台相互作用的QCM-D表征。
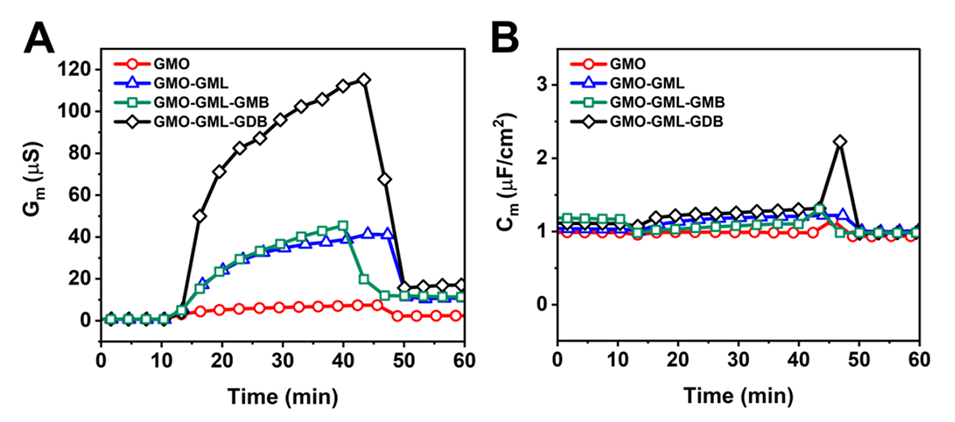
图5.纳米颗粒与锚定脂质双层平台相互作用的EIS表征。
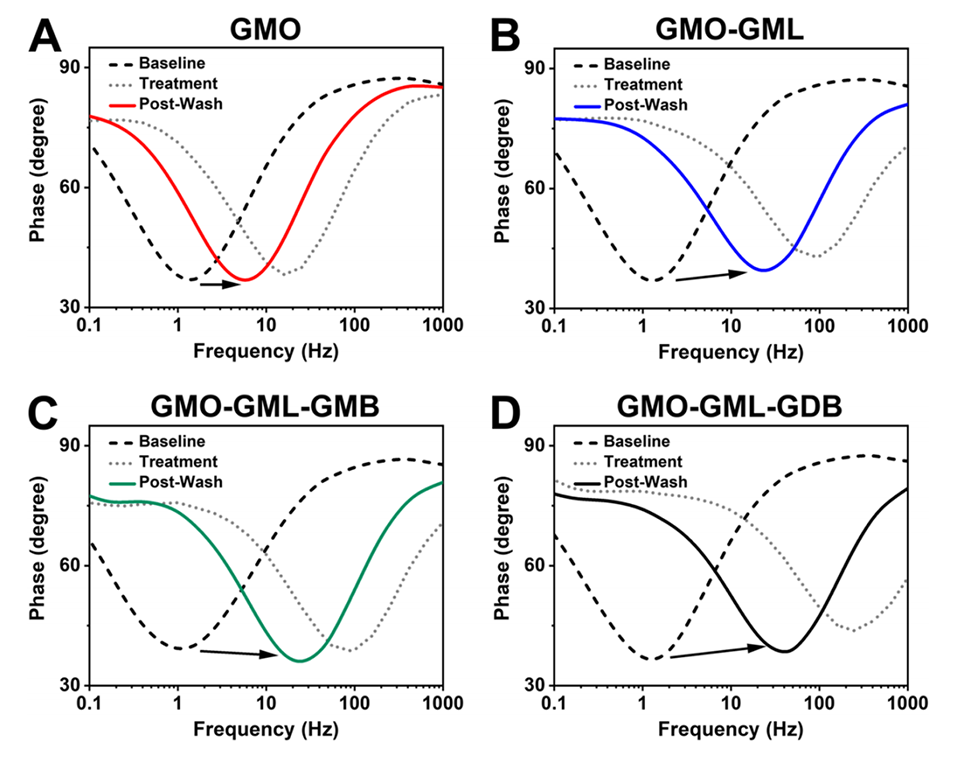
图6.纳米颗粒与锚定脂质双层相互作用的Bode图分析。提供了(A)GMO,(B)GMO−GML,(C)GMO−GML−GMB,以及(D)GMO−GML−GDB纳米颗粒的数据。基线指的是纳米颗粒添加前的tBLM,而处理和洗涤后分别指在纳米颗粒相互作用期间和缓冲洗涤后。
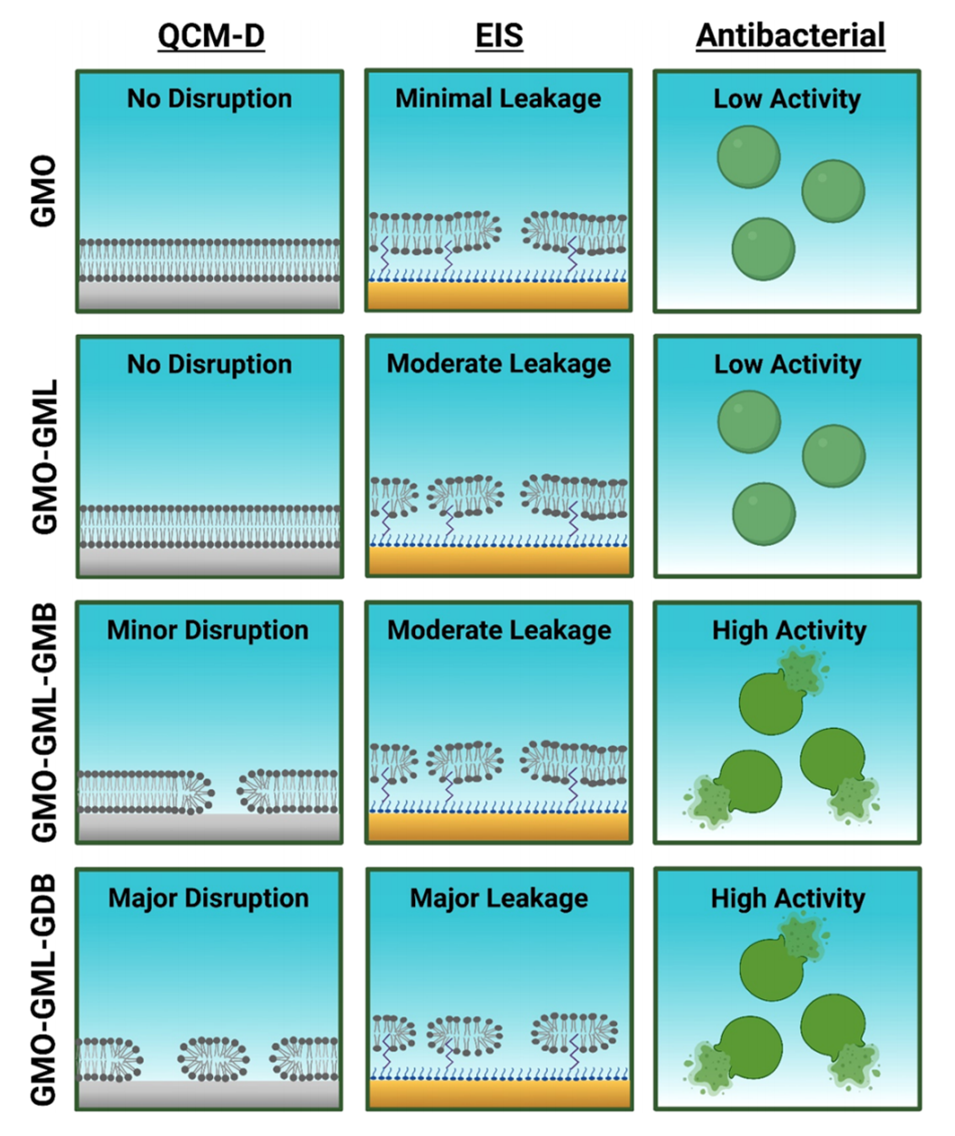
图7.不同纳米粒子组成的实验观察示意图总结。GMO和GMO-GML纳米颗粒的活性较低,而GMO−GML−GMB和GMO−GML−GDB纳米颗粒的活性水平较高,这与更广泛的膜破坏特性和抗菌活性有关。
论文链接:https://doi.org/10.1021/acsabm.4c01747














