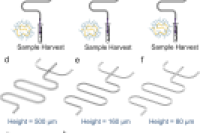
基因治疗通过外源性核酸调控基因表达,核酸的易降解性要求高效递送载体,脂质纳米颗粒(LNPs)和聚合物纳米颗粒(PNPs)是主流方向,其中PNPs具备化学稳定、热耐受性好、储存条件温和、可功能化修饰的优势,是LNPs的理想替代。
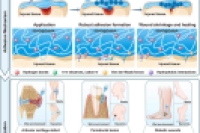
临床治疗中,牙周炎骨缺损、关节软骨损伤、糖尿病皮肤溃疡等湿组织缺损修复,一直是再生医学的棘手问题 —— 动态富液环境下生物支架黏附不稳,易被唾液、滑液、伤口渗出液冲脱,药物和细胞递送效率大打折扣,最终影响组织修复效果。
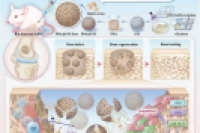
该研究开发了一种由仿生预处理骨髓间充质干细胞外泌体(BioPre-Exos)与聚多巴胺修饰的可注射多孔甲基丙烯酰化明胶(GelMA)微球(PDA@GM)组成的协同骨再生体系,旨在解决临界尺寸骨缺损修复中内源性自愈能力不足、外泌体生物活性低且递送效率差的临床难题。
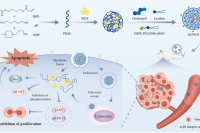
该研究构建了一种脂质杂化纳米粒(SLHN)递送系统,用于靶向输送SH2超亲体蛋白(SH2S)治疗乳腺癌,显著提升其体内稳定性、肿瘤靶向性与治疗效果。
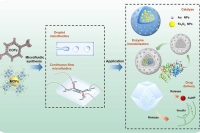
重点阐述了依托微流控技术实现MOFs/COFs精准制备与结构定制的突破性进展。
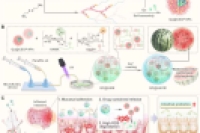
开发了一种名为QC@HACM的创新型“西瓜样”微/纳复合递药系统,旨在通过多维度干预策略实现溃疡性结肠炎(UC)的高效治疗。
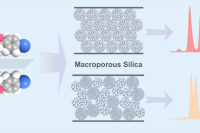
多糖功能化大孔二氧化硅微球是高效液相色谱中应用最广泛的手性固定相之一。
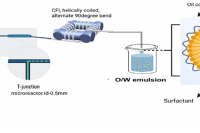
以微流控技术为核心,开发出适用于航天领域的壳聚糖包覆褪黑素载药水包油纳米乳剂,成功解决了液态药物在太空模拟环境中的稳定性难题,同时实现了药物的可控缓释,为航天制药的研发提供了全新的微流控解决方案,也为极端地面环境的药物制备拓宽了思路。
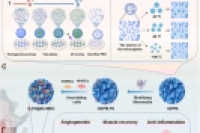
本研究开发了一种仿生分级多孔微球(GEPM-FN),该微球不仅支持高质量的细胞培养与扩增,还可作为重症肢体缺血(CLI)治疗的递送载体。

该研究开发了一种pH响应性益生菌-益生元层级微球(MicroSym),旨在通过重塑肠道菌群、调控免疫代谢来治疗肥胖相关免疫代谢疾病,解决传统益生菌/益生元疗法胃部存活率低、肠道递送效率不足等关键问题。
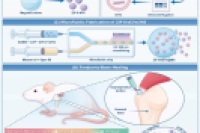
该研究研发了一种载有ZIF-8纳米颗粒和骨髓间充质干细胞来源小细胞外囊泡(BMSC-sEVs)的GelMA水凝胶微球复合体系(ZIF-8/sEVs@MS),通过协同调控免疫微环境、促进组织特异性分化,实现腱-骨的功能性愈合。
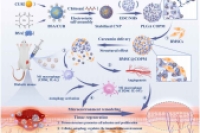
本研究通过气体辅助挥发微乳液技术结合表面碱处理,设计合成了开放多孔聚乳酸-羟基乙酸共聚物(PLGA)微球,将姜黄素与牛血清白蛋白(BSA)制备为纳米颗粒并接枝于微球,同时负载骨髓间充质干细胞(BMSCs)构建出BMSC@COPM复合体系。
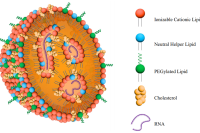
本文阐述了载核酸脂质纳米颗粒的研究现状,重点介绍其常用配方体系与微流控制备方法。
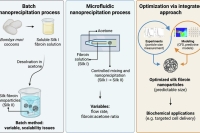
丝素蛋白因具备良好的生物相容性、稳定性,且可通过溶剂诱导自组装形成纳米颗粒,成为极具吸引力的药物递送载体材料。微流控纳米沉淀法相较批次制备法,能实现更优的工艺控制与重复性,但由于流体动力学、溶剂交换及丝素蛋白自组装过程之间存在紧密耦合,难以实现该方法的合理工艺优化,也对纳米颗粒的形成造成了阻碍。
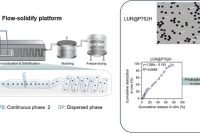
开发出一体化连续制备平台,实现可控液滴形成与超快固化的协同整合。
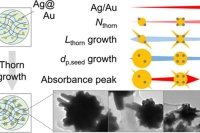
金纳米颗粒(AuNP)具备优异的光学、吸光和产热性能,广泛应用于有机太阳能电池、导电材料、催化剂等领域。
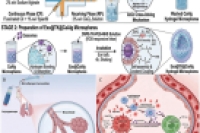
急性肺损伤/急性呼吸窘迫综合征(ALI/ARDS)是由失控性炎症引发的严重临床综合征,以弥漫性肺泡损伤和大量炎症细胞浸润为特征,过量的活性氧与细胞因子释放会进一步加重组织损伤。
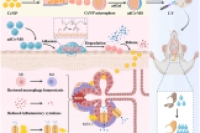
针对口干症现有治疗手段效果有限、副作用明显等问题,南通大学附属医院顾志峰教授、朱玉娟教授团队研发出一种基于微流控技术的口腔粘膜粘附性纳米酶微球系统(adCe-MS),为干燥综合征相关口干症的治疗提供了新型靶向策略。
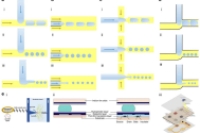
本文全面综述液滴微流控技术制备高价值天然微球的最新进展。
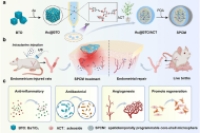
该研究提出一种新型时空响应性压电微球治疗平台,可应用于超声引导下的子宫内膜再生与生育功能恢复。